Szövet-nátrium tárolása: bizonyíték a vese-szerű extrarenalis ellenáramú rendszerekre?
Lucas H. Hofmeister
1 klinikai farmakológiai osztály, Vanderbilt University School of Medicine, Nashville, Tennessee, USA
Stojan Perisic
2 Interdiszciplináris Klinikai Kutatóközpont és Nefrológiai és Hipertónia Osztály, Universitätsklinikum Erlangen és Friedrich-Alexander Universität (FAU) Erlangen-Nürnberg, Németország
Jens Titze
1 klinikai farmakológiai osztály, Vanderbilt University School of Medicine, Nashville, Tennessee, USA
2 Interdiszciplináris Klinikai Kutatóközpont és Nefrológiai és Hipertónia Osztály, Universitätsklinikum Erlangen és Friedrich-Alexander Universität (FAU) Erlangen-Nürnberg, Németország
Absztrakt
A szöveti elektrolit és a víz összetételének kémiai elemzéséből származó legfrissebb bizonyítékok azt mutatták, hogy a test Na + tartalma a kísérleti állatokban nem állandó, nem mindig egyensúlyozódik könnyen a vízzel, és nem szabályozható kizárólag a vese vértisztítási folyamatával. Ehelyett nagy mennyiségű Na + tárolódik a bőrben és a vázizmokban. A Na + -tartályok kvantitatív, nem invazív detektálása 23NaMRI-vel arra utal, hogy ez a titokzatos Na + -tárolás nemcsak állatkísérlet, hanem emberben is fennáll. A klinikai vizsgálatok során a szöveti Na + tárolás szorosan összefügg az esszenciális magas vérnyomással. Állatkísérletekben a tartályszövet Na + tartalmának modulálása kiszámítható vérnyomásváltozásokhoz vezet. A rendelkezésre álló bizonyítékok tehát arra utalnak, hogy a Na + tárolásának pato (?) - fiziológiai folyamata akár az emberi egészség és a betegségek szempontjából is releváns lehet.
Az extrarenalis Na + tárolás jelenségét a közelmúltban alaposan áttekintették [29,10,27,30,28]. Úgy gondoljuk, hogy a rendelkezésre álló bizonyítékok újabb áttekintése plágizálná ezeket az összefoglalókat. Ezért röviden kiemeljük a közelmúlt további bizonyítékait, amelyek alátámasztják azt az elképzelést, hogy a vérnyomás szabályozott a bőrben, majd a bőr elektrolitgradiens-képződésével kapcsolatos, még mindig nagyon korlátozott információkra összpontosítunk.
Vérnyomásszabályozás: csak a bőr mélye, és összefügg a bőr elektrolit anyagcseréjével?
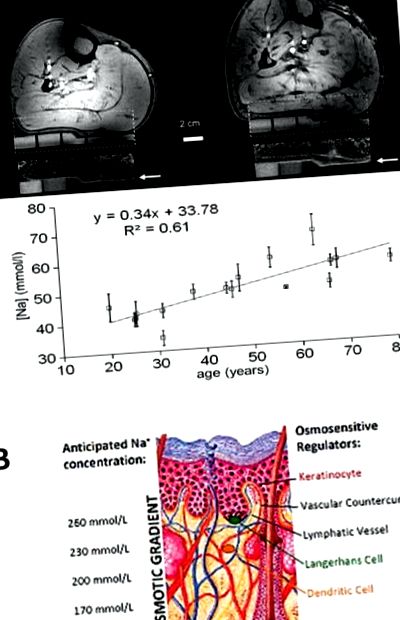
Panel A. 1 H/23 Na MR képek emberi borjú bőréről. Balra: 1H kép (felső és 23Na MR kép (alsó) egy 25 éves férfi alsó végtagjáról. Jobbra: ugyanaz a képalkotó eljárás 67 éves férfiban. A 7T erős térerősségénél a bőr ( nyilak) nagyon jól körülhatárolhatók a 23Na MRI felvételeken, amelyek az agaróz gél standardokat is mutatják növekvő Na + tartalommal (fehér). A Na + elsősorban az epidermiszben vagy közvetlenül az alatt van felhalmozódva. Mennyiségi elemzés azt mutatja, hogy a sótárolás ebben az epidermiszben/a szubepidermális réteg az életkor előrehaladtával növekszik. Linz és mtsai. [Ref. 16] engedélyével adaptálva. B. panel. Javasolt elektrolitkoncentráció a bőr ellenáramú rendszerében. A keratinociták Na + -t pumpálnak a dermisbe, megnövekedett Na + koncentrációt hozva létre. a dermális papilla tetején, ahol a Langerhans-sejtek és a dendritikus sejtek laknak. A dermális papillát vér-érrendszeri ellenáramú rendszerrel infundálják, amely tovább koncentrálja az intersticiális elektrolitokat a dermális papillában és egy elvezető nyirok-kapilláris rendszerrel amely a nyirokelvezetés révén csökkenti az intersticiális elektrolitokat. A különböző rétegekben elhelyezkedő, eltérő elektrolitkoncentrációjú immunsejtek a bőr elektrolit homeosztázisának fiziológiai szabályozói lehetnek.
Bár ezek a részletek arra utalnak, hogy a bőr „vese-szerű” ellenáram-rendszerként működhet, meglepő módon nem végeztek fiziológiai vizsgálatokat az ellenáramú elektrolitkoncentrációról a bőrben. Itt felhasználjuk a rendelkezésre álló szűkös információkat a bőr elektrolit-eloszlásának mikroanatómiájáról, amely véleményünk szerint alátámasztja azt a hipotézist, miszerint a bőr funkcionális ellenáram-rendszerként működik. Az ellenáramú mechanizmus lehetővé teheti a bőr számára a saját mikrokörnyezetének differenciált irányítását, létrehozva egy hiperosmolális biológiai akadályt, amely megakadályozza az intersticiális folyadékvesztést, ahogy Taylor és munkatársai korábban javasolták [32,33].
Adatok kiválasztása
Megvizsgáltuk az irodalmat a bőr elektrolitkoncentrációjának rendelkezésre álló mérésére a bőr keratinocita rétegében és alatt. Wei és mtsai. elemzett eloszlást tanulmányozott a tengerimalac bőrében röntgenanalízissel, pásztázó elektronmikroszkóppal, és adatokat szolgáltatott az epidermisz és a dermis Na +, K + és klórszintjéről. A szerzők jelezték, hogy „a mikroszkóp oszlopban előforduló klórozott szénhidrogének szennyezhetik a mintákat a röntgen mikroanalízis során.” [34] Ezért nem vettünk fel kloridadatokat, és modellelemzésünket Na + és K + -ra korlátoztuk. Később összehasonlítható Na + és K + gradiens képződést figyeltek meg az emberi bőr vizsgálata során [33,7,1,18]. Feltételezzük tehát, hogy a kiválasztott adatok reprezentatív mintát nyújthatnak az emlõs bõr elektrolitgradiensének kialakulásához.
Adatok bemutatása, modellgenerálás és korlátozások
A bőr Na + és K + tartalmának elektronszondás elemzése nem tehet különbséget intracelluláris vagy extracelluláris mikrokörnyezet között. Az epidermiszben a potenciális Na + és K + gradiens képződés energetikai aspektusainak megkísérlésével három egyszerűsített elméleti modellt alkottunk a bőr elektrolit összetételéről (2A. Ábra). Általános feltételezés, hogy az öt mért bőrréteg (stratum corneum, stratum granulosum, stratum spinosum, stratum germinativum és dermis) négy egymást követő bináris alrendszert képvisel, amelyeket elméleti féligáteresztő membránok választanak el egymástól (2B. Ábra). Modellünk feltételezi, hogy az összes szomszédos réteg ideális oldószerként vizet tartalmaz, amelyben a Na + és a K + könnyen egyensúlyba hozhatók. Wei és mtsai az epidermális elektrolittartalom mikroanatómiai eloszlását mmol/kg nedves szövet tömegében mérték meg [34]. Ahhoz, hogy ezeket az elektrolittartalom-méréseket az epidermális rétegek elektrolitkoncentrációjának közelítőibe vigyük át, három különböző modellt használtunk.
Az A panel a bőr hisztomorfológiai entitásait jeleníti meg, a rétegek megfelelő vastagságával (referenciaként [25] adaptálva, engedéllyel). B panel - olyan modellek, amelyek nagyban befolyásolják a bőrrétegek kolligatív tulajdonságait. 1. modell - mind a két réteget ideális megoldásnak tekintik. 2. modell - a rétegben lévő szilárd anyag a réteg térfogatának 50% -át teszi ki, az ideális megoldás kitölti a második felét. 3. modell - az epidermális rétegek ideális megoldásként viselkednek, míg a dermis 50% szilárd anyagból és 50% ideális oldószerből áll. C panel - a B panelen bemutatott modellekből és a fagyasztva szárított bőrrészekben végzett mérésekből származó javasolt K + és Na + koncentrációk. Az eredeti mérések Wei és munkatársai, referencia [24].
1. modell feltételezi, hogy a bőr minden mért rétege egy idealizált oldószert jelent. Az eredeti adatokat használjuk fel, amelyeket mmol/kg szövetben adtunk meg, és mmol/dm 3 folyadékként fejezzük ki az egyes mért rekeszekben (2B. Ábra). A modell nem tehet különbséget a Na + és K + koncentrációk közötti különbségek között az egyes rétegek intra- és extracelluláris terében. Nem veszi figyelembe a folyadékterek intracelluláris vagy extracelluláris szétválasztását, és ezáltal azt is elhanyagolja, hogy az oldott anyag ozmotikus hajtóerő létrehozásának hatékonysága eltérhet (jellemzően a reflexiós együtthatóval indexálva). Mivel ez a modell elhanyagolja a szilárd anyag jelenlétét a sejtekben és az extracelluláris mátrixban, alábecsüli a tényleges elektrolit-koncentrációt a víztérben. Összehasonlítható feltételezéseket tettek korábban Warner et al. [32,33].
Az 1. modellel ellentétben, 2. modell emellett figyelembe veszi, hogy a sejtek és az extracelluláris mátrix vízből és szilárd anyagból áll. Feltételezi, hogy mindkét réteg 50% szilárd anyagot és 50% vizet tartalmaz, amely egy idealizált oldószer, ahol az összes Na + és K + feloldódik és könnyen egyensúlyba kerül. Az 1. modellhez hasonlóan a rétegeken belül nincs megkülönböztetés az intracelluláris és az extracelluláris tér között. A modell ismét nem veszi figyelembe a folyadékterek intracelluláris vagy extracelluláris rekeszizálódását, és figyelmen kívül hagyja a reflexiós együtthatók lehetséges eltéréseit. Az 1. modellel összehasonlítva ezért ezt a modellt a Na + és K + koncentráció kétszeres növekedése jellemzi az idealizált oldószerben (2B. Ábra).
Hasonló az 1. modellhez, 3. modell feltételezi, hogy az epidermális keratinocita rétegek mindegyike idealizált oldószert jelent szilárd anyag nélkül. A 2. modellhez hasonlóan az extracelluláris mátrixban gazdag dermis 50% szilárd anyagot és 50% oldószert tartalmazna. Nincs megkülönböztetés az intracelluláris extracelluláris tér, a víz vagy az elektrolit kompartmentalizációjának elhanyagolása között.
Gibbs energia számítása
Először arra kerestük a választ, hogy a Wei és mtsai által mért elektrolitkoncentrációkat okozhatja-e az elektrolitok passzív felhalmozódása a bőrben, vagy egy aktívan kialakult gradiens. Ehhez úgy véltük, hogy a Gibbs-energia (ΔG 0, 1. egyenlet) jelzi a rendszerben tárolt energiát.
ahol ci az elektrolit moláris koncentrációja (molaritás) az 1 (′) és a 2 (″) bináris rétegekben,
A tökéletesen nem szelektív membránok ekvivalens rNa-t és rK-t eredményeznek. Ez a kapcsolat azokra a testfolyadék rétegekre vonatkozik, amelyekben a Na + és K + ionok aránya ekvivalens, ezért ΔG 0 megközelíti a nullát. Ezt az állapotot ideális Donnan-egyensúlynak nevezik, és úgy értelmezik, hogy az elválasztás membrán-nem szelektív. Azoknál a sejteknél és szöveteknél, amelyek aktív Na + és K + szelekciót hajtanak végre a membránokon, a Gibbs-energia változása nem nulla. A ΔG 0 pozitív változása tehát egy olyan rendszert mutat, amely nem egyensúlyi állapotban van, és energiabevitelt igényel a különbség fenntartásához. Amint itt látható, a bőr elektrolit eloszlása a Gibbs-energia pozitív változását eredményezi minden modellben a germinativum rétegből a dermisbe történő átmenetkor (3. - 5B. Ábra). Ez arra utal, hogy az epidermisz/dermis bináris rendszer elektrolitgradiensét aktív transzporttal hozták létre. Közel nulla ΔG 0 értéket figyelünk meg a bőr felső rétegeiben, ahol az eredetileg életképes epidermális sejtek leereszkednek, és nagy valószínűséggel elveszítik képességüket az elektrolitok aktív szállítására.
(A) mutatja a Na + és a K + (mmol/dm 3) hozzávetőleges moláris koncentrációját az epidermális rétegekben (s. corneum, s. granulosum, s. spinosum és s. germinativum), a dermiszben és a plazmában. (B) a Gibbs-energia változását (kJ/mol) mutatja a bőrrétegeken és a plazmán. (C) ábrázolja a [Na +] vagy [Na + + K +] cellaelem-potenciálját mV-ban az (A) grafikonon bemutatott értékekből számítva, az 1. modellünkből származtatva. (D) az 1. modell által meghatározott körülmények szerint számított ozmotikus nyomást ábrázolja.
(A) mutatja a Na + és a K + (mmol/dm 3) hozzávetőleges moláris koncentrációját az epidermális rétegekben (s. corneum, s. granulosum, s. spinosum és s. germinativum), a dermiszben és a plazmában. (B) a Gibbs-energia változását (kJ/mol) mutatja a bőrrétegeken és a plazmán. (C) a [Na +] vagy [Na + + K +] cellaelem-potenciálját mutatja mV-ban, az (A) grafikonon bemutatott értékekből számítva, a 3. modellünkből származtatva. (D) a 3. modell által meghatározott feltételeknek megfelelő számított ozmotikus nyomást ábrázolja.
Elektromos potenciál kiszámítása
Míg a Gibbs-energia kiszámítható az ionok mérhető arányaiból, az általánosabb gyakorlat az elektromos potenciál mérése. Ezért a Goldman-egyenletet (2. egyenlet) használtuk a rétegek közötti elméleti elektromos potenciálkülönbség kiszámításához az 1–3 modellek koncentrációinak felhasználásával.
ahol F = 96500 C mol z = töltés [C] P = relatív permeabilitás
Modelljeinkben feltételezzük, hogy az egyes ionok relatív permeabilitása ekvivalens, és ezért P = 1 mind Na +, mind K + esetén. A keratinocitákban a Na + transzport releváns a germinativum réteg elektrolitgradiens generációja szempontjából [37]. Ezért figyelembe vettük a pusztán a nátriumeloszlás okozta elektromos potenciált, valamint a nátrium- és káliumeloszlás okozta potenciált. Amint az a parcellákon látható (3. - 5C. Ábra), a germinativum/dermis réteg körülbelül 50 mV elektromos potenciált generálhat, a negatív jel a szérumra utal. Ezt az eredményt támasztják alá transzkután elektromos potenciálok kísérleti mérései, amelyeket Barker és munkatársai végeztek tengerimalacokban [1]. Ezt jelzésnek vesszük, hogy a bőr elektrolit/víz arányának kezelése ezekben a modellrendszerekben fiziológiailag releváns eredményt ad.
Oszmotikus nyomás kiszámítása
Az ozmotikus nyomások kiszámításához a Morse-egyenletet használtuk a disszociálható elektrolitok ideális megoldásához:
ci - elektrolit moláris koncentráció (molaritás), R - univerzális gázállandó, T - hőmérséklet, i - dimenzió nélküli Van’t Hoff-faktor.
A számítások a következő további feltételezéseken alapulnak: a Na + és a K + összege megközelíti az ideális megoldásban jelenlévő kationok teljes számát. Két szomszédos réteg mindegyik bináris rendszere egyensúlyi állapotban van. Az elektromos gradiens képződését elhanyagolva azt is feltételezzük, hogy a Na + és a K + egyenlő számú megfelelő monovalens aniont kísér, ami az ozmoliták ideális disszociációját eredményezi a következő módon:
Következtetések
(A) mutatja a Na + és a K + (mmol/dm 3) hozzávetőleges moláris koncentrációját az epidermális rétegeken (s. corneum, s. granulosum, s. spinosum és s. germinativum), a dermisben és a plazmában. (B) a Gibbs-energia változását (kJ/mol) mutatja a bőrrétegeken és a plazmán. (C) a [Na +] vagy [Na + + K +] cellaelem-potenciálját mutatja mV-ban, az (A) grafikonon bemutatott értékekből számítva, a 2. modellünkből származtatva. (D) a 2. modell által meghatározott feltételeknek megfelelő számított ozmotikus nyomást ábrázolja.
Köszönetnyilvánítás
A JT-t a német szövetségi gazdasági és technológiai minisztérium/DLR Forschung unter Weltraumbedingungen (50WB0920), az Interdiszciplináris Klinikai Kutatóközpont (IZKF Junior Kutatócsoport 2), az NIH (RO1 HL118579-01), az AHA (14SFRN20770008), az AHA támogatásával támogatja. ), valamint a National Research for Resources Center 1UL-1RR024975 számú klinikai transzlációs tudományos díját.
- A nátrium-glükóz kotransporter-2 gátlásával járó fogyás gátolja a bizonyítékok áttekintését és
- A korall suttogó fehérítése és szövetvesztése a korallokban - mi; s a Különbség
- A vese étrend nátrium megértése
- Használja a nátriumot, hogy teljes, érrendszeri és szakadt izom legyen; Fitness
- Az étrendi nátrium és az alacsony sótartalmú étrend egészségre gyakorolt hatása