A garcinolban dúsított frakció ízületi gyulladáscsökkentő hatása az adjuváns által kiváltott ízületi gyulladással szemben
Purnima Warriar
1 SPP- Gyógyszerészeti és Technológiai Menedzsment Iskola, SVKM NMIMS, V.L. Mehta Road, Vile Parle (W), Mumbai400056, Maharashtra, India
Kalyani Barve
1 SPP- Gyógyszerészeti és Technológiai Menedzsment Iskola, SVKM NMIMS, V.L. Mehta Road, Vile Parle (W), Mumbai400056, Maharashtra, India
Bala Prabhakar
1 SPP- Gyógyszerészeti és Technológiai Menedzsment Iskola, SVKM NMIMS, V.L. Mehta Road, Vile Parle (W), Mumbai400056, Maharashtra, India
Társított adatok
Absztrakt
Háttér:
A Garcinia indica, más néven kokum, a hagyományos orvostechnikai rendszerben gyulladás és reumatikus fájdalmak enyhítésére szolgál. A garcinolról, amely a gyümölcshéjából nyert benzofenon, gyulladáscsökkentő hatása van az arachidonsav-anyagcsere modulálásával, az iNOS expressziójának elnyomásával, az NF-KB aktivációval és a COX-2 expresszióval. Antioxidáns és rákellenes aktivitást is vizsgáltak. Ezeken kívül kevés szabadalom állítja, hogy a garcinol elhízásgátló és hepatoprotektív hatással is rendelkezik, és potenciálisan alkalmazható vesebetegségek, endometriózis és szívműködési zavarok kezelésére.
Célkitűzés:
A Garcinia indica gyümölcshéjából származó garcinol-dúsított frakciónak (GEF) hatékonynak kell lennie az ízületi gyulladás kezelésében, amely a krónikus gyulladásos rendellenességek egyike, gyulladáscsökkentő tulajdonsága miatt, amint azt a korábbi kísérletek jelezték.
Mód:
A GEF-t a Garcinia indica gyümölcs héjából készítettük, és LC-MS/MS alkalmazásával számszerűsítettük. Megállapították, hogy 89,4 tömeg% garcinolt tartalmaz. A GEF-t 10 mg/kg dózisban értékelték a teljes Freund-adjuváns (CFA) által kiváltott ízületi gyulladással szembeni hatékonyságára Wistar albínó patkányokban. Mindkét oldal mancstérfogatát Plethysmometerrel mértük, és a testtömeget 0., 1., 5., 12. és 21. napon regisztráltuk. A hiperalgéziás reakciót motilitási és lépcsőmászási teszttel is mértük.
Eredmények:
A GEF a mancs duzzadásának jelentős csökkenését mutatta (p Kulcsszavak: Benzofenon, teljes Freund-adjuváns, Garcinia indica, gyulladás, kokum, rheumatoid arthritis
1. BEMUTATKOZÁS
A Kokum gyümölcsök 23-26% zsírt tartalmaznak, amelyet kereskedelmi és orvosi célokra használnak fel. A gyümölcs héja fehérjéket, tanninokat, pektineket, cukrokat, szerves savakat, például (-) hidroxi-citromsavat, hidroxi-citromsav-laktont és citromsavat tartalmaz; antocianinok, például cianidin-3-glükozid és cianidin-3-sambubiózid; valamint poliizoprenilezett fenol-garcinol és izogarcinol [2]. A hidroxi-citromsav, a gyümölcs héjának egyik alkotóeleme, potenciális elhízás elleni szer [11]. A Kokum pigmentek képesek elnyelni az UV fényt. A kozmetikai iparban napvédő krémek és paszták gyártásához használják. Ugyanazok az antocianin pigmentek színüket vörösről kékre/lilára változtatják, amikor a pH-érték meghaladja az 5-öt. Ez a tulajdonság felhasználható a pH-érzékeny indikátorok készítéséhez [12]. A gyümölcs kérge számos élelmiszer- és élelmiszer-készítményben természetes természetes színezékforrás lehet [1].
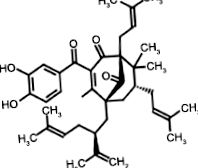
Ábra. ( 1 1 ) a garcinol kémiai szerkezetét ábrázolja. Nyilvánvaló, hogy a ketoncsoport, a hidroxilcsoportot tartalmazó fenilgyűrű és az izoprenilcsoport kettős kötése biztosítja az oxidációs helyeket. Ezenkívül a hidrofób természetű izoprenil-lánc biztosítja a biológiai célpontokhoz való kapcsolódás helyét [23, 24]. A garcinolt prenilezett kalkonnak tekinthetjük, amely két aromás gyűrűt tartalmaz, amelyeket karbonilcsoportok választanak el egymástól, és szerkezetileg hasonlóak a kurkuminnal kinyitáskor. A jelentések szerint a szintetikus kalkonok gyulladáscsökkentő hatást mutatnak [25].
A garcinol szerkezete.
Egy olyan növénynek, mint a Garcinia indica, amelynek garcinol van, gyulladáscsökkentő és antioxidáns rész, kedvező biológiai hozzáférhetőséggel, alkalmaznia kell a reumás ízületi gyulladás kezelésében. Ezenkívül a hagyományos rendszer gyulladás és gyulladásos rendellenességekkel, például reumás fájdalommal járó tünetek kezelésére írja elő. Ezért ezt a vizsgálatot a garcinollal dúsított frakció gyulladáscsökkentő hatásának értékelésére végezték rheumatoid arthritisben.
2. ANYAGOK ÉS MÓDSZEREK
2.1. Üzem neve és használt alkatrészei
A Garcinia indica friss gyümölcseit Dr. Badhe Waadi-tól (Phoolpada Road, Virar (Kelet)) szerezték be, és hitelesítésüket az Agharkar Research Institute-tól (Pune, Maharashtra, India) szerezték be.
2.2. Kémiai vegyületek
A standard garcinolt a Cayman Chemical Company-USA-tól szerezték be. A metanolt (HPLC minőségű) az SD Fine Chemical Limited-től (Mumbai, India) vásároltuk. N-hexánt, toluolt, etil-acetátot, hangyasavat és egyéb vegyszereket a Loba Chemie-től (Mumbai, India) vásároltak.
2.3. Kivonás
700 g levegőn szárított gyümölcshéjport extraháltunk hexánnal Soxhlet készülékkel 72 órán át. Az extraktumot rotációs vákuumban bepároljuk, így 10 g pépes masszát kapunk. Ezt a kivonatot fitokémiai szűrővizsgálatnak vetettük alá, hogy kimutassuk a különböző fitokomponensek jelenlétét.
2.4. Frakcionálás és a dúsított frakció LC-MS/MS elemzése
Az extraktumot (9 g) szilícium-dioxidon adszorbeáltuk és szilícium-dioxid-oszlopra töltöttük (100-120 mesh méretű). N-hexán-etil-acetát (1: 0 - 0: 1) gradiens elúciója négy fő frakciót eredményezett, az A, B, C, D frakciókat. Mind a négy frakciót vékonyréteg-kromatográfiának vetettük alá, álló helyzetű GF254 szilikagéllel., Toluol: etil-acetát: hangyasav (4: 1: 0,5) mozgófázisként, vanillin-kénsav permetező reagensként és standard garcinol referencia-standardként. Az n-hexán: etil-acetát (0,95: 0,05) C-frakciója (800 mg) a garcinol maximális koncentrációját mutatta. A dúsított frakciót LC-MS/MS (Shimadzu LC-MS 8040) alkalmazásával metanollal oldószerként értékeltük a garcinol tartalmára. asztal 1 1 megadja az LC-MS/MS elemzés részleteit. Ezt a garcininnal dúsított frakciót használták állatkísérletekben, és ezentúl GEF-nek nevezik.
Asztal 1
| Áramlási sebesség | 10µl |
| Mobil fázis | Metanol: víz (0,1% hangyasav), 80:20 |
| Nebulizáló gáz (N2) áramlása | 3,0 liter/perc |
| Szárítógáz (N2) áramlása | 15,0 l/perc |
| Hőblokk hőmérséklete | 400 ° C |
| DL (deszolválás) hőmérséklet | 250 ° C |
| Az ionizálás módja | Pozitív |
| Ionizációs szonda | ESI |
| Szkennelési módok | Q1 Scan |
2.5. Állatok
180-200 g közötti Wistar hím patkányokat a Bharat szérumból (Thane, Maharashtra, India) szereztünk be. Valamennyi állatot ketrecbe helyeztük és normál környezeti körülmények között [23 ° C + 5, 60% + 5 relatív páratartalom és 12: 12 órás sötét és világos ciklus] tartottuk, normál étrenddel etettük, és az ivóvízhez szabad hozzáférést biztosítottunk a akklimatizáció (egy hét).
2.6. Patkány adjuváns ízületi gyulladás és kezelési rend létrehozása
Adjuváns ízületi gyulladás (AA) patkány modellt 0,1 ml komplett Freund adjuváns (CFA) egyszeri befecskendezésével dolgoztunk ki, amelyet Sigma Aldrich-től (Mumbai, India) szereztünk be. a bal hátsó mancs altalpiája a leírás szerint [35].
A patkányokat négytagú csoportokra osztottuk, amelyek mindegyikében hat állat volt
I. csoport - normál kontroll, II. Csoport - betegség elleni védekezés, III. Csoport - pozitív kontroll (diklofenák-nátrium, 10 mg/kg) és IV. Csoport - GEF (10 mg/kg).
A 0. naptól a 12. napig a IV. Csoportba tartozó AA patkányokat GEF-vel (10 mg/kg, p.o.) és a III. Csoportban diklofenak-nátriummal (10 mg/kg, p.o.) kezeltük naponta egyszer. A normál és a betegség kontroll csoportok egyidejűleg vivőanyagot kaptak. A 13-21. Napon az állatokat nem adagolták, de a paraméterek monitorozását folytatták.
2.7. Az ízületi gyulladás duzzadásának értékelése
A bal hátsó mancs térfogatát elektronikus víz-pletiszomométerrel mértük a 0., 1., 5 12., 16. és 21. napon, jelezve az elsődleges elváltozást és a terápiás szerek hatását ebben a fázisban. A jobb hátsó mancs térfogatát is mértük, hogy megértsük a másodlagos elváltozások súlyosságát. A vizuális ízületi gyulladás indexét mértük az AA súlyosságának értékelésére. Ehhez a patkányokat vizuálisan megvizsgálták a fül, az orr, a farok, az elülső és a hátsó mancs gyulladásos elváltozásainak jelenlétére vonatkozóan, és az ízületi gyulladás súlyosságát értékelték. A mancsot, a fület, az orrot, a szemet és a farokot külön osztályozták, a kumulatív pontozás pedig a vörösségtől, duzzanattól és a csomók jelenlététől/hiányától függ [35]. A megfigyeléseket az vette nyilvántartásba, aki vak volt a vizsgálattal szemben.
2.8. A testtömeg mérése
Az összes állat testtömegét a 0., 1., 5., 12., 16. és 21. napon mértük.
2.9. Lépcsőmászó teszt
Az állatokat egy héten át arra oktatták, hogy felmászhassanak a fa lépcsőkre, a megfigyelő ketrecbe helyezve, 3 lépésben 5, 10 cm és 15 cm magasan, a második lépésben vizet, a harmadikban élelmet. A mászóképesség 0-ra került, ha a patkány nem mászik; 1. ha a patkány felmászik az 1. lépésre; 2, ha a patkány felmászik az 1. és 2. lépésre; 3, ha a patkány felmászik az 1., 2. és 3. lépésre. Ezt a tesztet a CFA injekciót követő 0., 1., 5., 12., 16. és 21. napon hajtották végre.
2.10. A motilitási teszt értékelése
Minden állatot egy héten át képeztek egy fadobozban a motilitási vizsgálat céljából. Minden patkány motilitását a CFA injekciót követő 0., 1., 5., 12., 16. és 21. napon hajtottuk végre. Az állatok mozgékonyságát 5 percig figyeltük meg egy megfigyelő ketrecben. Ha a patkány lefekszik, a motilitási mintát 0-ra értékeltük; 1, ha a patkány mászik; 2 ha a patkány jár; 3, ha a patkány némi nehézséggel fut és mászik, és 4, ha a patkány jól fut és mászik [36, 37].
- A test összetétele fiatalkori idiopátiás ízületi gyulladásban szenvedő gyermekek étrendi bevitelének
- A mérési hibák elszámolása a levegőszennyezés omikus jelekre gyakorolt hatásának felmérésére
- A véralvadás és a köpölyözés mellrákkal kapcsolatos lymphedema adjuváns terápiájaként
- 7 oka a fogyásnak a pikkelysömör ízületi gyulladásával
- 10 meglepő tény az ízületi gyulladásról