Helicobacter pylori és gyomorsav: intim és kölcsönös kapcsolat
Helge L. Waldum
Rákkutatás és Molekuláris Orvostudományi Tanszék, Norvég Természettudományi és Technológiai Egyetem, Orvostudományi Kar, Trondheim, Norvégia
Per M. Kleveland
Rákkutatás és Molekuláris Orvostudományi Tanszék, Norvég Természettudományi és Technológiai Egyetem, Orvostudományi Kar, Trondheim, Norvégia
Øystein F. Sørdal
Rákkutatás és Molekuláris Orvostudományi Tanszék, Norvég Természettudományi és Technológiai Egyetem, Orvostudományi Kar, Trondheim, Norvégia
Absztrakt
A Helicobacter pylori (Hp) a gasztritisz, a peptikus fekélybetegség és a gyomorrák fő oka. Még mindig megválaszolatlan kérdések vannak a Hp és az ember közötti kölcsönhatással kapcsolatban, például arról, hogy mi határozza meg a kezdeti fertőzés iránti hajlamot és a karcinogén hatás mechanizmusait. Úgy tűnik, hogy a kezdeti fertőzés időbeli gyomorsavtartalmat igényel. Ahhoz, hogy a Hp fennmaradjon a gyomor nyálkahártyájának rétegében, némi savtartalom szükséges. Maga a Hp valószínűleg nem közvetlenül rákkeltő. Csak akkor, ha hiposzavtartalmú oxyntikus nyálkahártya-gyulladást és atrófiát vált ki, a Hp hajlamosít a gyomorrákra. A gasztrin nagy valószínűséggel központi szerepet játszik a nyombélfekély és a gyomorrák Hp-patogenezisében.
A filogenezis során megmaradt a sav termelése a gyomor-bél traktusban [Johnsen, 1998], tükrözve a gyomornedv fő funkciójának fontosságát; vagyis a lenyelt mikroorganizmusok megölése [Wilder-Smith és mtsai. 1992]. A normál gyomornedv ellenséges környezetet teremt a mikroorganizmusok számára, így a gyomor és a vékonybél luminális tartalma viszonylag steril lesz. A gyomornyálkahártya-gyulladás néhány évtizeddel ezelőtt olyan elterjedt volt [Siurala és mtsai. 1968], hogy a gyomorhurutot még az öregedés természetes következményének is tekintették. Azt azonban meglehetősen korán felismerték, hogy a gyomorhurut összefügg a gyomorrákkal, mivel a gyomorrák csak a gyomor gyulladásában alakult ki [Morson, 1955]. Nagy áttörést jelentett tehát, amikor bebizonyosodott, hogy a Helicobacter pylori (Hp) fertőzés a gasztritisz fő oka [Marshall és Warren, 1984]. Habár több mint 25 év telt el azóta, hogy a Hp központi szerepet játszott a felső gasztrointesztinális betegség patogenezisében, még mindig vannak megoldatlan kérdések a Hp és a gazda közötti interakcióval kapcsolatban, mint például a karcinogén hatás mechanizmusa és a Hp-re való hajlam fertőzés. Ennek a cikknek a tömör áttekintése a Hp és az emberek közötti kölcsönhatások áttekintése.
Helicobacter pylori által okozott akut fertőzés
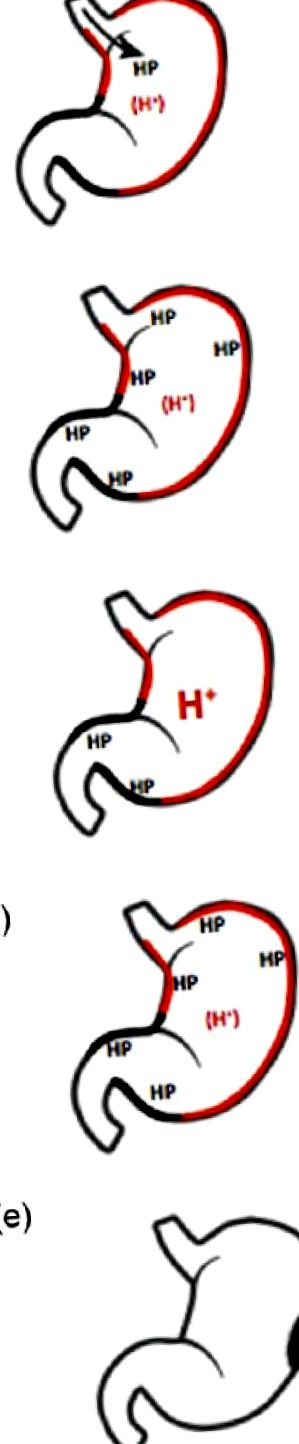
A Helicobacter és a gyomorsav kapcsolatának különböző fázisai.
a) A kezdeti fertőzést a gyomorsav csökkenése segíti elő. (b) A kezdeti fertőzés a gyomor savasságának csökkenését okozza. (c) Bár a fertőzés továbbra is fennáll, a gyomorsav valamilyen okból vagy a másik miatt helyreáll. (d) Amikor a Hp-fertőzés az oxyntikus mirigyek atrófiáját okozza, a gyomorsav-szekréció csökken. (e) Ha az oxyntikus atrófia olyannyira hangsúlyos, hogy a gyomor elégséges savtartalma nem érhető el, hypergastrinemia alakul ki, és a beteg egyidejűleg hajlamos a gyomorrákra.
Így a gyomorsavnak valószínűleg védő szerepe van a kezdeti Hp-fertőzés elleni védekezésben. A gyomorsav-szekréció gátlóinak alkalmazása kisgyermekeknél, amelyekről a közelmúltban beszámoltak a Clostridium-fertőzés hajlamáról [Nylund et al. 2014] szintén hajlamosabbá teheti ezeket a gyermekeket a Hp-fertőzésre.
A hipo-savasság mechanizmusai a kezdeti fertőzés során
Az akut Hp gyomorhurut vagy járványos hipoklorhidria lefolyása, amelyet szinonimával használnak, hetekig vagy hónapokig tarthat [Marshall és mtsai. 1985; Morris és Nicholson, 1987; Ramsey és mtsai. 1979]. A Hp-fertőzés akut fázisában a gyomorsav csökkenésének hátterében álló mechanizmus nem ismert, de magának a Hp-nek és a gyulladásnak, amelyet ez a fertőzés kivált, azok tulajdonságai felmerültek [Calam, 1995] [1. ábra (b)]. Így a Hp-fertőzés citokinek, például interleukin (IL) -1β termelését indukálhatja [Noach és mtsai. 1994] gátló hatást gyakorol a gyomorsav-szekrécióra [Wallace és mtsai. 1991]. A Hp által a savszekrécióra gyakorolt közvetlen hatást izolált parietális sejtekben végzett vizsgálatok támasztják alá [Cave és Vargas, 1989]. Az akut fertőzés során a gyomor savasságának csökkentésében szerepet játszó Hp-eredetű faktorok közé tartozik az NH3, a zsírsavak vagy a H +/K + -ATP-aszé gátló hatású anyag [Calam, 1995]. Több mint 20 éve bebizonyosodott, hogy a Hp és a Hp által termelt zsírsavak blokkolják a H +/K + -ATP-asét [Beil és mtsai. 1994] és nemrégiben, hogy a Hp elnyomja a protonpumpa expresszióját is [Saha et al. 2010]. Egyes, a gyulladás által felszabadított citokinek szintén nagy hatással lehetnek a savszekrécióra [Saperas és mtsai. 1990].
Átmenet krónikus fertőzésre
Nem tudjuk biztosan, de az uralkodó hipotézis szerint a fertőzés után a Hp gastritis krónikussá válik; ha nem, akkor a Hp-t kezeléssel irtják ki. Az akut és a krónikus gyomorhurut közötti átmenet a gyomorsav-szekréció helyreállításával jár [Ramsey és mtsai. 1979; Morris és Nicholson, 1987]. Hogy mi történik a gyomorban ebben a fázisban, nem ismert. Sőt, hogy miért egyes betegeknél a fertőzés az antrális nyálkahártyára korlátozódik, míg másoknál a pan-gastritis jelentkezik, nem tudni, bár a nyálkahártya savasságának különbségei szerepet játszhatnak. A gyomorsav-szekréció gátlása által okozott fertőzés orális terjedése [Logan et al. 1995] arra is utal, hogy a helyi savasság szerepet játszik a Hp-fertőzés eloszlásában.
A spirális forma és a flagella elősegíti a Hp behatolását a nyálkahártyába [Calam, 1995], ahol pH-gradiens van a luminalis oldalról diffundáló H + és a HCO3 - a hámsejtek miatt. A Hp a boldoguláshoz egy közeli semleges pH-értéktől függ; a Hp ureázaktivitása [Marshall és mtsai. 1990] növeli a pH-értéket a környéken, ezáltal lehetővé téve a Hp túlélését egy savasabb helyen. Sok szempontból az enyhén savas miliő ideális a Hp növekedéséhez, mivel NH3-termelése különben túl lúgos környezetet indukálhat a baktérium számára [Scott és mtsai. 1998].
Beszámoltak arról, hogy az antrális Hp fertőzésnek trofikus (pozitív vagy negatív) hatása lehet a G és különösen a D sejtekre [Moss és mtsai. 1992], amely várhatóan semleges pH mellett is befolyásolja a gasztrin felszabadulását. Ebben az összefüggésben emlékeztetni kell arra, hogy a neuroendokrin (NE) sejtek hosszú élettartammal rendelkeznek [Fossmark et al. 2005], és így bármilyen hatás hosszú ideig fennmaradhat a Hp felszámolása után. A trofikus hatásokat az ammóniummal történő lúgosítás krónikus hatásai okozhatják. Ezért nehéz kizárni a jelen irodalomból, hogy a Hp gasztrin-felszabadulásra gyakorolt hatását nem az ureaz aktivitás okozza. Az, hogy a H + közvetlenül érinti-e a G-sejtet vagy az antrális D-sejtet, még nem rendeződött, de funkcionális szempontból nem fontos. Mind a G-sejt, mind az antrális D-sejt nyitott típusú, és így a gyomortartalom befolyásolja. Ebből valószínű, hogy a G-sejtből származó gasztrin felszabadulást mind a gyomortartalom, mind a D-sejtekből származó szomatosztatin közvetve befolyásolja. A Hp-vel fertőzött betegeknél azonban jelzik az antrális gasztrin növekedését és az antrális szomatosztatin csökkenését [Odum et al. 1994]
Korábban azt feltételezték, hogy a nyombélfekély a gyomor metaplázia foltjain fejlődött ki [Carrick és mtsai. 1989]. A gastrinomában szenvedő betegeknél azonban fekély alakul ki Hp-fertőzés nélkül [Weber és mtsai. 1997], amely azt mutatja, hogy a fokozott savszekréció elegendő a peptikus fekélyek kiváltásához. Hozzá kell tenni, hogy a nyombélfekélyben szenvedő betegeknél a vér gasztrinszintjének növekedése kicsi [Lanzon-Miller és mtsai. 1987] a gasztrin felszabadulásának a gyomor savasságának növekedésével való visszafogása miatt [Walsh és mtsai. 1975] okozta a kis gasztrinszint emelkedés. A gasztrin iránti érzékenység fő fiziológiai hatása, vagyis az ECL sejtből történő hisztamin felszabadulás stimulálása szempontjából nagyon magas [Sandvik és Waldum, 1990]. Ezért a nyombélfekélyben szenvedő betegek többségében nincs hypergastrinemia, de ennek ellenére bizonyos nem megfelelő hypergastrinemia a gyomor savasságához viszonyítva [Smith és mtsai. 1990]. Van egy esettanulmány, amely két gyomorfekélyben szenvedő páciensnél fokozott gyomorsav-szekréciót és mérsékelt hipergastrinémiát ír le, ahol mind a gasztrin, mind a gyomorsav-szekréció normális szintre csökkent a Hp felszámolása után [Metz és mtsai. 1995]. Ennek a két betegnek a gyomor savasságától elvártnál magasabb gasztrin-értékek mechanizmusát nem magyarázták.
A sav hiperszelekciójának mechanizmusa Hp-vel kapcsolatos nyombélfekély esetén
Arra a következtetésre juthatunk, hogy a Hp által kiváltott nem megfelelő hipergastrinémia és a sav hiperszekréció mechanizmusaival kapcsolatos zavartság elsősorban a hosszú életű NE sejteken kiváltott trofikus változásoknak köszönhető. Ezenkívül a gyomorsav-szekréció szabályozásának téves álláspontja ezen tanulmányok többségében szintén hozzájárult a félreértésekhez.
Hp és gyomorrák
Hp és gasztrinóma
A legtöbb gasztrinóma miatt fekélyes páciens nem fertőzött Hp-vel [Weber és mtsai. 1997], bizonyítva, hogy a gyomorsav fokozott szekréciója önmagában elegendő a peptikus fekélyek kiváltására. A gasztrinómák ritkán jelentkeznek felnőttkor előtt [Soga és Yakuwa, 1998], míg a Hp-fertőzés leggyakrabban gyermekkorban fordul elő [Thomas és mtsai. 1999]. A gasztrinómában szenvedő betegeknél a Hp-fertőzések alacsonyabb gyakorisága az életkornak megfelelő kontrollokhoz képest azt jelzi, hogy a megnövekedett gyomorsavasság felszámolhatja a Hp-t.
Hp és hipo-savasság/savasság
A Hp által okozott oxyntikus gyomorhurut korai szakaszában a gyomorsav-szekréció csak mérsékelten csökkenhet, és a Hp felszámolása még bizonyos fokú atrófiában szenvedő betegeknél is fokozhatja a savszekréciót [Tari et al. 2007]. Pan-gastritisben és oxyntikus atrófiában szenvedő betegeknél előfordulhat, hogy a Hp nem mutatható ki [Karnes et al. 1991]. Feltételezzük, hogy a Hp nem élhet ilyen körülmények között. Lehet, hogy a Hp-t más mikroorganizmusok helyettesítik, amelyek ebben a helyzetben élhetnek a gyomorban, vagy alternatív megoldásként a Hp-ureáz által termelt NH3 termel egy helyi közeget, amely túl lúgos a hatóanyag számára a gyomorban, sav nélkül [Marshall et al. 1990]. A savnak a Hp fejlődésének szerepét megmutatják az antibiotikumokkal kombinált savgátlás hatásai a Hp felszámolásában is [Unge és mtsai. 1989], valamint az esetleges orális terjedés a gyomorban a gyomorsav-szekréció gátlóinak kezelése során [Logan és mtsai. 1995]. Érdekes módon a gyomorsav-szekréció új gátlója, a vonoprazan, amely a kálium-kompetitív savblokkolókhoz tartozik, és valószínűleg hatékonyabban gátolja a savszekréciót, mint a protonpumpa-blokkolók, hatékonyabbnak tűnik az antibiotikumokkal együtt a Hp felszámolásában, mint a proton- szivattyú inhibitorok [Murakami és mtsai. 2016].
Következtetés
Megállapítható, hogy a Hp elsődleges fertőzése az időbeli hipo-savasságtól vagy savasságtól függ, de a savasság hosszú ideig fennmarad. Az antral nyálkahártyájában található Hp-fertőzés a nyombélfekélyeket okozza, amelyeket a G-sejtekből származó enyhe fokozott gasztrinkibocsátás miatt másodlagos gyomorsav-szekréció indukál, valószínűleg az ureaz által kiváltott NH3-termelés miatt. A gyulladást okozó oxyntikus nyálkahártya megfertőzésekor a felszíni sejtek funkciói (nyálkahártya és HCO3-termelés) csökkentek, hajlamosítva a gyomor gyomorfekélyére. Az oxyntikus nyálkahártya tartós fertőzése atrófiát és jelentős gyomorsav-szekréciót okoz, ami gyomor hipo-savassághoz és markáns hypergastrinemiához vezet, amely valószínűleg gyomorrákra hajlamosít. A HP nem él túl túl savas (gasztrinómában szenvedő betegek) vagy anacid gyomorban.
A Hp és a gyomor közötti kölcsönhatások nagyon összetettek, de ma már megértettük a legtöbb gyomor- és nyombélbetegség patogenezisét, mivel a Hp ezen állapotok többségében központi szerepet játszik.
Lábjegyzetek
Finanszírozás: Ez a kutatás nem kapott külön támogatást egyetlen finanszírozó ügynökségtől sem az állami, sem a kereskedelmi, sem a nonprofit szektorban.
Összeférhetetlenségi nyilatkozat: A szerzők kijelentik, hogy nincs összeférhetetlenség.
Közreműködői információk
Helge L. Waldum, Rákkutatás és Molekuláris Orvostudományi Kar, Orvostudományi Kar, Norvég Tudományos és Technológiai Egyetem, Trondheim, Norvégia.
Per M. Kleveland, a Norvég Tudományos és Technológiai Egyetem Orvostudományi Karának Rákkutatás és Molekuláris Orvostudományi Tanszék, Trondheim, Norvégia.
Øystein F. Sørdal, a Norvég Tudományos és Technológiai Egyetem Orvostudományi Karának Rákkutatás és Molekuláris Orvostudományi Tanszék, Trondheim, Norvégia.
- A Helicobacter pylori fertőzés kezelése - amerikai családorvos
- Helicobacter Pylori C13 karbamidlégzési teszt - ausztrál klinikai laboratóriumok
- A magas diétás sótartalom súlyosbítja a Helicobacter pylori által kiváltott gyomor karcinogenezis fertőzést
- Helicobacter pylori - tükröződések a következő millenniumi bélben
- Helicobacter pylori fertőzés, atrófiás gyomorhurut és a hasnyálmirigyrák kockázata A populáció alapú