A szív- és érrendszeri mágneses rezonancia kimutatja a károsodott miokardiális perfúziós tartalék és a megnövekedett bal kamrai tömeg progresszióját egerekben, amelyek zsírtartalmú étrendet fogyasztanak
Absztrakt
Háttér
A károsodott szívizom-perfúziós tartalék (MPR) elhízás és cukorbetegség esetén is elterjedt, még obstruktív koszorúér-betegség (CAD) hiányában is, és a nemkívánatos események prognosztikája. Megállapítottuk a csökkent MPR időbeli lefutását és a kapcsolódó vaszkuláris és szöveti tulajdonságok vizsgálatát magas zsírtartalmú étrenddel (HFD) táplált egerekben, mivel ezek az emberi elhízás, a cukorbetegség és a csökkent MPR obstruktív CAD nélküli modelljei.
Mód
A HFD-vel vagy alacsony zsírtartalmú étrenddel (kontroll) táplált C57Bl/6 egereket a diéta utáni 6., 12., 18. és 24. héten készítettük. A kardiovaszkuláris mágneses rezonancia (CMR) protokoll magában foglalta a többszeletes cine képalkotást az ejekciós frakció (EF), a bal kamra (LV) tömegének, az LV falvastagságának (LVWT) és az LV térfogatának felmérésére, valamint az első passzusú perfúziós CMR-t az MPR számszerűsítésére. . Koronária érrendszeri reaktivitást, aorta érelmeszesedést, miokardiális kapilláris sűrűséget és szöveti fibrózist is értékeltünk.
Eredmények
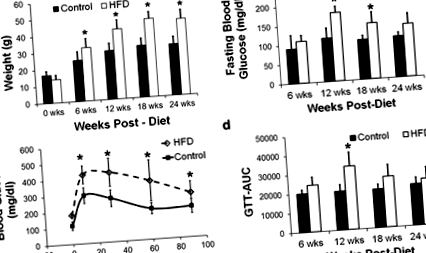
A testtömeg nőtt a HFD egerekben a diéta után 6–24 héttel (o
Háttér
Az iszkémiás szívbetegségek kezelésében több évtizede a szívizom ischaemia és az obstruktív koszorúér-betegség (CAD) egyenértékűek [1]. Ennek megfelelően a miokardiális ischaemia terápiáinak többsége a koszorúér-szűkület eltávolítását célozza. Van azonban egyre több bizonyíték arra vonatkozóan, hogy nem minden ischaemiás betegnek van obstruktív CAD-je, és paradigmaváltást javasoltak [1]. A felmerülő koncepció az, hogy több tényező, beleértve a mikrovaszkuláris betegségeket, a koszorúér-érgörcsöt és más tényezőket, jelentősen hozzájárulhat a szívizom ischaemiájához, és hogy az obstruktív CAD-nak számos lehetséges oka lehet [1]. Valójában tanulmányok kimutatták, hogy a szívizom ischaemia obstruktív CAD hiányában jelentős prevalenciával fordul elő bizonyos betegpopulációkban, beleértve a cukorbetegeket [2], az elhízást [3], a metabolikus szindrómát [4] és a nőket [5].
A miokardiális ischaemia jelenlétét és súlyosságát kvantitatív módon értékelhetjük a miokardiális perfúziós tartalék (MPR) képalkotásával PET vagy kardiovaszkuláris mágneses rezonancia (CMR) alkalmazásával. A csökkent MPR-ről kimutatták, hogy a káros kardiovaszkuláris események prognosztikus és független előrejelzője a szívhalandóságnak obstruktív CAD-vel rendelkező és anélkül szenvedő betegeknél [6]. Egy nemrégiben végzett vizsgálat több mint 1000 cukorbeteg és 1600 nem cukorbeteg alanyon azt mutatta, hogy az obstruktív CAD nélküli, de MPR károsodott diabéteszes betegeknél az események aránya megegyezik a nem diabéteszes betegek korábbi CAD-jával [2]. Obstruktív CAD hiányában az MPR károsodása nagyrészt a mikrovaszkulatúra rezisztencia-edényeinek diszfunkcióját tükrözi. Míg a mikrovaszkuláris diszfunkció csökkent MPR-hez és megnövekedett kardiovaszkuláris kockázathoz vezet, a mikrovaszkuláris diszfunkció hátterében álló mechanizmusok nem teljesen ismertek, és a megfelelő kezelési stratégiák nincsenek kialakítva.
Az egérmodelleket széles körben alkalmazzák a szív- és érrendszeri kutatásokban a mögöttes molekuláris mechanizmusok tanulmányozásához, és a magas zsírtartalmú étrenddel (HFD) táplált egerek az emberi elhízás és a cukorbetegség közös modelljeként jelennek meg. Egy nemrégiben elvégzett tanulmány jellemezte a HFD hosszú távú hatásait az egerek szív- és érrendszerére, és megállapította, hogy a 8–16 hónapig HFD-vel táplált egerek elhízást, hiperglikémiát, hiperinsulinémiát, inzulinrezisztenciát, kardiomiocita hipertrófiát és szív metabolikus rendellenességeket okoznak [7]. Egy másik friss tanulmány CMR-t használt annak kimutatására, hogy a HFD egerekben 20 hetes étrend után diasztolés diszfunkció alakul ki [8]. Ezenkívül nemrégiben első passzusú kontrasztanyaggal fokozott perfúziós CMR-t alkalmaztunk annak bizonyítására, hogy a HFD egerek MPR-t károsítottak a diéta megkezdése után 24 héttel [9]. Ebben a tanulmányban arra törekedtünk, hogy meghatározzuk az idő lefutását és megvizsgáljuk a vaszkuláris és szöveti tulajdonságokat a megnövekedett LV tömeg és a csökkent MPR progressziójának hátterében HFD egerekben.
Mód
Kísérleti terv
Az állatok kezelése
Minden állatkísérletet a laboratóriumi állatok gondozására és felhasználására vonatkozó útmutatónak (NIH 85–23. Kiadvány, felülvizsgált 1996) összhangban lévő protokollok szerint hajtottak végre, és intézményünk Állatgondozási és Felhasználási Bizottsága jóváhagyta azokat. Bent lakott farokvénás katétert hoztak létre a Gd-DTPA (Magnevist, 0,1 mM/testtömeg-kg) és a Regadenoson (Lexiscan, Astellas Pharmis, 0,1 μg/g testtömeg) bejuttatására CMR során. A testhőmérsékletet 36 ± 0,5 ° C-on tartottuk, az érzéstelenítést pedig 1,1–1,25% O2-izoflurán alkalmazásával. Az étrend megkezdése előtt és minden képalkotó vizsgálat elején minden állat testtömegét feljegyeztük.
Glükóz tolerancia tesztek
A GTT-k esetében [12] az egereket intraperitoneálisan injektáltuk 1 g/kg glükózzal milli-Q vízben egy éjszakán át tartó, 15-16 órás éhezés után. Farokvénából vett vérmintát vettünk a glükóz beadása előtt az éhomi vércukorszint mérésére, valamint a glükózoldat 10, 30, 60 és 90 perccel történő beadása után. A görbe alatti területet (AUC) kiszámítottuk a glükóz tolerancia értékelésére trapéz alakú szabály alkalmazásával [7].
CMR felvásárlások
Érrendszeri reaktivitás
Diéta után 26 hét után a HFD és a kontroll egerek egy alcsoportját eutanizálták és koszorúereket (n ≥ 4) a bal szívkoszorúér második arborizált ágaitól izoláltuk (a lumen átmérője = 90,9 ± 9,5 μm). Az artériákat megszabadítottuk a környező szívizomsejtektől, és egy arteriográfba helyeztük (Danish MyoTechnology, DMT, Ann Harbor, MI), ahol mindkét végén kanüláltuk őket, és 40 Hgmm nyomás alá helyeztük, ahogy azt korábban leírtuk [16–18]. Az adenozin és az acetilkolin kumulatív dózis-válaszait és a passzív tónus értékeléséhez szükséges lépésenkénti nyomásnövekedést mértük a korábban leírtak szerint [16–18].
Szövettan
Az egereket szövettan céljából eutanizálták (n = 5, mindegyik csoport), a szíveket összegyűjtöttük, és a kamrai középtengely rövid tengelyes szakaszait (3 mm vastagságú) 4% paraformaldehidben rögzítettük 4 órán át, majd paraffinba ágyazottuk. A metszeteket (5 μm vastagsággal) anti-CD31 antitesttel (Santa Cruz Biotechnology) festettük a kapilláris sűrűség számszerűsítésére, a Masson’s Trichromot pedig az intersticiális fibrózis és a perivascularis fibrózis számszerűsítésére. A szisztémás érelmeszesedés értékeléséhez a felemelkedő aortákat kivágták és Szudán IV-vel festették.
A szövettan számára a képelemzést ImageJv1,49 g (NIH) alkalmazásával végeztük. A kapilláris sűrűség számszerűsítését 6 véletlenszerű mezőn végeztük (40x), és a kapillárisokat és a kardiomiocitákat megszámoltuk az ImageJ „részecskék elemzése” funkciójával. Az intersticiális fibrózis számszerűsítését 15 véletlenszerű mezőn (40x) végeztük (az ereket nem számítva), és küszöbérték-meghatározási módszert alkalmaztunk a kollagén által elfoglalt terület százalékos számszerűsítésére [19]. Egérenként 2 artérián (40x) végeztük a perivaszkuláris fibrózis számszerűsítését, és feljegyeztük az ér luminális területére normalizált átlagos perivaszkuláris kollagén területet. Az Imageort használva számszerűsített aorta plakk területét az aorta ér területének százalékában fejeztük ki.
MR képek elemzése
Statisztikai analízis
A statisztikai elemzést a SigmaPlot (Systat Software Inc., Point Richmond, CA) alkalmazásával végeztük. A testtömeg, EDV, ESV, EF, LV tömeg, LV EDWT, LV ESWT, pihenő perfúzió, stressz perfúzió, MPR, globális Ecc, Ecc-subepi, Ecc-subendo és CURE különbségeket kétirányú ismételt mérési elemzéssel elemeztük: variancia (ANOVA). A szövegben, táblázatokban és grafikonokban szereplő összes érték átlag ± szórásként jelenik meg.
Eredmények
Testtömeg és glükóz tolerancia tesztek
A testtömeg szignifikánsan magasabb volt a HFD egereknél a diéta után 6 héttel, és ez idővel fokozatosan növekedett (1a. Ábra), o 1. ábra
Perfúzió
A 2a. Ábra az egér szívéből kapott első lépéses perfúziós képeket mutatja. A két egércsoport között a többi perfúziós mérésben egyik időpontban sem volt különbség (2b. Ábra). A HFD egerek stressz perfúziója azonban csökkent a kontroll egerekhez képest a diéta után 18 és 24 héttel (2c. Ábra), o 2. ábra
LV szerkezete és működése
A 3a. Ábra példákat mutat be a fekete-vér cine képekről, amelyeket kontroll és HFD egérből nyertek ED-nél és ES-nél a diéta után 18 héttel. Az LV tömege szignifikánsan magasabb volt a HFD egerekben a kontroll egerekhez képest a diéta után 18 és 24 héttel (3b. Ábra, o 3. ábra
Vérnyomás és pulzus
A diéta utáni 25. héten a szisztolés vérnyomás 106 ± 7 Hgmm volt a kontrollcsoportban és 110 ± 7 Hgmm a HFD csoportban. A diéta utáni 25. héten a diasztolés vérnyomás 81 ± 8 Hgmm volt a kontrollcsoportban és 80 ± 9 Hgmm a HFD csoportban. Ezek a különbségek statisztikailag nem voltak szignifikánsak. A vizsgálat teljes időtartama alatt nem volt szignifikáns pulzusszámkülönbség a két egércsoport között (1. táblázat).
Érrendszeri reaktivitás
Az adenozinra adott kumulatív dózis-válasz görbék 26 hétig HFD-vel táplált egerekben szignifikánsan csökkentek arteriolák tágulási képességét (4a. Ábra), o 4. ábra
Szövettan
Az 5. ábra CD31-vel festett képeket mutat be egy kontrollból (5a. Ábra) és egy HFD egér szívéből (5b. Ábra). A két egércsoport között nem volt szignifikáns különbség a kardiomiocitánként levő kapillárisok számában (5c. Ábra). Ezenkívül a kontroll vagy a HFD egerekben nem volt aorta érelmeszesedés. Az aorta lepedék 3,7 ± 1,8% volt a kontroll egerekben és 3,2 ± 1,4% a HFD egerekben. Az 5. ábra a kontroll egérből (5d. Ábra) és a HFD egérből (5e. Ábra) kapott szívizom Masson Trichrom-festett metszeteit mutatja. Megnövekedett interstitialis fibrózist találtunk HFD egerekben (5f. Ábra, o 5. ábra
Vita
Vaszkuláris reaktivitási eredményeink összhangban vannak a Yamamoto és mtsai korábbi tanulmányaival. [32] és Calligaris et al. [7], akik a kivágott mellkasi aortákban károsodott endothelium-függő relaxációt mutattak az acetilkolinra adott válaszként HFD egerekben a 17. héten és a diéta utáni 8–16. Hónapban. Ezen túlmenően ezek az eredmények összhangban vannak azokkal a korábbi tanulmányokkal, amelyek elhízott betegeknél beszámoltak a koszorúér endothel funkciójának károsodásáról [3, 33].
Korábbi tanulmányok C57Bl/6 egereket használtak különféle étrend-összetételekkel az elhízás, a cukorbetegség és a metabolikus szindróma szívműködésre gyakorolt hatásainak tanulmányozására [7, 8, 11, 32, 34–37]. Az étrend a zsírból származó kalória százalékos aránya (30–78%), valamint a szénhidrát, fehérje, zsírsav és cukor mennyisége szerint változik [38]. Az étrend speciális összetétele megváltoztathatja a súlygyarapodás mértékét és az anyagcsere patofiziológiáját. Részben a különféle étrendek miatt a HFD szívműködésre gyakorolt hatását vizsgáló korábbi tanulmányok ellentmondásos eredményeket hoztak [8, 26, 34].
A jelen vizsgálat során három HFD egér és egy kontroll egér pusztult el. Az egerek a képalkotó ülések között haltak meg, nem CMR vagy glükóz tolerancia teszt során. Az elhullott magas zsírtartalmú diétás egerek egyikénél hasi daganat alakult ki, a másik két magas zsírtartalmú diétás egérnél apró hasi elváltozások voltak. A jelen vizsgálatot, valamint a laboratóriumunkban végzett más vizsgálatokat is beleértve, több mint 60 egerünk volt protokollban, 24 hetes HFD táplálással, és ez a három volt az egyetlen haláleset. Az is nagyon ritka, hogy a kontroll étrendben lévő egerek elpusztulnak. A pusztult egereken kívül a jelen vizsgálat összes többi egere általában egészséges volt, azzal a kivétellel, hogy a HFD egerek elhízottak.
Következtetés
CMR, GTT, vaszkuláris reaktivitás és szövettani vizsgálatok segítségével kimutattuk, hogy a C57Bl/6 egerek 18-24 hétig táplálták a HFD-t reaktivitás normál kapilláris sűrűséggel és aorta plakk nélkül. Ezek a vizsgálatok megállapítják, hogy a HFD-vel táplált egerek mint modellrendszer elhízott és diabéteszes betegek csökkent MPR-jének klinikai forgatókönyvéhez jelentős koszorúér-betegség hiányában. A CMR-t és a HFD-vel táplált génmódosított egereket használó jövőbeni tanulmányok fényt deríthetnek a kulcsfontosságú molekuláris mechanizmusokra, amelyek az elhízás és a cukorbetegséggel összefüggő kardiomiopátia hátterében állnak a miokardiális ischaemia mögött.
- A válás és az akut miokardiális infarktus keringésének kockázata közötti összefüggés kardiovaszkuláris
- A sztatinok keringésének jó kardiovaszkuláris pleiotróp hatásai
- A normál testsúlyú központi elhízás és a szív - és érrendszeri megbetegedések kockázati tényezői közötti összefüggések
- A dohányzás, az alkohol és az elhízás, a szív - és érrendszeri halál és az iszkémiás stroke összefüggése
- A mérsékelt szénhidráttartalmú étrend növényi fehérjével fordítottan összefügg a kardiovaszkuláris kockázattal