A krónikus pangásos szívelégtelenség diuretikus rezisztenciájának perspektívája
Niel Shah
Szent Ferenc Kórház, The Heart Center ®, Advanced Cardiac Therapeutics Center, Roslyn, NY, USA
Raef Madanieh
Szent Ferenc Kórház, The Heart Center ®, Advanced Cardiac Therapeutics Center, Roslyn, NY, USA
Mehmet Alkan
Brown Egyetem, Művészeti és Tudományos Főiskola, Providence, RI, USA
Muhammad U. Dogar
Szent Ferenc Kórház, The Heart Center ®, Advanced Cardiac Therapeutics Center, Roslyn, NY, USA
Constantine E. Kosmas
Icahn Orvostudományi Kar, Sínai-hegyi Kórházközpont, New York, NY, USA
Timothy J. Vittorio
St. Francis Hospital, The Heart Center ®, Advanced Cardiac Therapeutics Center, 100 Port Washington Boulevard, Roslyn, NY 11576-1348, USA
Absztrakt
A krónikus pangásos szívelégtelenség (CHF) egy összetett rendellenesség, amelynek jellemzője, hogy a szív nem képes megfelelni a vele szemben támasztott követelményeknek, majd a progresszív szivattyúhiba és a folyadék felhalmozódása következik. Noha a hurok diuretikumokat széles körben használják szívelégtelenségben szenvedő betegeknél, úgy gondolják, hogy mind a farmakodinamikai, mind a farmakokinetikai változások felelősek a diuretikus rezisztenciáért ezekben a betegeknél. A vizelethajtó rezisztencia leküzdésére irányuló stratégiák között szerepel a nátrium bevitel korlátozása, a diuretikus dózis és az alkalmazás módjának megváltoztatása, valamint a szekvenciális nephron diuretikus terápia. Ebben az áttekintésben megvizsgáljuk a HF betegek diuretikus rezisztenciájának meghatározását, prevalenciáját, fejlesztési mechanizmusát és kezelési stratégiáit.
Bevezetés
A hurok diuretikumokat gyakran használják krónikus pangásos szívelégtelenségben (CHF) szenvedő betegeknél, mivel vitathatatlanul hatékonyak a pangásos tünetek enyhítésében. Egyszerűbben kifejezve, a szívelégtelenségben (HF) szenvedő betegek diuretikus rezisztenciája a diuretikumok sikertelenségének tudható be a só- és vízvisszatartás szabályozásában, még akkor is, ha megfelelő dózisokban alkalmazzák őket. 1 Előfordulhat a vesefunkció csökkenése miatt, amely olyan farmakokinetikai rendellenességekhez vezet, mint például a hurok diuretikumok csúcskoncentrációjának csökkenése vagy késése a vesetubuláris folyadékban. 1 Ugyanakkor előfordulhat ilyen farmakokinetikai rendellenességek hiányában is.
A diuretikus rezisztencia meghatározása és prevalenciája
A „diuretikus rezisztencia” kifejezés növekvő gyakorisága ellenére továbbra sem elégségesen meghatározott. Egyszerűen definiálható vagy a válasz elvesztéseként, vagy a hurok diuretikumokra adott válasz csökkenéseként. 2 Minden három HF-betegből egynél kialakulhat. 3 Általában az extracelluláris folyadék mennyiségének csökkentésének elmulasztása a vizelethajtók megfelelő alkalmazása ellenére „diuretikus rezisztenciának” nevezhető. Pontosabban, a vizelethajtó rezisztencia kifejezhető a nátrium (FENa +) 4 frakcionális kiválasztásaként
Epstein és munkatársai tanulmányt végeztek a metolazon-furoszemid kezelés hatékonyságának meghatározására diuretikus refrakter oedemában szenvedő betegeknél. 5 A kutatók 24 beteget vizsgáltak, akiket 18 hónapos időszak alatt eredetileg refrakternek tekintettek a hagyományos hurok diuretikumok nagy adagjaival szemben. E 24 beteg közül 8-nak feltételezhetően refrakter oedema volt, és így belépett a vizsgálatba. A vizsgálati kritériumok egyikében a vizelethajtó rezisztenciát említették, mivel a nátrium (legalább 90 mmol) nem ürül ki 72 órán belül az orális furoszemid (160 mg) napi kétszeri beadása után. 5 A vizsgálatba bekerült nyolc beteg közül csak három teljesítette a diuretikus refrakter ödéma vizsgálati kritériumait.
Diuretikus rezisztencia ritkábban fordul elő enyhe CHF-ben és konzervált vesefunkcióban szenvedő betegeknél, szemben a közepesen súlyos és súlyos CHF-ben szenvedő betegekkel. 6,7 Eközben egy másik tanulmány arról számolt be, hogy a CHF-ben szenvedő betegek 38% -ának van vesekárosodása, és ezért fokozott a kockázata a diuretikus rezisztencia kialakulásának. 8 Számos vizsgálat kimutatta, hogy a HF-hez általában a becsült glomeruláris filtrációs ráta (eGFR) csökkenése társul, és a közepesen súlyos vagy súlyos vesekárosodás prevalenciája körülbelül 30–60% a HF-ben szenvedő betegeknél. 9–13 Az akut dekompenzált szívelégtelenség nemzeti nyilvántartás (ADHERE) adatbázisa több mint 100 000 kórházi kezelést igénylő, HF-ben szenvedő beteg adatairól számolt be, és ezeknek a betegeknek körülbelül 30% -ánál diagnosztizáltak krónikus vesebetegséget, míg csak 9% -uk normális eGFR volt. 10,11
A diuretikus rezisztencia mechanizmusai szívelégtelenség esetén
Számos elmélet magyarázhatja a diuretikus rezisztencia kialakulásának mechanizmusát. A CHF számos fiziológiai változása megváltoztathatja a gyógyszer farmakokinetikáját, mint például a felszívódás, az eloszlás, az anyagcsere és a hurok diuretikumok eliminációja. A CHF-es betegeknél a diuretikus rezisztencia azonban önmagában nem magyarázható teljes mértékben, mivel ha csak a farmakokinetika változásai voltak felelősek, akkor a diuretikus rezisztenciát le kell győzni az adag növelésével vagy az alkalmazás módjának megváltoztatásával. Ehelyett a diuretikus rezisztencia jobban magyarázható a gyógyszer farmakodinamikájának és farmakokinetikájának párhuzamos változásával, amely befolyásolja a gyógyszer beadásának időbeli lefolyását. 14 Egészséges önkéntesekkel összehasonlítva a CHF-ben szenvedő betegeknél alacsonyabb a gyógyszer felszívódása, ami késlelteti a küszöbérték eléréséhez szükséges időt, és ennek következtében kialakul a diuretikus rezisztencia. 15,16 A diuretikumok biohasznosulása azonban változatlan marad, ezért ezek a változások jobban magyarázhatók az aktív HF-ben szenvedő betegek gyomor-bélrendszeri ödémájának jelenlétével. 17.
Általában a furoszemid a proximális tubulusban található szerves anion transzporterből szekréciójával éri el a tubuláris folyadékot. 18 CHF-ben szenvedő betegeknél a veseelégtelenség diuretikus rezisztenciához vezet a diuretikumok elégtelen intratubuláris koncentrációja miatt, ami a vesék véráramlásának csökkenésével és a proximális tekercselt tubulus (PCT) károsodásával magyarázható. 17,19 A hurok diuretikumok szekréciója csökken az endogén szerves anionok felhalmozódása miatt, amelyek versenyeznek a hurok diuretikumokkal a szerves anion transzporter receptorán való kötődéséért. 20 Ezt a kompetitív gátlást a hurok diuretikumok dózisának emelésével lehet leküzdeni, és ez megmagyarázza a magasabb hurok diuretikus dózisok szükségességét a vizelet terápiás koncentrációjának eléréséhez veseelégtelenségben szenvedő CHF betegeknél.
A diuretikus rezisztencia másik fontos elmélete a gyógyszer-gyógyszer kölcsönhatások, például a nem szteroid gyulladáscsökkentők (NSAID-ok), amelyek a prosztaglandinok gátlásával és ezáltal a vese perfúziójának csökkentésével zavarhatják a diuretikumok hatását. 17,21 –23 Súlyos HF-ben a prosztaglandinok létfontosságúak a vesef perfúzió fenntartásához, valamint a nátrium- és vízkiválasztás elősegítéséhez. Ezért a prosztaglandinok gátlása akár aszpirinnel, akár bármely más NSAID-szal végül csökkentheti a vizelethajtó hatékonyságot azáltal, hogy gátolja a nátrium és a víz kiválasztását. 23 Beszámoltak arról, hogy a terminális, intravénás (IV) katekolamin-függő HF-ben szenvedő betegeknél a 100 mg aszpirin abbahagyása után a hyponatremia jelentős javulása, stabilizálódása és enyhülése következett be, a diuretikus szükséglet lenyűgöző csökkenésével. Állati modellben a prosztaglandin E2 indometacinnal kezelt patkányokban történő beadása kimutatta, hogy helyreállítja a furosemidre adott natriuretikus választ, és így a modell támogatja azt a tényt, hogy az NSAID-ok alkalmazása a látszólagos diuretikus rezisztencia egyik fő oka. 25
Általában a hurokdiuretikumok akut adagolása egészséges betegeknél a renin-angiotenzin-aldoszteron rendszer (RAAS) reflexes aktiválódását okozhatja, ami tovább növeli a nátrium- és vízvisszatartást, és ezáltal korlátozza a diuretikus hatást. 26 Ennek nem szabad hangsúlyosnak lennie súlyos CHF esetén, mivel az ilyen betegeknél már aktivált RAAS van, így a hurok diuretikumok nem tudják tovább aktiválni a RAAS-t, és nem növelhetik a neurohormonok felszabadulását. 3 Ezenkívül a legtöbb CHF-ben szenvedő beteg RAAS-gátlókat kap, így ennek ellensúlyoznia kell a RAAS további aktiválódását a diuretikumok akut beadását követően. 27 Haller és munkatársai beszámoltak egy olyan 29 éves beteg esetéről, amelynek dilatált kardiomiopátia refrakter volt a nagy dózisú furoszemiddel szemben, és arra a következtetésre jutottak, hogy a diuretikus rezisztencia a szívpumpa elégtelenségének, az étrendi indiszkréció és a hiperaldoszteronizmus kombinációjának volt köszönhető. Így tehát nem szokatlan, hogy a CHF-ben szenvedő betegeknél több mechanizmus áll a diuretikus rezisztencia kialakulásának hátterében.
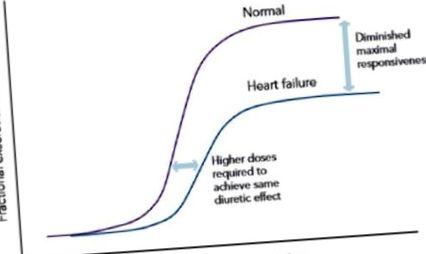
A magas nátrium bevitel elfedheti a vizelethajtó hatásokat, és ezáltal nehézséget okozhat a klinikus számára a vízhajtó rezisztencia meghatározásában. Az étrend nem megfelelősége nem a diuretikus rezisztencia tényleges formája, de diuretikus meghibásodáshoz vezethet. Az étrendi indiszkrécióval nem rendelkező betegeknél a hurok diuretikumok eredetileg kifejezett natriuresishez vezetnek, de ezt posztdiurézis utáni avid nátrium visszaszívódás követheti, ezáltal diuretikus kudarcot okozva. 29 CHF-ben szenvedő beteget általában hosszú távú diuretikus kezelésnek vetnek alá, amely a nephronon belüli farmakológiai változásokkal társulhat, ami súlyosbítja a nátrium-bevitelre adott választ. 3 A magas vérnyomásban szenvedő betegek és kísérleti állatkísérletek adatai azt mutatták, hogy a Henle hurokjában a nátrium újbóli felszívódásának krónikus gátlása a hurok diuretikumok krónikus beadása miatt nagyobb mennyiségben vezetett be nátriumot a korai disztális tekercsbe (DCT), ami sejtes hipertrófia és ezáltal a megnövekedett nátrium-újrafelszívódás, ami végül csökkent natriuresishez vezetett a dózis-válasz görbe lefelé és jobbra tolásával (lásd 1. ábra). Ezt a hurkolt diuretikumok krónikus adagolásának köszönhetően csökkent natriuretikus hatást „fékjelenségnek” nevezik. 18,26,30 –32
Dózis-válasz görbe CHF-ben szenvedő betegeknél krónikus hurok diuretikumokkal.
A vizelethajtó rezisztencia kezelése
Meg nem felelés
Az első lépés, amelyet diuretikus rezisztencia esetén tapasztalunk, az, hogy kizárjuk a gyógyszerbevitel vagy a nátriumkorlátozás be nem tartását (a nátriumbevitelnek 1-nek kell lennie. Amint fentebb említettük, amikor a nátrium-bevitel meghaladja a 100 mmol/nap értéket, a diurézis által elvesztett nátriumot teljes mértékben kompenzálni lehet. posztdiuretikus avid nátrium-visszatartás. 34 A nátrium-bevitelt általában úgy mérjük, hogy mérjük a 24 órás vizelet-nátrium-kiválasztást egyensúlyi állapotban. 1 Diétás hiányosság gyanúja merül fel diuretikum-terápiában részesülő betegeknél, amikor a nátrium-kiválasztás meghaladja a napi> 100 mmol/napot semmilyen kapcsolódó súly nélkül. Eközben a gyógyszeres kezelés (vizelethajtó) megfelelőségét a vizelettel kiválasztott vizelethajtó mennyiségének mérésével lehet értékelni, bár ez az értékelés csak nagyon kevés esetben bizonyul hasznosnak 1.
Az adag beállítása
Amint az 1. ábrán látható, a megfelelő vizelethajtás eléréséhez szükséges vizeletkoncentrációk egészséges egyéneknél nem biztos, hogy képesek elérni a várt diurézist CHF-es betegeknél. Ez azt jelenti, hogy gyakran szükség van a hurok diuretikus adagjának emelésére, még akkor is, ha a gyógyszer farmakokinetikájában nincs rendellenesség. A bumetanid és a torsemid biológiai hasznosíthatósága jobb, mint a furoszemidé, ezért egyes orvosok hatékonyabbnak tartják őket, mint a furoszemid a CHF-ben szenvedő betegeknél. 1 Általában a furoszemid biohasznosulása jelentős intrapatient/interpatient változékonyságot mutat és 10–100% között mozog. 37 Ezzel szemben a bumetanid és a torsemid biohasznosulása 80, illetve 80–100%. 15 Mind a furoszemid, mind a bumetanid azonos hatásfokúnak bizonyult ekvipotens dózisok beadásakor, annak ellenére, hogy a bumetanid 40-szer erősebb, mint a furoszemid súlyára vonatkoztatva. 38,39
IV bolus injekció vagy hurok diuretikum folyamatos infúziója
A hurok diuretikum folyamatos IV infúziója akkor bizonyulhat hatékonynak, ha a diuretikus rezisztencia kezelésére szolgáló egyéb stratégiák kudarcot vallanak. 1 Megállapították, hogy biztonságos és hatékony terápia olyan CHF-betegeknél, akik refrakterek a nagy dózisú orális, valamint az IV-es diuretikus terápiára, és teljesen megakadályozza a posztdiuretikus só-visszatartást is. 1 Számos tanulmány összehasonlította a folyamatos infúzió hatékonyságát a hurok diuretikum szakaszos IV bolus adagolásával előrehaladott HF-ben szenvedő betegeknél. 45–47 A furoszemid adagja folyamatos infúziók esetén 3–200 mg/h volt, a betegek többsége 10–20 mg/h-ot kapott, míg a bumetanidot 0,5 mg bolusban adták, majd folyamatos infúziót hajtottak végre 0,5 mg/h-val. Beszámoltak arról, hogy a hurok diuretikumok hasonló napi dózisa folyamatos infúzióként adva nagyobb mennyiségű vizelet és elektrolit kiválasztódását okozta. Ezenkívül az ototoxicitás kockázata alacsony volt, mivel a furoszemid maximális plazmakoncentrációja szignifikánsan alacsonyabb volt. 45 –48
Kombinált diuretikus terápia (szekvenciális nephron blokád)
Számos tiazidszerű diuretikumot értékeltek hurok diuretikumokkal kombinált terápiában. Valamennyi kombináció összességében hasonló eredményeket mutatott, és így azt mondhatjuk, hogy egyetlen tiazidszerű diuretikum sem jobb a másiknál. Előrehaladott veseelégtelenségben szenvedő betegeknél a metolazont más tiazid-szerű diuretikumoknál jobbnak ítélték meg, de más tiazid-szerű diuretikumok szintén javították a hurok diuretikumok reakcióját hasonló típusú betegeknél. Egy nemrégiben készült, kisméretű, retrospektív egyközpontú kohorszvizsgálat, amely összehasonlította a két leggyakrabban alkalmazott tiazidszerű diuretikumot, nevezetesen az orális metolazont és az intravénás klórtiazidot a hurok diuretikumok kiegészítéseként, nem talált statisztikailag szignifikáns különbséget a biztonságosságban vagy a hatásosságban. 55
A spironolakton mineralokortikoid antagonista és kálium-megtakarító vizelethajtó. Elsősorban a DCT-ben található aldoszteron-függő nátrium-káliumcserélőhelyekhez és a gyűjtőcsatornához való kompetitív kötődéssel hat. Egy kisméretű tanulmány arról számolt be, hogy a nagy dózisú hurok diuretikummal szemben rezisztens 16 HF-ben szenvedő beteg közül 13-ban sikeres volt a spironolakton bevezetése. 56 Azonban egy betegnél dehidráció miatt reverzibilis hyperkalaemia és azotemia alakult ki, de érdemes megemlíteni, hogy a vizsgálatban alkalmazott spironolakton dózisa (100 mg/nap) jóval magasabb volt, mint az átlagos dózis (25 mg/nap), amely túlélést eredményezett. előny a RALES tanulmányban. Ennek a nagy dózisnak az alkalmazásakor tanácsos figyelemmel kísérni a hidratációs állapotot és a szérum káliumszintet. Ezt a nagy dózist 25 mg fenntartó adag követi, amint az összes felesleges folyadék eltávolodik. 1 A spironolakton alkalmazása vizelethajtó rezisztencia kezelésére CHF-ben szenvedő betegeknél általában nem ajánlott, mivel a spironolakton mellett szóló bizonyítékok korlátozottak. 1
Következtetés
A hagyományos dózisú diuretikus terápiával szemben ellenálló folyadék túlterhelés gyakori probléma a CHF-ben szenvedő betegeknél. A fenti megbeszélésből arra a következtetésre jutunk, hogy a CHF betegeknél a vesekárosodás magas prevalenciája a diuretikus rezisztencia magasabb kockázatával jár. A vesekárosodás mellett a gyenge vizelethajtó felszívódás, a gyógyszer-gyógyszer kölcsönhatások, a krónikus diuretikumok adagolása és a magas nátrium-bevitel további potenciális tényezők a HF diuretikus rezisztenciájának kialakulásában. A diuretikus rezisztencia leküzdhető a kezelésével lépésről lépésre, például kizárva a gyógyszer nem megfelelőségét, növelve a diuretikum dózisát, megváltoztatva az adagolás módját orálisról IV-re, és végül kombinált diuretikus terápia alkalmazásával. Ez a lépésenkénti megközelítés a vizelethajtó rezisztencia kezelésében a tünetek gyorsabb enyhüléséhez és potenciálisan a tartózkodási idő csökkenéséhez vezethet dekompenzált HF miatt kórházba került betegeknél. Miután a diuretikus rezisztenciát sikeresen kezelték, a CHF kezelését optimalizálni kell a további morbiditás és mortalitás csökkentése érdekében.
Köszönetnyilvánítás
Timothy J Vittorio ötlettel állt elő e munkáról, és jóváhagyta a végleges kéziratot; Niel Shah feladata volt az irodalmak és tanulmányok áttekintése, a vázlat és a fő kézirat elkészítése, valamint a fő kézirat szerkesztése; Raef Madanieh, Mehmet Alkan, Muhammad U. Dogar és Constantine E. Kosmas voltak felelősek a kézirat kritikai felülvizsgálatáért a szellemi tartalomért, az irodalmak áttekintéséért és a fő kézirat szerkesztéséért.
Lábjegyzetek
Finanszírozás: Ez a kutatás nem kapott külön támogatást egyetlen finanszírozó ügynökségtől sem az állami, sem a kereskedelmi, sem a nonprofit szektorban.
Összeférhetetlenségi nyilatkozat: A szerzők kijelentik, hogy nincs összeférhetetlenség.
Közreműködői információk
Niel Shah, Szent Ferenc Kórház, The Heart Center ®, Fejlett Kardioterápiás Központ, Roslyn, NY, USA.
Raef Madanieh, Szent Ferenc Kórház, The Heart Center ®, Fejlett Kardioterápiás Központ, Roslyn, NY, USA.
Mehmet Alkan, Brown Egyetem, Művészeti és Tudományos Főiskola, Providence, RI, USA.
Muhammad U. Dogar, Szent Ferenc Kórház, The Heart Center ®, Fejlett Kardioterápiás Központ, Roslyn, NY, USA.
Constantine E. Kosmas, Icahn Orvostudományi Kar, Sínai-hegyi Kórház Központ, New York, NY, USA.
Timothy J. Vittorio, Szent Ferenc Kórház, The Heart Center ®, Advanced Cardiac Therapeutics Center, 100 Port Washington Boulevard, Roslyn, NY 11576-1348, USA.
- A testmozgás 7 szívelőnye Johns Hopkins Medicine
- 10 legjobb ellenálló zenekari gyakorlat erős, tónusú lábak számára 2020-ban
- A koriandermag 7 lenyűgöző előnye fokozza a szív egészségét, kezeli a cukorbetegséget és még sok más
- 7 ellenállási sávgyakorlat zsírégetésre és izomépítésre
- 7 tea, amely segíthet vagy károsíthatja a szívét a mindennapi egészségben