A magnéziumpótlás és a fogyás hatása a májenzimekre alkoholmentes zsírmájbetegségben szenvedő betegeknél
Majid Karandish
Táplálkozási és anyagcsere-betegségek kutatóközpontja, Ahvaz Jundishapur Orvostudományi Egyetem, Ahvaz, Irán
Mahtab Tamimi
1 Táplálkozástudományi tanszék, Arvand Nemzetközi Osztály, Ahvaz Jundishapur Orvostudományi Egyetem, Ahvaz, Irán
Ali Akbar Shayesteh
2 Gasztroenterológiai Tanszék, Orvostudományi Kar, Ahvaz Jundishapur Orvostudományi Egyetem, Ahvaz, Irán
Mohammad Hosein Haghighizadeh
3 Biostatikai és epidemiológiai tanszék, Népegészségügyi Kar, Ahvaz Jundishapur Orvostudományi Egyetem, Ahvaz, Irán
Mohammad Taha Jalali
4 Hyperlipidemia Kutatóközpont, Ahvaz Jundishapur Orvostudományi Egyetem, Ahvaz, Irán
Absztrakt
Háttér:
Kevés tanulmány készült a magnézium (Mg) kiegészítés májenzimekre gyakorolt hatásának vizsgálatára. Ennek a vizsgálatnak az volt a célja, hogy értékelje az Mg-kiegészítés és a fogyás májenzimekre, lipidprofilra és éhomi vércukorszintre gyakorolt hatását alkoholmentes zsírmájbetegségben (NAFLD) szenvedő betegeknél.
Anyagok és metódusok:
Ez a vizsgálat kettős-vak, placebo-kontrollos, randomizált klinikai vizsgálat volt. Ultrahangvizsgálatot alkalmaztak zsírmáj diagnosztizálására olyan betegeknél, akik alanin-aminotranszferáz (ALT) értéke ≥ 40 U/L, és egyéb májbetegség nélkül. Összesen 68 (18-59 éves) NAFLD-vel rendelkező résztvevőt véletlenszerűen két csoportra osztottak, hogy vagy Mg-kiegészítést (350 mg elemi Mg naponta), vagy placebót kapjanak 90 napig. A kiinduláskor és a beavatkozás végén az ALT, az aszpartát-aminotranszferáz (AST), az alkalikus foszfatáz (ALP), az összes koleszterin (TCHO), a nagy sűrűségű lipoprotein-koleszterin (HDL-C), a triglicerid (TG), a vércukor és a szérum inzulint és az Mg szintet éhgyomorra mértük. Az alacsony sűrűségű lipoprotein-koleszterint (LDL-C) és az inzulinrezisztenciát (IR) Friedewald-képlet és az inzulinrezisztencia homeosztázis-modelljének (HOMA-IR) alkalmazásával számítottuk ki. Minden résztvevő életmódra vonatkozó javaslatokat kapott, beleértve az alacsony kalóriatartalmú étrendet és a fizikai aktivitást.
Eredmények:
Jelentős csökkenést figyeltek meg az intervenciós és a placebo csoportban az ALT-ben (57,00 (25) - 41,82 ± 19,40 U/L, P = 0,000; 68,50 ± 26,96 - 40,17 ± 19,40 U/L, P = 0,000 Mg és placebo csoportokban ). Hasonló szignifikáns csökkenést figyeltek meg az AST-ben és az éhomi szérum inzulinban a vizsgálati csoportokban. A súlycsökkenés mindkét csoportban szintén szignifikáns volt (91,05 ± 13,77 - 87,60 ± 14,37 kg, illetve 94,59 ± 16,85 - 91,45 ± 16,39 kg Mg, illetve placebo csoportban). Az LDL-C és a TCHO szignifikánsan csökkent a placebo csoportban, de az intervenciós csoportban nem. A szérum Mg jelentősen megnőtt az intervenciós csoportban. Statisztikai szempontból szignifikáns különbséget nem figyeltünk meg a két vizsgálati csoport között a kiinduláskor és a beavatkozást követően.
Következtetés:
A tanulmány megállapításai szerint az Mg-kiegészítés nem befolyásolja a májenzimeket, de a súlyvesztés fontos szerepet játszhat a zsírmáj betegség javításában.
BEVEZETÉS
A nem alkoholos zsírmájbetegséget (NAFLD) a rendellenességek spektrumaként határozzák meg, amelyeket főleg makrovesikuláris máj steatosis jellemez. A NAFLD klinikai jelentősége abból adódik, hogy e betegek jelentős részénél (20-30%) alkoholmentes steatohepatitis (NASH) alakul ki, és ez az állapot az egyszerű zsírmájjal szemben potenciálisan progresszív májbetegség, amely végstádiumú májbetegség és hepatocelluláris carcinoma. [1] Noha a NASH kialakulásának pontos mechanizmusa nem ismert, a legújabb vizsgálatok kimutatták, hogy a NASH-ban szenvedő betegeknél nagyobb az inzulinrezisztencia prevalenciája. [2,3] Az elhízás szintén szorosan összefügg a máj steatosisával. [3] Ezenkívül néhány tanulmány összefüggést jelentett a csökkent szérum-magnézium (Mg) szint és a NASH között. [4]
Az Mg a test több mint 300 metabolikus reakciójának kofaktora. [5] A magnéziumnak fő szerepe van a sejtek általános funkcióiban, ideértve a DNS- és fehérjeszintézist, a glükóz- és zsíranyagcserét, valamint az oxidatív foszforilezést. [6] A Mg-hiány a gyulladásos válasz kiváltásával, a mitokondriális diszfunkcióval, a profibrogén reakcióval és az antioxidáns rendszer aktivitásának csökkenésével függ össze; amely stimulálja a lipidperoxidációt és a citokinindukciót, valamint a steatohepatitis és a májfibrózis kialakulásának jól ismert útjait. [7]
Néhány tanulmányban beszámoltak arról, hogy a Mg-kiegészítés javuló gyulladásos faktorokkal, [7] glükóz-anyagcserével és inzulinrezisztenciával jár. Ilyen összefüggést más vizsgálatok nem mutattak ki. [8,9,10,11] Az Mg-kiegészítés előnyeit a NAFLD-ben szenvedő betegeknél nem állapították meg. Ezért ebben a kettős-vak, placebo-kontrollos, randomizált vizsgálatban megvizsgálták az Mg-pótlás és a fogyás szérum májenzimekre, lipidprofilra és inzulinrezisztenciára gyakorolt hatását.
ANYAGOK ÉS METÓDUSOK
Résztvevők
Ez a vizsgálat kettős-vak, placebo-kontrollos, randomizált klinikai vizsgálat volt. A résztvevőket az Irán délnyugati részén található Ahvazból toborozták. Minden betegnél írásos tájékoztatáson alapuló beleegyezést kaptak. A felvételi kritériumok a következők voltak: 18-59 év közötti életkor, rendellenes májfunkció alanin-aminotranszferáz (ALT) ≥40 U/L mellett és zsírmáj ultrahangvizsgálattal. A kizárási kritériumok a következők voltak: Krónikus hasmenés, alkoholfogyasztás (legalább 30 g/nap), diuretikumok vagy korábbi orális Mg-kiegészítők fogyasztása, májbetegség, hemochromatosis, Wilson-kór, cirrhosis, bármely más máj-, vese- vagy egyéb kórtörténet. tüdő rendellenességek.
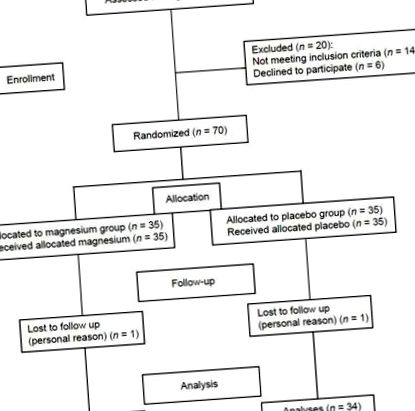
Felvételi folyamatábra a kettős-vak, placebo-kontrollos, randomizált, kontrollált Mg-kiegészítéses vizsgálathoz a NAFLD-ben
Hetven NAFLD-s beteget véletlenszerűen két csoportra osztottak: Az intervenciós csoport (n = 35) napi 350 mg elemi Mg-t kapott magnézium-oxid formájában 90 napig, a kontroll csoport (n = 35) placebót (laktóz) kapott ). A kiegészítő és a placebo kapszulák azonosak voltak, és a Darou-Pakhsh Company (Teherán, Irán) kifejezetten erre a vizsgálatra készítették el, és 20-25 ° C-on tárolták. Ezt az Mg-dózist az Mg tolerálható felső beviteli szintje (UL) és Heriberto Rodriguez-Hernandez beszámolója szerint választották meg az Mg-kiegészítés ALT-re gyakorolt hatásáról. [7]
A táplálkozási szokásokat, a demográfiai és antropometriai adatokat személyes interjúval vagy méréssel nyertük.
A napi tápanyag-bevitelt, beleértve az energiát és a magnézium-tartalmat, három 24 órás étrendi visszahívás alapján becsülték meg a vizsgálat első hónapjában egy képzett dietetikus. Az étrendi adatokat a Nutritionist IV szoftver elemezte. A fizikai aktivitást az általános gyakorlatban végzett fizikai aktivitás kérdőív (GPPAQ) segítségével értékelték ki az alapon. [12]
Kiszámolták az alacsony kalóriatartalmú étrendet, és a résztvevőket felkérték, hogy folytassák ezt a diétát. Az energiaigényt az Egészségügyi Világszervezet (WHO) képletével számolták ki, majd 500 kcal/napra csökkentették (≥ 55% szénhidrát, 15-20% fehérje és ≤30% zsír). Minden résztvevőnek azt tanácsolta, hogy legalább 30 perc fizikai aktivitást végezzen naponta. A megfelelést és az életmódbeli beavatkozást kéthetente értékelték telefonon. A vizsgálat végén megmaradt kapszulákat kaptak a megfelelési arány kiszámításához.
Mérések
A biokémiai változásokat a kiinduláskor és a vizsgálat végén mértük.
A magasságot és a súlyt standard protokollok alkalmazásával mértük, könnyű résztvevőkkel és cipők nélkül. A testtömeg-indexet (BMI) a tömeg (kg) és a négyzetmagasság (m 2) hányadosaként számítottuk ki, és a testzsír százalékát az Omron testzsír-monitorral (HBF-306) becsültük meg a kiinduláskor és a vizsgálat végén. A vérmintákat 12-14 órás éjszakai éhezés után vettük a kiindulási értéknél és az intervenciós periódus után. A szérummintákat mikrotubusokba helyeztük, és az elemzésig -70 ° C-on tároltuk. Az ALT-t és az aszpartát-aminotranszferázt (AST) a Nemzetközi Klinikai Kémiai Szövetség (IFCC) által kifejlesztett módszerrel határoztuk meg. (TCHO), nagy sűrűségű lipoprotein koleszterint (HDL-C), trigliceridet (TG) és a szérum Mg-t enzimatikus kolorimetriás módszerrel mértük. Az éhomi vércukrot (FBS) kolorimetriás módszerrel mértük. Az alacsony sűrűségű lipoprotein-koleszterint (LDL-C) a Friedewald-képlettel számítottuk ki. [16] Az inzulinkoncentrációt immunoenzimometriai módszerrel határoztuk meg, az inzulinérzékenységet pedig az inzulinrezisztencia (HOMA-IR) homeosztázis-modelljének értékelésével a következő képlettel becsültem: Éhomi inzulin (μIU/ml) × éhomi glikémia (mg/dl)/405. [17]
Statisztikai analízis
EREDMÉNYEK
Összesen 68 résztvevő fejezte be a próbát. Két résztvevőt veszítettek nyomon (minden csoportból 1 beteg). Személyes okok miatt nem szerették folytatni részvételüket. A vizsgálati csoportokban azonos számú követett nyomon követhetővé tették a csoportokat e változó tekintetében. A résztvevők nem jelentettek káros vagy mellékhatásokat. A megfelelési arány 85,2, illetve 84% volt az Mg-kiegészítésben, illetve a placebo-csoportban. A kiindulási helyzetben nem volt szignifikáns különbség a demográfiai jellemzőkben és a táplálkozási állapotban az intervenciós és a placebo csoport között [1. táblázat]. A résztvevők átlagos életkora 36 ± 7 év volt. A vizsgálat során a résztvevőknek hat, a placebo csoportból pedig két résztvevőnek napi egy metformin tablettát (500 mg) írtak fel. A gyógyszerek bevitelét tekintve azonban nem volt statisztikailag szignifikáns különbség a csoportok között (P = 0,25). A teljes Mg bevitel átlagos ± SD, kiegészítéssel együtt, 553,83 ± 54,38 és 188,25 ± 70,16 volt a kiegészítő és a placebo csoportban.
Asztal 1
68 NAFLD-s beteg demográfiai és táplálkozási adatai
A vizsgálat kezdetén és végén a 68 beteg antropometriai és biokémiai jellemzőit a 2. és 2., illetve a 3., 3. táblázat mutatja. A kiinduláskor nem volt szignifikáns különbség az összes mért változóban a két csoport között. A beavatkozás után a testtömeg és a BMI (P = 0,004 és P = 0,000 Mg és placebo csoportokban), a testzsír százalékos aránya, az inzulin és az inzulinrezisztencia (IR), az ALT (mindkét csoportban P = 0,000) és az AST jelentősen csökkent intervenciós és placebo csoportok. Az intervenciós periódus végén a szérum ALAT szintje 40 U/L alatt volt Mg (n = 19), illetve placebo csoportban (n = 22). Az FBS és a TG mindkét csoportban csökkent, de nem szignifikánsan (P> 0,05). Nem szignifikáns növekedést figyeltünk meg a HDL-C-ben mindkét csoportban. Másrészt a TCHO és az LDL-C szignifikánsan csökkent a placebo csoportban, de nem az intervenciós csoportban. Az ALP csökkent a placebo csoportban és nőtt az intervenciós csoportban, de nem szignifikánsan. A vizsgálat végén nem figyeltek meg statisztikailag szignifikáns különbséget az intervenciós és a placebo csoport között.
2. táblázat
Az antropometriai jellemzők összehasonlítása a kiinduláskor és a beavatkozás után 90 nappal 68 NAFLD-ben szenvedő betegnél (átlag ± SD)
3. táblázat
A kiindulási és a beavatkozást követő 90 nap biokémiai jellemzőinek összehasonlítása 68 NAFLD-ben szenvedő betegnél
VITA
Ez a tanulmány kimutatta, hogy az Mg-kiegészítés nem befolyásolja a májenzimeket a NAFLD-ben. Az Mg-kiegészítés előnyeit a NAFLD-ben szenvedő betegeknél még nem állapították meg.
Tudomásunk szerint mind a mai napig csak egy kontrollvizsgálatot tettek közzé az Mg-kiegészítő ALT-szintre gyakorolt hatásáról. [7] Az Mg-kiegészítő ALT-szintre gyakorolt jelentős hatása ebben a vizsgálatban ellentétes volt tanulmányunk megállapításával. Két vizsgálat között nagy a különbség. A résztvevőket a hypomagnesemia szerint osztályozták, és a tolerálható UL-nél magasabb Mg-dózist (450 mg/nap elemi Mg) használtak. A vizsgálat időtartama 4 hónap volt, ami valamivel hosszabb, mint ez a vizsgálat. Bár a Mg-kiegészítés a Mg-hiányban szenvedő egyének számára lehet a legelőnyösebb, [7,8,9,21], de tanulmányunkban a résztvevők normomagnesemiásak voltak.
Ebben a tanulmányban az ALT, az AST, az inzulin és az IR szignifikáns csökkenését figyelték meg az intervenciós és a placebo csoportban, és feltételezhető, hogy mindkét csoport súlyának és BMI-jének jelentős csökkenése következik be. Az ALT, AST, TCHO és TG szint csökkenése elhízott nőknél, akik 6 hónapig alacsony szénhidráttartalmú étrendet vagy alacsony zsírtartalmú étrendet (LFD) kaptak, Heriberto Rodriguez-Hernandez és mtsai. [23] azt sugallták, hogy függetlenül attól, hogy A táplálkozási szokások szempontjából az anyagcsere-változások a súlycsökkenéstől függenek. Wang és munkatársai [24] kimutatták, hogy az egyszerű életmódbeli beavatkozások, beleértve az étrend megváltoztatását és a fokozott fizikai aktivitást az elhízott NAFLD-s gyermekeknél, jelentősen javíthatják a máj működését és az inzulinrezisztenciát. Wong és munkatársai [25] azt sugallták, hogy a súlycsökkenés a NAFLD progressziójának csökkenésével jár, és ezeknek a betegeknek életmódbeli módosításokat kell végrehajtaniuk.
Vizsgálatunkban az intervenciós betegek és a placebo csoportok a kezdeti testsúly 3,78, illetve 3,31% -át csökkentették. Ezek a csökkentések az életmód megváltoztatásából származnak. A publikált szakirodalom azt mutatja, hogy az 1-10% közötti súlycsökkenés különböző mértéke összefügg az IR és a májenzimek javulásával. [26,27,28,29,30]
Vizsgálatunkban a TCHO és az LDL-C szignifikáns csökkenését figyelték meg a placebo csoportban. Ezek az eredmények váratlanok voltak, és erre nincs egyértelmű magyarázat. Mivel a változások átlaga nem volt nagy, úgy tűnik, hogy statisztikai szignifikancia volt klinikai jelentőség nélkül, az LDL-C és a TCHO szintjeinek átlaga mindkét csoportban 130 mg/dl, illetve 200 mg/dl alatt volt,.
Két korábbi vizsgálatban kimutatták az Mg-kiegészítés májenzimekre gyakorolt hatását, de ezeket a vizsgálatokat alkoholista résztvevőkön végezték [31,32], és ez nem hasonlít ehhez a tanulmányhoz, mert ismereteink szerint az alkoholistákban a rendellenes májenzimek patogenezise eltér a NAFLD-től. Ez a tanulmány az első randomizált klinikai vizsgálat, amely az Mg-kiegészítés NAFLD-re gyakorolt hatását vizsgálta.
Néhány korlátozás létezett ebben a vizsgálatban: A zsírmáj meghatározásához ultrahangvizsgálatot alkalmaztunk, de a vizsgálat végén nem ismételtük meg. Azonban a NAFLD fokozatának változásai nem voltak a vizsgálat elsődleges eredményei. A vizsgálat rövid időtartama egy másik korlátozás, ezért nem világos, hogy a testtömeg, a májenzimek és az inzulinszint változása hosszú ideig fennmarad-e. A vizsgálat további korlátai az inzulin homeosztázis, a kálium és a kalcium közvetlen mérésének hiánya. Megállapítást nyert azonban, hogy a HOMA-IR hasznos módszer az inzulinérzékenység meghatározására cukorbeteg és nem cukorbeteg résztvevőknél, és a vizsgálatok során megbízhatóan felhasználható, hogy csak éhomi vérmintákat mérnek a glükózból és az inzulinból. [17,33] Az Mg homeosztázis összefügg a kalcium és a kálium állapotával, és ezt a két ásványi anyaggal együtt kell értékelni. [5]
Fontos szempont, hogy a vizsgálat eredményei a normál szérum Mg-szinttel rendelkező résztvevőkhöz kapcsolódnak, és ezeket a megállapításokat nem lehet extrapolálni hipomagneszémiás betegekre.
Összefoglalva, ennek a randomizált klinikai vizsgálatnak az eredményei azt mutatják, hogy a Mg-kiegészítés nem befolyásolja a szérum májenzimszintjét, a lipidprofilt és a glikémiás kontrollt NAFLD-ben szenvedő normomagnesemiás betegeknél. Az életmód módosítása, különösen a súlycsökkentés, javíthatja a betegség állapotát.
ELISMERÉS
A cikkben felhasznált adatok forrása Mahtab Tamimi, az Ahvaz Jundishapur Orvostudományi Egyetem hallgatójának diplomamunkája; és pénzügyi támogatást az Ahvaz Jundishapur Orvostudományi Egyetem nyújtott.
Lábjegyzetek
A támogatás forrása: Arvand Nemzetközi Osztály, Ahvaz Jundishapur Orvostudományi Egyetem, Abadan, Irán, NRC-9011 sz. szám IRCT201203128753N1)
Összeférhetetlenség: Egyik sem nyilatkozott.
- A fehérje táplálékkiegészítők hatása masszív fogyókúrás betegeknél
- A súlyvesztés mértéke és hatása akut mieloid leukémiában szenvedő betegeknél, akik indukciót és
- Súlycsökkenés és a májfibrózis javulása krónikus hepatitis C-ben szenvedő egyiptomi betegeknél
- Kapcsolja be a Hula Hoop karcsúsító fogyás mozgását, edzés, fogyás hatása, tornaterem PNG és vektor
- A; Stallone-effektus; Sziklás út a fogyáshoz; Joe DeGiorgio