A moxibustion terápiás hatásai egyidejűleg célozva Nrf2 és NF-κB diabéteszes perifériás neuropathiában
Absztrakt
Háttér
A tartós hiperglikémia valószínűleg a neuroinflammáció és a neuropátiás fájdalomhoz vezető idegkárosodás fő oka. Nrf2 egy redox által szabályozott transzkripciós faktor, amely részt vesz az antioxidáns védekező rendszerek modulációjában. Nrf2 serkenti az endogén antioxidáns védekező és méregtelenítő enzimek termelését. NF-κB egy transzkripciós faktor, amely immunológiai funkciója mellett részt vesz a proinflammatorikus citokintermelésben. A rendelet Nrf2 koordinálva van a NF-κB a redox homeosztázis fenntartása az egészséges sejtekben. Ez a szabályozás azonban kóros körülmények között zavart; mint ilyen nyilvánvalóvá válik a terápiás beavatkozás lehetősége. A diabéteszes neuropathia olyan állapot, amelyben megváltozik a Nrf2 és NF-κB számoltak be [22].
Vizsgálatunk során megállapítottuk a DPN patkánymodelljét, és ultrahang alatt megfigyeltük a periodontális szövetek szövettani változásait. Az idegvezetési indikátorokat elektrofiziológiai módszerrel detektáltuk. A. Kifejezési szintjei NF-κB és Nrf2 immunblotton keresztül figyelték meg. Tanulmányunk célja a Nrf2 és NF-κB a diabéteszes neuropathiában és összefoglalni a célzott moxibustion terápiás eredményeit Nrf2-NF-κB diabéteszes neuropathiában.
Anyagok és metódusok
Reagensek és állatok
Állatcsoportok és modell
Ebben a kísérletben 100 patkányt használtunk. Miután a patkányokat egy éjszakán át éheztették, a cukorbetegséget 80 patkányhoz indukálták, 0,1 mg nátrium-citrát-pufferben (pH 4,5) oldott STZ intraperitoneális injekciójával 60 mg/kg dózisban [23]. A cukorbetegség sikeres kiváltását akkor igazolták, amikor az éhomi vércukorszint meghaladta a 16,7 mmol/l-t az STZ beadása után 3 nappal, és az a vizsgálat során> 16,7 mmol/l volt. A normál kontrollcsoportban (N) a fennmaradó 20 patkányt ugyanolyan térfogatú hideg citrátpufferrel kezelték, és nem cukorbeteg patkányoknak tekintették.
Ischaemia-reperfúziót indukáltak a DPN modellcsoport diabéteszes patkányaihoz, a korábban leírtak szerint [24]. Röviden, az STZ-diabéteszes patkányokat 4 hetes indukció után 50 mg/kg oldható pentobarbitál-nátrium [25] intraperitoneális adagolásával altattuk. Az iszkémiát a hasi aorta, a jobb közös iliaca artéria és a femorális artéria elzárásával artériaklipszel okozták, amelyeket 3 óra múlva eltávolítottak. Hatvanhárom patkányt vontak be a 4 hétig tartó utolsó vizsgálatba. Tizenhét patkányt kizártunk a 80 patkányból a fertőzés miatti műtét során bekövetkezett halál miatt (n = 5, a százalék 6,25%), vagy az éhomi vércukorszint elégtelen növekedése miatt (
Eredmények
A moxibustion hatása a patkányok idegvezetési sebességére DPN-vel
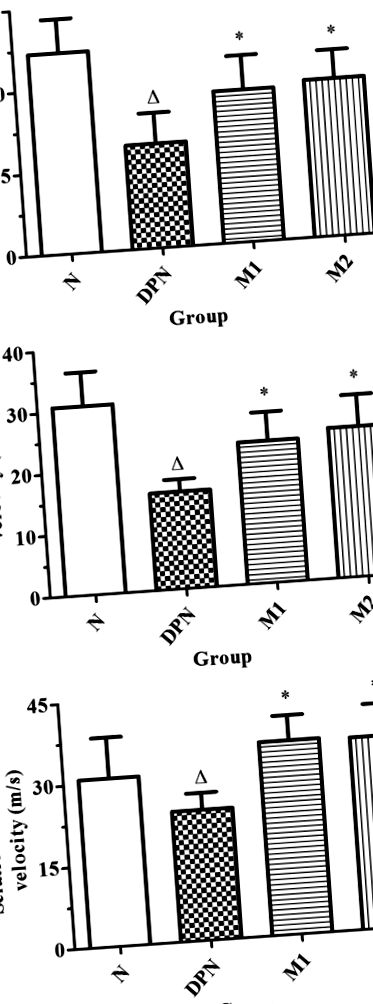
A moxibustion DPN-re gyakorolt potenciális terápiás hatásának meghatározásához kezdetben azonosítottuk a moxibustion hatását a patkányok idegvezetésére a DPN-mel. A normál kontroll (N) csoportéval összehasonlítva az SNCV, NAP amplitúdó és TNCV szignifikánsan csökkent a DPN modell (DPN) csoportban [N versus DPN; SNCV (m/s): 44,23 ± 5,3, szemben 25,18 ± 3,35; NAP amplitúdó (mV): 12,2 ± 2,42, szemben 6,25 ± 1,08; TNCV: 31,46 ± 6,14, szemben 16,27 ± 2,83; n = 20 az N csoportban, míg n = 23 a DPN csoportban, o 1. ábra
Az ülőideg ultraszerkezete
Figyelembe véve, hogy a moxibustion kezelés javítja a DPN-ben szenvedő patkányok NCV-jét, feltételeztük, hogy a moxibustion megvédheti az idegszövet ultrastruktúráját a diabéteszes és ischaemiás sértések ellen. Az ülőidegek ultrastruktúráját transzmissziós elektronmikroszkóp segítségével vizualizáltuk. Az ábrák az N csoport reprezentatív ultrastrukturális jellemzőit mutatják: × 6000, a ábra; a DPN csoport: × 6000, b ábra; az M1 csoport: × 6000, c ábra; és az M2 csoport: × 6000, d ábra. A 2. ábra a tipikus elektronmikroszkópos eredményeket mutatja, amelyek megerősítették az ödémás és ischaemiás ideg myelinjét. A 2. ábra a mielinhüvely duzzadását és megszakadását, axon atrófiáját és a sejt organellájának csökkenését is feltárja a DPN modellcsoportban. Miután a moxibustion-kezelést 15 vagy 30 percig alkalmazták, a kezelt patkányokban a kóros változások csökkentek a normál kontrollcsoportban lévőkhöz képest. A kóros változások közé tartozott az ödéma enyhítése, valamint a mielinhüvely és az axonok sérülése.
Az ülőideg ultrastruktúrája (urán-ólom festés). Normál kontrollcsoport (N) (a): ülőideg ép myelinhüvelyekkel és egészséges axonok szaporodó sejtorganellákkal. Modellcsoport (DPN) (b): az ülőideg súlyos myelinizált axonveszteséggel és megnövekedett endoneuriális kollagénnel, megszakadtak és összegubancolódtak a mielinhüvelyek és csökkentek a sejtorganellumok. M1 (c): moxibustion 15 perc/nap. M2 (d): moxibustion 30 perc/nap
A szérum IL-1β, IL-6 és IL-8 expressziós szintje
Az ELISA elemzés kimutatta, hogy a szérum IL-1β, IL-6 és IL-8 expressziós szintje patkánymodellben szignifikánsan emelkedett a DPN csoport megfelelő értékeihez képest (n = 23, o 3. ábra
Az ülőideg immunblotja
Meghatároztuk a NF-κB és Nrf2 az ülőidegben a korábbi kísérletekből nyert adatok megerősítésére. Az N csoporthoz képest (n = 20.), a kifejezési szint NF-κB a DPN csoport ülőmintáiban szignifikánsan megnőtt, míg a Nrf2 jelentősen csökkent (n = 23, o 4. ábra
Az ülőideg RT-PCR-je
Az immunoblot-kísérlet során kapott megfigyelések megerősítéséhez tovább vizsgáltuk a NF-κB és Nrf2. Összehasonlítva az N csoporttal (n = (20), az mRNS expressziós szintje NF-κB az ülőidegben a DPN csoportban jelentősen megnőtt (n = 23, o 5. ábra
Vita
A DPN okozza a diabetes mellitus leggyakoribb hosszú távú szövődményeit. Mint ilyen, az idegsejtek fontos szerepet játszanak a DPN patogenezisében. Az ideghiány a gliasejtek és az idegsejtek abnormális reakcióival jár együtt a hiperglikémia hatására [27]. A moxibustiont hatékony és biztonságos kezelésként alkalmazzák a DPN számára [28, 29]; a terápiás mechanizmust azonban még nem sikerült teljesen tisztázni. Ebben a vizsgálatban a patkányok ülőidegében bekövetkező idegi ultrastrukturális változásokat és vezetést számszerűsítettük a DPN indukálása után. Hogy ezek a változások társulnak-e NF-κB és Nrf2 a moxibustion kezelés során is vizsgálták.
Az akupunktúra és a moxibustion megelőző kezelése a betegségnek, amely a TCM betegségmegelőzési kezelésének fontos eleme, az ókortól kezdve széles körben elterjedt. Az akupunktúra javíthatja a betegségekkel szembeni ellenállást és visszaállíthatja a test egyensúlyi állapotának fenntartását. Ez egyúttal a kínai orvoslás toborzása is "egészségben maradj, ne légy gonosz". Az ST 36 és a BL 26 pont szoros kapcsolatban áll a veleszületett vese- és a megszerzett lépvel és gyomorral qi, míg az EX-B 3 kiküszöböli az egészségtelen trendeket. A pontkombináció a tünetekkel és a kiváltó okokkal egyaránt foglalkozik azáltal, hogy egyenlő figyelmet fordít a megelőzésre.
A vizsgálat fő erősségeit feltüntették. Tudomásunk szerint ez a tanulmány az első, amely a moxibustion kezelés DPN-re gyakorolt hatásait vizsgálja; így ez a tanulmány előzetes eredményeket szolgáltatott a jövőbeli vizsgálatok alapjaként. Az új kezelési stratégiának fontos szerepe lehet egy kísérleti környezetben, mivel a jelenlegi farmakológiai megközelítések nem elegendők a DPN-hez kapcsolódó ideggyulladáshoz. Megállapítottuk azt is, hogy a 15 perces moxibustion kezelés kellően javíthatja a DPN-t, ami jelentősen hozzájárul a meglévő irodalomhoz.
Vizsgálatunk kimutatta, hogy a moxibustion képes szabályozni és helyreállítani az egyensúlyt az expressziós szintjei között NF-κB és Nrf2 valamint a diabéteszes patkányok parodontális szöveteinek kóros változásai. A moxibustion enyhítette a parodontális szövetek lebomlását és elnyomta az interleukinek, például az IL-1β, az IL-6 és az IL-8 szintézisét és szekrécióját DPN patkányokban. A moxibustion gátolt NF-κB és megmentette a Nrf2 expresszió az ülőidegben. Összefoglalva, a moxibustion olyan terápiás hatásokat válthat ki, amelyek egyszerre célozzák meg a Nrf2 és NF-κB útvonalak a DPN-ben.
A vizsgálat egyik korlátja az, hogy bár a DPN-ben szenvedő patkányokat 4 hétig kezelték idegvezetésük felmérése érdekében, nem végeztek folyamatos mérést a moxibustion hosszú távú hatásának a NF-κB és Nrf2 kifejezések. A jövőbeni vizsgálatoknak ötvözniük kell a kísérleti értékelést az idegvezetés mikroszkópos és molekuláris vizsgálataival, hogy tisztázzák a moxibustion hosszú távú hatékonyságát. A további vizsgálatoknak azt is ki kell deríteniük, hogy a moxibustion gátolja-e vagy szabályozza-e a szervezet metabolikus funkcióját a gyulladásos tényezők kiküszöbölésével és közvetett szabályozásával. NF-κB és Nrf2 útvonal. Ezenkívül az emberen végzett klinikai kutatásra való áttérés további vizsgálatokat igényel.
Következtetések
Eredményeink azt mutatják, hogy a moxibustion gátolta a fehérje és az mRNS expresszióját NF-κB hanem a fehérje és mRNS expresszióját indukálta Nrf2 az ülőidegben. A Moxibustion helyreállította az egyensúlyt NF-κB és Nrf2 patkányokban DPN-vel. Így az idegi gyulladást az interleukin gyulladásos tényezők szabályozásával enyhítették [ábra. 6].
- A kurkumin terápiás hatása a máj ultrahangos morfológiai jellemzőire a betegeknél
- A hidrogén-peroxid metabolizmusának terápiás lehetőségei az agyi ischaemia kezelésében
- A Fucoidan terápiás hatásainak áttekintése a legújabb tanulmányokról
- A legjobb kenyér választás cukorbetegek számára!
- A nyers kannabisz fogyasztásának terápiás és étrendi előnyei - RQS Blog