Alkoholmentes zsírmájbetegség: Klinikai megközelítés és áttekintés
Absztrakt
A nem alkoholos zsírmájbetegség (NAFLD) a májenzimek véletlen emelkedésének leggyakoribb oka Észak-Amerikában és Európában. A NAFLD kockázati tényezői közé tartozik a 25 kg/m 2 vagy annál nagyobb testtömeg-index, a központi elhízás és a diabetes mellitus. A betegség spektruma változó, a jóindulatú prognózissal rendelkező egyszerű szteatózistól az alkoholmentes steatohepatitisig és cirrhózistól kezdve, növelve a morbiditást és a mortalitást. A NAFLD-ben szenvedő betegeknél az elsődleges rendellenesség vagy „első találat” a máj steatosishoz vezető inzulinrezisztencia. A második találat több proinflammatorikus citokint tartalmaz, amelyek alkoholmentes steatohepatitist eredményeznek. A kezelés célja az agresszív kockázati tényezők ellenőrzése és a fogyás. Jelenleg nincsenek a NAFLD kezelésében ajánlott farmakológiai szerek, bár az előzetes tanulmányok ígéretes szereket javasolnak a jövőben.
Önéletrajz
La stéatose hépatique non alcoolique (SHNA) est la principale cause d’élévation auxiliaire des enzymes hépatiques en Amérique du Nord et en Europe. Az SHNA arcképe a 25 kg/m 2 testtömegű testtömegből és a tronculaire encore plusz fontos cukorbetegségből áll. Le specter de la maladie est változó, d’une stéatose simple au pronostic bénin à une stéatohépatite non alcoolique associée à une cirrhose qui augmente la morbidité et la mortalité. L’anomalie primaire, ou première előfordulás, chez les betegek atteints d’une SHNA un une inzulin- vagy rezisztencia-provokáló une stéatohépatite. La deuxième előfordulás touche des cytokines pro-inflammatoires multiples entraînant une stéatohépatite non alcoolique. Le traitement vise le contrôle agressif des facteurs de risque et la perte de poids. Pour l’instant, az aucun ágens farmakológiai javaslata, amely az SHNA traiter-t ajánlja, az előbbi előzetes promóciókat à cet égard.
Ludwig és munkatársai (1) 1980-ban leírták az alkoholmentes steatohepatitis (NASH) kifejezést, hogy leírják a biopsziás eredményeket steatohepatitisben szenvedő betegeknél, jelentős alkoholfogyasztás hiányában. Elég nehéz meghatározni, hogy a steatohepatitis milyen küszöbértéknél válik alkoholfüggővé. Hagyományosan a férfiaknál legfeljebb 20 g/nap és 40 g/nap, a nőknél 20 g/nap alkohol jelenti az alkoholfogyasztás felső határát az alkoholmentes zsírmájbetegség (NAFLD) diagnózisának fenntartása érdekében. A NAFLD spektruma széles, az egyszerű steatosistól a NASH-ig terjed. A NAFLD továbbra is olyan kóros diagnózis, amely a máj biopsziájának minimum 5% -os steatosisát igényli a diagnózis felállításához.
EPIDEMIOLÓGIA ÉS KOCKÁZATTÉNYEZŐK
ASZTAL 1
A steatosis és az alkoholmentes steatohepatitis társuló rendellenességek
| Diabetes mellitus | Gyulladásos bélbetegség |
| Extrém alultápláltság | Elhízottság |
| Hyperlipidemia | Teljes parenterális táplálás |
| Jejunoilealis bypass | Biliopancreaticus elterelés |
| Kiterjedt vékonybél reszekció | Gasztroplasztika kóros elhízás esetén |
| Részleges lipodisztrófia | Jejunal diverticulosis baktériumok elszaporodásával |
| Az anyagcsere veleszületett hibái | |
| Abetalipoproteinemia | Családi hepatosteatosis |
| Galactosemia | Glikogén tárolási betegség |
| Örökletes fruktóz-intolerancia | Homocystinuria |
| Szisztémás karnitinhiány | Tirozinémia |
| Weber-Christian szindróma | Wilson-kór |
2. TÁBLÁZAT
Nem alkoholos zsírmájbetegséghez kapcsolódó gyógyszerek
| L-aszparagináz | Azaserine | Amiodaron | Didanozin |
| Azauridine | Puromicin | Diklór-etilén | Sztavudin |
| Metotrexát | Bleomicin | Etil-bromid | Fialuridine |
| Tetraciklin | Hidrazin | ||
| Izoniazid | Zidovudin | ||
| Diltiazem | |||
| Coumadin | |||
| Ösztrogének | |||
| Glükokortikoidok | |||
| Tamoxifen | |||
| Nifedipin | |||
| Klorokin |
DIAGNÓZIS
PATOGENEZIS
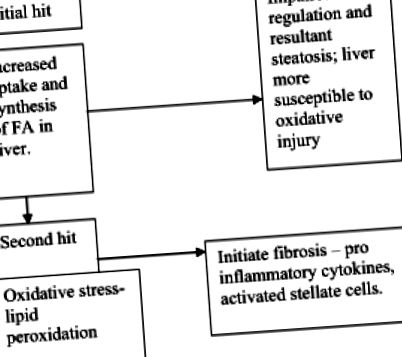
Az egyszerű steatosisról a steatohepatitisre, a fibrózisra és a cirrhosisra való előrehaladást két találatú hipotézisnek tartják (1. ábra).
Két találatú hipotézis. FA Zsírsavak
Első találat
Második találat
A második találat hepatocelluláris károsodás, amely az oxidatív stressz, a lipidperoxidáció és az FFA-k által okozott közvetlen sejttoxicitás következménye (18). Többféle mechanizmust javasoltak a májsejtek sérülésével kapcsolatban:
Kimutatták, hogy a citokróm P450 izoform CYP2E1 fokozott expressziója fordul elő NASH-ban szenvedő betegeknél. A CYP2E1 prooxidáns, amely megnöveli a sejtmembránok peroxidálására képes reaktív oxigénfajok termelését.
A megnövekedett inzulin perifériás lipolízishez vezet, amely felesleges zsírsavakat eredményez, amely katalizálja a lipid peroxiszómákat. A peroxiszómák részt vesznek a zsírsavak oxidációs folyamatában. Az oxidáció, valamint a zsírsavak megkötése és exportja az elsődleges módszer a máj védelmére a későbbi károsodásoktól.
A peroxiszóma proliferátorok által aktivált alfa-receptor (PPAR-α) felelős a nagyon alacsony sűrűségű lipoproteinben lévő zsírsavak észterezésének és exportjának szabályozásáért, a zsírsavak kötődéséért, valamint a mitokondriális és peroxiszomális oxidációban. A PPAR-α csökkent expressziójának fontos szerepe lehet a NASH patogenezisében (19).
Mitochondriális rendellenességeket írtak le NASH-ban szenvedő betegeknél, de egyszerű steatosisban szenvedőknél nem. Ezek a mitokondriális rendellenességek megnövekedett mitokondriális zsírsavak béta-oxidációjához vezetnek, ami végül szabad gyökök képződését eredményezi hepatocita sérülés és steatohepatitis. Azoknál a betegeknél, akik inzulinrezisztensek, de nincsenek mitokondriális rendellenességeik, zsírmáj alakulhat ki; azonban általában nem fejlődnek steatohepatitiszé (20).
VEZETÉS
Konzervatív vezetés
Jelenleg a menedzsment az életmód módosítására irányul, elsősorban az étrend módosításával és a testmozgással elért súlycsökkenést célozza meg. Ezenkívül meg kell kezdeni a metabolikus szindróma minden más aspektusának kezelését. A fogyás és a testmozgás egyaránt javítja az inzulinrezisztenciát (21), amelynek elméletileg javítania kell a steatosisban. Nem végeztek randomizált, kontrollált tanulmányt annak értékelésére, hogy a súlyvesztés után szövettani regresszió lép-e fel steatohepatitisben vagy fibrózisban szenvedő betegeknél, bár az esettanulmányok és a nyílt tanulmányok javulásra utalnak. A súlycsökkenés nem haladhatja meg a heti 1 kg-ot, mert a gyors fogyás súlyosbíthatja a steatózist. Hasonlóképpen a nagyon alacsony kalóriatartalmú étrendet, amely kevesebb, mint 500 kcal/nap, és a jejunoileális bypass műtétet el kell kerülni a fogyás módszereként, a fibrózis súlyosbodásának kockázata miatt. A fogyás ajánlott célja az ember testtömegének 10% -a hat hónap alatt (22).
Számos népszerű diéta létezik a fogyás módszereként. Egyes étrendek több éves orvosi tapasztalaton alapulnak, míg mások jelentősen eltértek az általános orvosi tanácsoktól. A Weight Watchers program a hagyományos modellek egyike, korlátozza az adagok méretét és az összes elfogyasztott kalóriát. Egyéb népszerű étrendek közé tartozik a zsír korlátozás nélküli szénhidrát-korlátozás (Atkins-diéta), a makrotápanyagok és a glikémiás terhelés módosítása (zóna-diéta) és a zsír-korlátozás (Ornish-diéta). Elhízott betegeknél, akiknek a BMI-értéke meghaladja a 35 kg/m 2 -et, nem találtak szignifikáns különbséget az egy év végén leadott súly mennyisége tekintetében (23). A kardiovaszkuláris kockázati tényezők csökkenése korrelált a súlycsökkenés mértékével. Egy év alatt 3–6 kg súlycsökkenést sikerült elérni az alkalmazott étrend típusától függetlenül. Jelenleg nem állnak rendelkezésre adatok a NASH-ban szenvedő betegek különféle étrendjeiről.
Súlycsökkentő gyógyszerek
A testsúlycsökkenést kiváltó gyógyszereket nem szokásosan alkalmazzák a NAFLD kezelésében, és randomizált klinikai vizsgálatokban sem vizsgálták őket. Az egyik esetsor azt sugallta, hogy az NASH-ban szenvedő betegek orlisztátja biztonságos, és hat-12 hónapos kezelés után szignifikáns szövettani javulást mutatott mind a steatohepatitis, mind a fibrózis mértékében (24). Az orlisztát a gyomor- és hasnyálmirigy-lipáz reverzibilis inhibitora, és az elhízás kezelésére jóváhagyott két szer egyike. Ez a gyógyszer kovalens kötést képez a gyomor és a hasnyálmirigy lipázának aktív szerinmaradékával a gyomorban és a vékonybélben, blokkolva az étrendi trigliceridek emésztését és felszívódását. Az orlisztát kontrollált energiatartalmú étrenddel kombinálva, nem csupán diétával, jelentősen megnövelte a fogyást elhízott felnőtteknél egyéves terápia után (25).
Természetesen az étrendet a testmozgással kell kombinálni a fogyás elindítása és fenntartása érdekében. A testmozgás fokozza a fogyáshoz szükséges kalóriahiányt. A testmozgásból származó egészségügyi előnyök megszerzéséhez legalább 30 perc közepes, tartós aktivitás szükséges heti öt napon keresztül (28). Minden fitnesz programnak tartalmaznia kell az aerob testmozgás, az erő és a rugalmasság edzésének egyensúlyát.
A NAFLD kezelésében értékelt farmakoterápia
3. TÁBLÁZAT
Randomizált, kontrollált vizsgálatok (RCT), amelyek nem alkoholos steatohepatitisben (NASH) szenvedő betegek farmakológiai terápiáját értékelték, valamint kísérleti tanulmányok a biokémiai és szövettani paraméterek javulását mutatták NASH-ban szenvedő betegeknél
| Metformin | 6. | RCT | - | - | - | Uygun és mtsai (35) |
| Ursodeoxycholic sav | 24. | RCT | - | - | - | Lindor és mtsai (36) |
| E- és C-vitamin | 6. | RCT | - | - | ↑ | Harrison és mtsai (37) |
| Roziglitazon | 12. | Nyitott címke | ↑ | ↑ | ↑ | Neuschwander-Tetri és mtsai (30) |
| Pioglitazon | 12. | Nyitott címke | ↑ | ↑ | ↑ | Promrat és mtsai (31) |
| Betain | 12. | Nyitott címke | ↑ | ↑ | ↑ | Abdelmalek és mtsai (38) |
| Orlisztát | 24. | Nyitott címke | ↑ | ↑ | ↑ | Harrison és mtsai (24) |
Bariatrikus műtét
A májbiopszia szerepe
Gyakran a NAFLD a kirekesztés diagnózisa. A betegeknek tanácsot adnak az életmód módosítására vonatkozóan, és néhány hónappal később, a rutinszerű nyomon követés során klinikai és biokémiai szempontból újraértékelik őket. Ez egyelőre ésszerű megközelítés lehet, mert a NAFLD kezelésében nincsenek hatékony gyógyszerek. Mivel azonban a farmakoterápia a jövőben opcióvá válik, szükség lehet ennek a gondolatmenetnek a felülvizsgálatára. A tiszta zsírváltozás és a steatohepatitis között csak szövettanilag lehet különbséget tenni. Ez a megkülönböztetés azért fontos, mert a NAFLD jóindulatú prognózissal rendelkezik, míg a NASH a cirrhosis felé halad. A NASH kockázata miatt azoknál a betegeknél, akiknek gyanúja szerint zsírmájuk van, azt lehetne állítani, hogy minden betegnek fel kell ajánlani a máj biopsziáját a betegség kialakulásához. A logisztika, a költségek és a mellékhatások tekintetében azonban ez nem biztos, hogy lehetséges. Ennélfogva ésszerű olyan betegeket biopsziálni, akiknél előrehaladottabb betegség kockázati tényezői vannak, például az életkor előrehaladása, az elhízás, a magas vérnyomás és a diabetes mellitus. Ezenkívül a májbiopszia alkalmanként feltárhatja a gyanútlan rendellenességeket, ami a zsírmáj alternatív vagy kiegészítő diagnózisát jelzi.
KÖVETKEZTETÉSEK
Mivel az elhízás járványa folyamatosan növekszik, a NAFLD előfordulása és prevalenciája is növekszik. Az elsődleges rendellenesség a belső inzulinrezisztenciának tűnik. A NAFLD természettörténete meglehetősen változó, a jóindulatú betegségtől a dekompenzált betegségig terjed, asciteset, varicealis vérzést, hepatocelluláris carcinomát vagy halált eredményezve. Jelenleg nincs engedélyezve farmakológiai terápia a NASH kezelésére. A kezelés fő támasza továbbra is a fogyókúrás kezelés étrenden és testmozgáson keresztül, valamint az agresszív kockázati tényezők ellenőrzése. Bár egyes gyógyszerek kedvezőnek tűnnek a NASH kezelésében végzett kísérleti vizsgálatok során, további randomizált, kontrollált vizsgálatokra van szükség, mielőtt ezen szerek rutinjavaslataira sor kerülne.
- A nem alkoholos zsírmáj betegség (NAFLD) tünetei, okai; Kezelés
- A nem alkoholos zsírmájbetegség (NAFLD) prevenciós szerepe a mediterrán étrendben és a fizikai aktivitásban
- Alkoholmentes zsírmájbetegség és alacsony szénhidráttartalmú étrend A táplálkozás éves áttekintése
- Alkoholmentes zsírmáj betegség MedlinePlus Medical Encyclopedia
- Az alkoholmentes zsírmáj betegség tünetei, okai, diagnózisa és kezelése