Az angioödéma megértése és kezelése a sürgősségi osztályon
kapcsolódó cikkek
Az akut dekompenzált szívelégtelenség kezelése a sürgősségi osztályon: II
Az asztma frissítése: Az asztma kezelése a Gyermek Sürgősségi Osztályon
Az akut dekompenzált szívelégtelenség kezelése a sürgősségi osztályon: I. rész
Kapcsolódó termékek
Az angioödéma megértése és kezelése a sürgősségi osztályon
Az erőszakos beteg kezelése a sürgősségi osztályon
A tetanusz kockázatának értékelése a Gyermek Sürgősségi Osztályon
Kulcsszavak
légút
angioödéma
csalánkiütés
c1-inh
SZERZŐI
Daniel Fisher, DO, FACEP, klinikai adjunktus, Sürgősségi Orvostudományi Osztály, Dél-Karolinai Orvostudományi Egyetem, Charleston.
Hesham F. Abukhdeir, MD, MPH, Sürgősségi Orvostudományi Osztály, Dél-Karolinai Orvostudományi Egyetem, Charleston.
TÁRSFELÜLVIZSGÁLÓ
Joseph J. Moellman, MD, sürgősségi orvoslás professzor, Cincinnati Egyetem Orvostudományi Főiskola, Orvosi igazgató, Deer Park/Silverton EMS.
A kiadvány esetleges elfogultságának feltárása érdekében és az Akkreditációs Tanács a továbbképző orvosi irányelveknek megfelelően közzétesszük, hogy Dr. Farel (CME kérdésellenőr) a Johnson & Johnson részvényekkel rendelkezik. Dr. Stapczynski (szerkesztő) a Pfizer, Johnson & Johnson, a Walgreens Boots Alliance Inc., a GlaxoSmithKline, a Bristol Myers Squibb és az AxoGen részvényeivel rendelkezik. Dr. Moellman (szakértői szakértő) beszámol arról, hogy kutatási/támogatási támogatást kapott Shire, Janssen, J&J, Medtronic, Gilead és Becton/Dickinson részéről. Dr. Schneider (szerkesztő), Ms. Fessler (nővértervező), Dr. Fisher (szerző), Dr. Abukhdeir (szerző), Ms. Mark (ügyvezető szerkesztő), Ms. Coplin (ügyvezető szerkesztő) és Mr. Landenberger ( szerkesztőségi és továbbképzési igazgató) nem számolt be pénzügyi kapcsolatokról azokkal a vállalatokkal, amelyek az e CME tevékenység által lefedett tanulmányi területhez kapcsolódnak.
VEZETŐI ÖSSZEFOGLALÓ
- Az allergiás angioödémát, különösen ha anafilaxiával vagy légúti kompromisszummal jár, 0,01 mg/kg IM-adrenalinnal kell kezelni (gyermekeknél legfeljebb 0,3 mg, felnőtteknél 0,5 mg). Megjegyzendő, hogy az epinefrin címkézése a közelmúltban megváltozott. A korábban 1: 1000 jelzésű gyógyszert most felcímkézték
1 mg/ml. - Az örökletes angioödémában és súlyos betegségben szenvedő betegeket általában icatibanttal vagy ecallantiddal kezelik.
- Az örökletes angioödémában szenvedő betegek többségének csökkent a C1-INH szintje. C4 és C1-INH szint megrajzolása akut roham során hasznos lehet.
- A hisztamin által közvetített allergiás reakcióktól eltérően az örökletes angioödémát a bradikinin közvetíti. Az epinefrin, a difenhidramin és a kortikoszteroidok nem fordítják meg a betegséget. Ők sem rontanak rajta. Tehát, ha kétség merül fel, a légúti tünetekkel küzdő és előzetes diagnózis nélküli betegek kapják az adrenalint.
Az oktatási tevékenység befejezése után a résztvevőknek képesnek kell lenniük felismerni és bemutatni az angioödéma megértését, megvitatni mind az állapottal kapcsolatos differenciáldiagnosztikát, mind a szövődmények körét, és a korszerű diagnosztikai és terápiás technikákat alkalmazni az értékelésben és a angioödéma kezelése a sürgősségi osztályon (ED).
Bevezetés
Az angioödéma a mély dermális, a szubkután és a nyálkahártya szövetek duzzanata a fokozott érpermeabilitás miatt. Az angioödéma első részletes leírását 1876-ban Dr. John Laws Milton dokumentálta Londonban, aki eredetileg „óriási csalánkiütésnek” nevezte ezt az állapotot. 1882-ben Heinrich Quincke újabb leírást adott az angioödémáról, amely később eredeti nevét a „Quincke-kór” -nak kapta. 1 1888-ban William Osler az örökletes angioödémát (HAE) különálló betegségként azonosította, miután tanulmányozták az öt generációt átfogó angioödéma-rohamokkal járó családot, 1963-ban pedig Donaldson és Evans a HAE okát a C1 észteráz inhibitor (I. típus) csökkent szintjeként jelentették be. ). 1-4. A HAE második formáját normális C1-észteráz inhibitor-szinttel, de rendellenes funkcióval találták, ami azt a felfedezést eredményezte, hogy mindkét forma összefüggésben állt a C1-inhibitor gén (SERPING1) (II. Típusú) mutációjával. A HAE új formáját azonban megtalálták normál SERPING1 esetén. 1
A C1 inhibitor örökletes hiányosságai mellett vannak szerzett típusok is. Úgy gondolják, hogy ezek másodlagosak a létező betegségfolyamatokból eredő autoantitesteknél, a leggyakoribb etiológia a limfoproliferatív rendellenességek. 1 További formák közé tartozik az angiotenzin-konvertáló enzim (ACE) gátló által kiváltott angioödéma és a nem hisztaminerg idiopátiás angioödéma. Ezeknek a változatoknak az egységes témája a bradikinin szabályozása körül forog. Az angioödéma egy másik formája a hisztamin-közvetítésű, amint az akut allergiás reakciókban és anafilaxiában is megfigyelhető.
A peptid bradikinin és amin hisztamin egyaránt erős értágítók, és a felesleges szint érrendszeri permeabilitást okozhat. Ez a vaszkuláris permeabilitás átmeneti duzzanatot eredményezhet a bőr mély dermiszében és a bőr alatti rétegeiben, valamint a légzőszervi és a gyomor-bél traktus submucosalis rétegében. Az angioödéma, más néven angioneurotikus és Quincke ödéma írja le azt a duzzanatot, amely ezekben a szövetrétegekben fordul elő a túlzott hisztamin vagy bradikinin körülményei miatt. 5.
Normális esetben az angioödéma nem szúrós, lehet bőrszín vagy erythemás, és gyakran olyan területeken fordul elő, ahol a bőr laza (azaz arc, nemi szervek). (Lásd az 1. és 2. ábrát.) A duzzanattal együtt hő és fájdalom is jelen lehet, de általában nem viszket. 2 Hasonló típusú reakció látható a csalánkiütésben is; az urticaria azonban az érpermeabilitás miatt duzzad, amely a bőr felszínesebb rétegeiben fordul elő. Jellemzően viszketés. A sürgősségi orvosok számára fontos ismerni az urticaria és az angioödéma közötti hasonlóságokat és különbségeket. (Lásd az 1. táblázatot.)
1. ábra Rendkívüli csalánkiütés
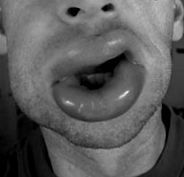
2. ábra: Az ajkak angioödémája
1. táblázat: Angioödéma és csalánkiütés jellemzőinek összehasonlítása 2
Funkció
Urticaria
Angioödéma
Bőr és nyálkahártya, különösen a szemhéjak és az ajkak
A papilláris dermis rétegben főként neutrofilek, eozinofilek, monociták és T-limfociták kiterjedt értágulat, kevés ödéma és ritka perivaszkuláris infiltrátum
Kiterjedt ödéma, kevés vazodilatáció és kevés vagy egyáltalán nincs sejtes infiltrátum, kivéve az allergiás angioödémát, ahol eozinofilek láthatók a retikuláris dermális, szubkután/submucosalis rétegekben
Epidemiológia és kórélettan
Örökletes angioödéma. A C1-INH-hiányos HAE egy autoszomális domináns betegség, szinte teljes behatolással, és nem hajlamos a szexre vagy a fajra. Az I. típus az esetek körülbelül 85% -át teszi ki, a többit a II. A HAE prevalenciája az általános populáció 1: 30 000 és 1: 80 000 között van. 1 Az I. típusú esetek mintegy 20-25% -a spontán mutációnak köszönhető. 5 Ezzel szemben a normál C1-INH-val rendelkező HAE (korábban HAE III típusú) szintén autoszomális domináns, de túlsúlyban van a nőknél. (Lásd a 2. táblázatot.) A népességre vonatkozó adatok egyelőre nem állnak rendelkezésre, mivel nincsenek világos diagnosztikai kritériumok. Az ebben a betegségben szenvedő férfiaknak kevésbé súlyos változata van. 1 A normál C1-INH-val rendelkező HAE oka ismeretlen, de oka lehet a XII faktor génjének téves működése. 5,6
2. táblázat: Angioödéma típusai 1,2
Szindróma
Kórélettan
Érintett betegek
Elterjedtség
C4 szint
C1-INH antigén
C1-INH funkció
C1q szint
A SERPING1 gén mutációja C1 inhibitor hiányt okoz
A SERPING1 gén mutációja funkcionális C1 inhibitor hiányt okoz
HAE normál C1-INH-val (korábban III. Típusú HAE-nek hívták)
Mind, de sokkal több nő
Szerzett C1-INH hiány
A C1-inhibitor túlzott fogyasztása hiányhoz vezet
A bradikinin katabolizmus gátlása
Az összes, de nőtt az afro-amerikaiaknál
A hízósejtek szenzibilizálása IgE-vel
A hízósejtek szenzibilizálása IgG-vel, autoimmun pajzsmirigy betegséggel összefüggésben
Az I. és II. Típusú HAE a C1-INH 1 hiányának tudható be, amelyet a SERPING1 gén mutációi okoznak. A C1-INH sok proteázt szabályoz. Részt vesz a komplement, a kinin, a plazmin és az alvadási rendszerek klasszikus útvonalának gátlásában. 7 C1-INH ezt úgy valósítja meg, hogy a célproteázzal kombinálva összetett proteáz képződik, amely egészében ürül. Az I. és II. Típusú HAE autoszomális domináns betegség, a SERPING1 gén több mint 280 különböző mutációjáról számolnak be jelenleg. A II. Típust szinte kizárólag missense mutációk okozzák, amelyek C1-INH termelődését eredményezik, amely képtelen összetett proteáz képződésére. 1,7
Az I. típus bármilyen típusú mutáció lehet, ami a C1-INH hiányát eredményezi, ami viszont a bradikinin feleslegéhez vezet az ödéma okaként, míg az ödéma másik feltételezett oka a felesleges C2 kinin. 1,7 E két peptid szintje megnő, ha hiányzik a gátlás. Ezek a peptidek a posztkapilláris venulára hatnak, ami az endoteliális sejtek visszahúzódását okozza, és teret képez, amelyen keresztül a plazma szivároghat és végül ödéma formájában felhalmozódhat. 7 Úgy tűnik, hogy az angioödéma mindkét típusa a C1q (a C1 komplex első alkomponense) használata nélkül aktiválja a komplement kaszkádot, amit laboratóriumi vizsgálatok igazolnak, amelyek normális C1q és csökkent C4 szinteket mutatnak be.
A normál C1-INH (korábban HAE III. Típusú) HAE kórélettana nem jól ismert. Ezen betegek hozzávetőleg 25% -ánál találtak mutációkat a XII faktorban. A bradikinin növekedése nem bizonyított, de esettanulmányok kimutatták, hogy a bradikinin termelésének gátlására irányuló kezelések voltak a legsikeresebbek a duzzanat csökkentésében. 1
Szerzett angioödéma. A megszerzett angioödéma (AA) a C1-INH hiányával is jár; ez a hiány azonban nem genetikai mutációnak köszönhető. Az AA középkorú és idősebb betegeknél tapasztalható, prevalenciája 1: 100 000-1: 500 000 között van, bár a populáció statisztikája nem biztos, hogy helytelen diagnózisú esetek miatt következik be. 1 A megszerzett C1-INH hiány két típusát írták le, mindkettőt a C1-INH aránytalan összetétele és kitisztulása okozta a termelt mennyiséghez képest. Ez gyakran másodlagos az alapbetegség miatt, ami a komplement pálya folyamatos aktiválódását okozza (I. típus). 1 A leggyakoribb betegségek a limfoproliferatív állapotok. Az AA betegek azonban autoantitesteket is termelhetnek a C1-INH ellen, amelyek miatt inaktív formába hasad, anélkül, hogy inaktiválnák a proteázokat, amelyekhez kötődnek (II. Típus). Mivel a megszerzett C1-INH között autoantitestekkel vagy anélkül nincs prognosztikai különbség, a két típus között már nincs diagnosztikai különbség. Ez a C1-INH csökkenés változatlanul a bradikinin szintjének emelkedéséhez vezet. Megjegyzendő, hogy az AA abban különbözik az örökletes típusoktól, hogy a komplement kaszkád aktiválásakor C1q-t és C4-et is fogyaszt.
ACE-gátló és gyógyszer által kiváltott angioödéma. Az ACE-gátlók a vérnyomáscsökkentők általában felírt osztálya. Az ACE-gátló által kiváltott angioödéma előfordulása 0,2–0,7% között fordul elő ezeket a gyógyszereket szedő betegek körében, és sokkal nagyobb a kockázata az afro-amerikaiaknak. Valójában az állapot ötször gyakoribb az afro-amerikaiaknál, mint a fehéreknél. 2 Fokozott a kockázata az immunszuppresszív terápiát igénybe vevő betegek számára is, akiknek kórtörténetében dohányzottak, idősebbek vagy nők. 1,8-10 Egy multicentrikus vizsgálat megállapította, hogy az ACE-gátló által kiváltott angioödéma az angioödémás betegek körülbelül egyharmadát teszi ki, akik az ED-ben jelentkeznek, de ezek csak 0,7 esetet jelentenek 10 000 ED-látogatás során. 11.
Az angiotenzin-konvertáló enzim hasítja a bradikinint és a P anyagot inaktív fehérjékké. Logikailag az ACE-gátló gyógyszerek így a bradikinin szintjének növekedését okozzák. Az a szint, amelyre a betegek hajlamosak lehetnek az angioödémára, más enzimek jelenlététől függhet, amelyek lebontják a bradikinint. A dipeptidil-peptidáz 4 (DPP-4) egy ilyen enzim. Azoknál a betegeknél, akik mind az ACE-gátlót, mind a DPP-4-gátlót szedik, az orális hipoglikémiás gyógyszerek egy csoportját, ideértve a cukorbetegség kezelésében alkalmazott szitagliptint is, nagyobb az angioödéma kialakulásának kockázata. Az immunszuppresszív gyógyszerek a DPP-4 csökkenését is okozhatják, ami megmagyarázhatja ezeknél a betegeknél az angioödéma fokozott kockázatát. 1,8-10 Az ACE-gátlókkal járó angioödéma mechanizmusa azonban nem feltételezhető immunológiai, mivel a támadások percekig vagy évekig is előfordulhatnak a gyógyszerek első bevétele után. 12 Egy másik gyógyszer, amely szerepet játszik ugyanezen útvonal befolyásolásában, a trombolitikus altepláz, amely aktiválja a kinint, és akiről kiderült, hogy orolingualis angioödémát okoz az akut stroke-os betegek kezelésében történő alkalmazás után. 13 Ezért körültekintően kell eljárni e gyógyszerek együttes alkalmazásakor, mivel az angioödéma lehetősége nagymértékben megnő.
Allergiás angioödéma. Az allergiás angioödéma az I. típusú azonnali túlérzékenységi válasz következménye. Megjelenhet önmagában vagy az anafilaxia egyéb jeleivel és tüneteivel együtt, és a hisztamin és más mediátorok IgE-közvetített felszabadulásának eredménye a hízósejtekből és a bazofilekből. 5 A hisztamin szerepe a szervezetben elsősorban immunológiai, és a négy ismert hisztamin receptor közül az 1. és a 2. típus aktívan vazodilatációt, vaszkuláris permeabilitást és folyadékfelhalmozódást okoz az interstitiumban, ami végül angioödéma kialakulásához vezet. 4 Az allergiás angioödéma az egyik leggyakrabban előforduló forma; valójában a thaiföldi Mahidol Egyetem 2007-es tanulmánya azt találta, hogy az összes beiratkozott angioödéma becsült 45,7% -a tapasztalt allergiás angioödémát, ezeknek az eseteknek a 41,7% -át étel, 39,6% -át pedig gyógyszerek okozták. 14
Idiopátiás és más típusú angioödéma. Az idiopátiás angioödéma bármely életkorban előfordulhat, de leggyakrabban a 40-50 éves korosztályban fordul elő. A nőket gyakrabban érintik, mint a férfiak, bár a férfiaknál ez gyakoribb lehet, ha nincs urticaria. 2 A krónikus idiopátiás angioödéma konkrét oka nem ismert, de az epizódok öt vagy több évig is megismétlődhetnek, és a betegség rendkívül alacsony kockázatot jelent a légúti szövődmények szempontjából. 5.
A nem hisztaminerg idiopátiás angioödéma a visszatérő angioödéma leírására szolgál olyan betegeknél, akik nem reagálnak a nagy dózisú antihisztaminokra, családjukban nincs angioödéma és magas a bradikinin szintjük. A bradikinin emelt szintjének oka jelenleg még nem jól ismert, és ezt a diagnózist csak akkor állítják fel, miután az összes többi vizsgálat nem tudta megmagyarázni a visszatérő tüneteket azoknál a betegeknél, akik hat vagy 12 hónapos időszakban három vagy több rohamot tapasztaltak. 1,15 Úgy gondolják, hogy az angioödéma rezgéssel, hőmérsékleti szélsőségekkel vagy napsugárzással kapcsolatos egyéb formái (gyakran csalánkiütéssel járnak) hisztamin-közvetítettek a hízósejtek degranulációján keresztül, ezek a fizikai ingerek miatt. Az antihisztaminok hatékony kezelést nyújthatnak ezekben az esetekben. 16-18
Bonyodalmak
Az angioödéma számos megnyilvánulása létezik, főként a puszta összetettség és a kórfolyamat okainak széles skálája miatt. Az angioödéma helye és súlyossága annak típusától és az egyes betegek bevonásának mértékétől függ. Így ennek a betegségnek a szövődményei egyszerűen kényelmetlenek, például végtagi ödéma és életveszélyesek; az angioödéma jelentős morbiditást és mortalitást okozhat.
A hasi fájdalom viszonylag gyakori a HAE-ben. Egy tanulmány kimutatta, hogy 153 HAE-ben szenvedő beteg életében összesen 33 671 hasi fájdalomrohamról számolt be. 19 Egy másik retrospektív HAE-betegek vizsgálata kimutatta, hogy 209 beteg közül 195-nek visszatérő hasi fájdalma volt, összesen 62 503 hasi roham volt. Az angioödéma másodlagos hasi fájdalma hányingerrel, hányással, hasmenéssel, hipotenzió tüneteivel és asciteszel járhat. Néhány kevésbé gyakori társult tünet a dysuria, a vérzéses hasmenés, a tetania és az intussuscepció, és a betegek keringési sokkot is tapasztalhatnak a hypovolemia miatt. 19 A hasi tünetek elsősorban a bélfal ödémája következtében fellépő zsigeri kellemetlenségek miatt következnek be. Ezért fontos, hogy az angioödéma az akut hasi fájdalom lehetséges oka legyen az ED-ben. A felesleges műtéti beavatkozás megelőzésében segíthet annak ismerete, hogy a betegnek személyes vagy családi kórtörténetében angioödéma van, vagy a betegség kockázata (azaz ACE-gátló alkalmazása). 21
Az angioödéma legveszélyesebb és közvetlenül a szövődménye a légutak kompromisszuma. A légúti kompromisszum által leginkább veszélyeztetett betegek közé tartoznak azok, akiknél az arc, az ajkak, a gége, az uvula és a nyelv duzzanata van. Ezeken a területeken az ödéma szubjektív vagy objektív nehézlégzéssé, beszéd nehézséggé (azaz forró krumpli hangzá), stridorrá és a légutak esetleges elvesztésévé fejlődhet. A légutak kompromisszumának e kezdeti jeleit és tüneteit időben fel kell ismerni a gyors és potenciálisan életmentő cselekvés megkönnyítése érdekében.
Megkülönböztető diagnózis
Sok olyan betegségfolyamat létezik, amely összetéveszthető angioödémával. A 3. táblázat ezek közül többet felsorol, beleértve mind a ritka, mind a gyakori állapotokat.
- Mi a teendő, ha a betegek elutasítják az ételt és a vizet? 2000-06-01 AHC Media továbbképzés
- A súlygyarapodás előnyeinek megértése és kezelése a dohányzásról való leszokás után - JEMS
- Az atópiás dermatitis megértése
- A mikotoxinok megértése és leküzdése a baromfiban a baromfitelepet táplálja
- A szénhidrát-glükóz és a vércukor megértése a cukorbetegség legyőzéséhez