A gasztrointesztinális autonóm neuropathia kezelése
Absztrakt
Fontos kiemelni a diabetes mellitusban a gasztrointesztinális autonóm neuropathia által okozott tüneteket, mivel a cukorbetegek nagy részét érintik, függetlenül attól, hogy ez 1. vagy 2. típusú. Gastroparesis és a bélműködési zavar általános jelei, mint például székrekedés, hasmenés és a hasi fájdalom leggyakrabban előfordul, és mind farmakológiai, mind nem farmakológiai kezelési lehetőségeket tartalmaz. Ez a mini-áttekintés összefoglalja az EASD 2015. évi éves ülésén az „Autonóm diabéteszes neuropátia diagnosztizálása és kezelése a bélben” szimpóziumon tartott előadást. Ehhez a szimpózium témájának újabb mini-áttekintése (Azpiroz és Malagelada, DOI: 10.1007/s00125-015-3831-1), valamint Kempler Péter ülésszakos elnök kommentárja (DOI: 10.1007/s00125-015 -3826-y).
A gyomor-bélrendszeri (GI) tünetek gyakoriak az általános populációban. Például a felnőttek 10–20% -a szenved funkcionális GI rendellenességekben [1]. Az egyik alaposabban elvégzett epidemiológiai vizsgálatban az 1. és a 2. típusú diabetes mellitusban szenvedő betegeknél Bytzer és mtsai azt találták, hogy a GI traktus minden részéből a tünetek még gyakoribbak a cukorbetegségben, és hogy a közepesen súlyos és súlyos intenzitású GI tünetek gyengébb glikémiás kontrollhoz társul [2]. A GI traktus minden részét érintheti a GI vegetatív neuropátia, de a leggyakrabban előforduló gyomor és bél diszfunkcióval kapcsolatos.
Autonóm GI neuropathia gyanúja esetén GI funkcióteszteket hajtanak végre, és a tanulmányok azt sugallják, hogy ezek eredményeit bizonyos óvatossággal kell értelmezni a megfigyelt diszfunkció és a specifikus GI tünetek közötti esetleges összefüggés értékelése szempontjából. Például egy amerikai felmérésben nem voltak olyan külön tüneti jellemzők, amelyek megkülönböztetnék a krónikus hányingert és a gastroparesis hányást szenvedő pácienst a normál gyomorürüléstől [3].
A GI autonóm neuropátia alábbi példáiban az alapkezelés fő alappillére, mint mindig, a jó glikémiás kontroll elérése/fenntartása.
Gasztroparézis
Diétás kezelés
Az étrendi kezelés a diabéteszes gasztroparézis kezelésének alapvető alapját képezi, függetlenül a többi terápiás törekvéstől. Az általános ajánlások a kicsi, gyakoribb étkezésekre vonatkoznak; Kerülni kell a zsír- és élelmi rostfelesleget, és a részecskeméretnek kicsinek kell lennie [4]. A dietetikus támogatása növeli annak esélyét, hogy az étrend olyan tápanyag-bevitelt kapjon, amely eléri a napi energiaigényt. Úgy tűnik, hogy nagy szükség van erre a támogatásra, mivel a betegek többségének nehézségei vannak az étrendi tanácsok nyomán [5]. Általában a tünetek enyhítése szempontjából a kis szemcseméretű étkezés központi jelentőségűnek tűnik [6].
Farmakológiai kezelés
A gasztroparézis kezelésére rendelkezésre álló gyógyszerekre vonatkozó ajánlások régi kísérletek eredményein alapultak, amelyek nem felelnek meg a modern, szigorúbb bizonyítékszabványoknak [7]. E tanulmányok többsége csak a rövid távú hatásokat értékelte (
Bélműködési zavar
Ha a gasztroparézissel járó tünetek és a terápiás lehetőségek bonyolultak, akkor a helyzet ugyanaz, amikor a GI traktus távolabbi részeit érinti az autonóm neuropathia. A tüneti komplexek közötti átfedés jelentős, és a klinikai gyakorlatban a kezelési lehetőségek nagyjából megegyeznek a funkcionális GI rendellenességekkel. Nagyon fontos, hogy az orvos elmagyarázza a betegnek, hogy egy adott terápiás intézkedés mely tüneteket vagy tüneteket javíthatja, hogy a betegnek és az orvosnak is reális elvárásai legyenek az elérhető.
Székrekedés
Ha csak a székrekedés enyhítését tekintjük elsődleges eredménymérőnek, akkor viszonylag hatékony hashajtó terápia már régóta elérhető [21]. Ha a mögöttes patofiziológia lassú tranzit székrekedéssel jár, akkor az ozmotikus hashajtókat részesítik előnyben a tömeges hatóanyagok és a rostkiegészítők helyett. Az elmúlt években a prukalopridot, az 5-HT4 receptor agonistáját vezették be a klinikai gyakorlatban székrekedés kezelésére olyan nőknél, akiknél a hashajtók nem eredményeztek megfelelő enyhülést. Három sarkalatos vizsgálat kimutatta, hogy a székrekedés kulcsfontosságú tüneteire (azaz a gyakoribb bélmozgásokra) jelentős hatások vonatkoznak a placebóval szemben, emellett pozitív hatásokról számoltak be az életminőségre és megnyugtató biztonsági adatokra [22–24]. Érdekes, hogy a székrekedéssel járó egyéb tünetek, például puffadás, kellemetlen érzés, a hiányos bélmozgás érzése és a túlzott megerőltetés a kezelés által javíthatóak [25]. A legfrissebb adatok a férfiaknál is alátámasztják [26].
A székrekedés egy másik új terápiás megközelítése magában foglalja a hám guanilát-cikláz-C (GC-C) receptorának stimulálását a bél hámsejtjein. A székrekedés és a székrekedéssel járó irritábilis bél szindróma (IBS-C) kezelésére jóváhagyott, nem felszívódó linaklotid anyag ehhez a specifikus receptorhoz kötődve hat. Az események intracelluláris kaszkádja a klorid szekréciójának aktiválásához és ezáltal a víz bél lumenbe történő nettó mozgásához vezet, ami lágyabb székletet és gyakoribb bélmozgást eredményez [27]. Különösen érdekes jellemző a székrekedéssel járó hasi fájdalom [28] és a puffadás [29] csökkenése, amely hónapok alatt fokozatosan kialakulhat a kezelés kezdetétől számítva.
Végül kimutatták, hogy a kolinészteráz gátlás orális piridosztigminnel felgyorsítja a vastagbél tranzitját és javítja a bélműködést kifejezetten krónikus székrekedésben szenvedő cukorbetegeknél [30]. Ennek a vizsgálatnak az adatait nagyobb kísérletekben kell megerősíteni, mielőtt meggyőző ajánlások tehetők.
Hasmenés
Hasi fájdalom
Az autonóm neuropátia legféltettebb és gyakran bántalmazott tünete a hasi fájdalom. A központilag célzott farmakoterápia alkalmazásának logikájának megértése érdekében alapvető ismeretekkel kell rendelkezni a növekvő és csökkenő zsigeri fájdalom útjairól és a krónikus hasi fájdalom kialakulásában szerepet játszó események sorrendjéről. Egy olyan szomatikus betegségben, mint a cukorbetegség, amely neurodegenerációt is magában foglalhat, az egyes hajlamosító tényezők, például genetikai mechanizmusok, környezeti expozíció, korai trauma, bántalmazás erősen változó fájdalomhelyzetet eredményezhetnek, különösen, ha nem tartósító tényezők, például szorongás és depresszió. elismert és kezelt [32]. Az opioid hatású fájdalomcsillapítók helytelen használata hozzájárulhat a nagyon nehezen kezelhető fájdalomhelyzet kialakulásához - a kábítószeres bél szindróma [33].
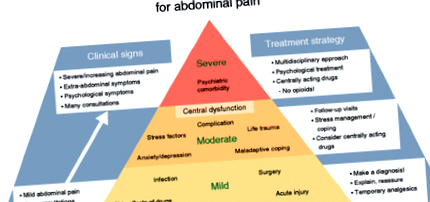
Ehelyett a neuropátiás fájdalmat jobban szabályozhatja az antidepresszáns gyógyszerek egyes osztályai és a betegeknek a fájdalom mechanizmusaira vonatkozó oktatása (1. ábra). A depresszió kezelésében és az állatmodellekben szerzett tapasztalatok azt mutatják, hogy az antidepresszánsokkal végzett farmakoterápia elősegítheti egy neuroplasztikus, regeneratív helyzet kialakulását [34, 35], amely hasznos lehet mind a neuropathia, mind a kísérő szorongás és depresszió kezelésében [36].
Fogalmi modell a régóta fennálló hasi fájdalmak kezeléséről
Sok orvos bízik abban, hogy alacsony dózisú triciklusos antidepresszánsokat (TCA) ír fel krónikus fájdalom kezelésére, de a klinikai helyzettől függően a szelektív szerotonin újrafelvétel gátlók (SSRI) és a szelektív szerotonin – noradrenalin újrafelvétel gátlók (SNRI) is hasznosak. Ha a beteg komorbid szorongásban vagy depresszióban szenved, megfelelő lehet SSRI vagy SNRI kezelés a pszichiátriai javallatokhoz ajánlott adaggal megegyező dózisban. Az SSRI-k valószínűleg a legkevesebb társított mellékhatással rendelkeznek, de az SNRI-k előnye a hivatalos indikáció a perifériás diabéteszes neuropátiás fájdalom kezelésében [37].
Záró megjegyzés
A gasztrointesztinális autonóm neuropathia kezelése kihívást jelent. A cukorbetegségben a metabolikus kontroll a legfontosabb terápiás cél, és ez a jövőben is a GI szövődmények kialakulásának kockázatának csökkentése és a hiperglikémia GI működésére gyakorolt akut hatásainak csökkentése érdekében. A bélmotilitás és a bél-agy kommunikáció idegi szabályozásában szerepet játszó specifikus mechanizmusok szerepének fokozódó betekintése azonban új terápiás lehetőségeket eredményezhet a specifikus mechanizmusok irányába, a jelenlegi kezeléseken kívül.
Rövidítések
Élelmiszer- és Gyógyszerügyi Hivatal
A vékonybél baktériumok elszaporodása
Hivatkozások
Lovell RM, Ford AC (2012) Az irritábilis bél szindróma globális prevalenciája és kockázati tényezői: metaanalízis. Clin Gastroenterol Hepatol 10: 712–721.e4
Bytzer P, Talley NJ, Leemon M, Young LJ, Jones MP, Horowitz M (2001) A diabetes mellitushoz társuló gyomor-bélrendszeri tünetek előfordulása: 15 000 felnőtt populációs alapú felmérése. Arch Intern Med 161: 1989–1996
Pasricha PJ, Colvin R, Yates K és mtsai (2011) Krónikus, megmagyarázhatatlan hányingerrel és hányással, valamint normál gyomorürüléssel rendelkező betegek jellemzői. Clin Gastroenterol Hepatol 9: 567–576.e1–4
Abrahamsson H (2007) Súlyos gastroparesisben szenvedő betegek kezelési lehetőségei. Bél 56: 877–883
Parkman HP, Yates KP, Hasler WL et al (2011) Diétás bevitel és táplálkozási hiányosságok diabéteszes vagy idiopátiás gasztroparézisben szenvedő betegeknél. Gasztroenterológia 141: 486–498, 498.e1–7
Olausson EA, Storsrud S, Grundin H, Isaksson M, Attvall S, Simren M (2014) A kis részecskeméretű étrend csökkenti a felső gyomor-bélrendszeri tüneteket diabéteszes gasztroparézisben szenvedő betegeknél: randomizált, kontrollált vizsgálat. Am J Gastroenterol 109: 375–385
Parkman HP, Hasler WL, Fisher RS, American Gastroenterological Association (2004) American Gastroenterological Association technikai áttekintés a gasztroparézis diagnózisáról és kezeléséről. Gasztroenterológia 127: 1592–1622
Janssen P, Harris MS, Jones M és mtsai (2013) A tünetek javulásának és a gyomor kiürülésének kapcsolata a diabéteszes és idiopátiás gasztroparézis kezelésében. Am J Gastroenterol 108: 1382–1391
Snape WJ Jr, Battle WM, Schwartz SS, Braunstein SN, Goldstein HA, Alavi A (1982) Metoklopramid a diabetes mellitus okozta gastroparesis kezelésére: kettős-vak, kontrollált vizsgálat. Ann Intern Med 96: 444–446
McCallum RW, Ricci DA, Rakatansky H és mtsai (1983) Orális metoklopramid multicentrikus, placebo-kontrollos klinikai vizsgálata diabéteszes gasztroparézisben. Diabetes Care 6: 463–467
Ricci DA, Saltzman MB, Meyer C, Callachan C, McCallum RW (1985) A metoklopramid hatása a diabéteszes gasztroparézisre. J Clin Gastroenterol 7: 25–32
Perkel MS, Moore C, Hersh T, Davidson ED (1979) Metoklopramid terápia késleltetett gyomorürülésben szenvedő betegeknél: randomizált, kettős-vak vizsgálat. Dig Dis Sci 24: 662–666
Patterson D, Abell T, Rothstein R, Koch K, Barnett J (1999) A domperidon és a metoklopramid kettős-vak multicentrikus összehasonlítása a gastroparesis tüneteivel rendelkező diabéteszes betegek kezelésében. Am J Gastroenterol 94: 1230–1234
Janssens J, Peeters TL, Vantrappen G és mtsai (1990) A gyomorürülés javítása diabéteszes gasztroparézisben eritromicinnel. Előzetes tanulmányok. N Engl J Med. 322: 1028–1031
Erbas T, Varoglu E, Erbas B, Tastekin G, Akalin S (1993) A metoklopramid és az eritromicin összehasonlítása a diabéteszes gasztroparézis kezelésében. Diabetes Care 16: 1511–1514
Tack J, Vanormelingen C (2014) A gasztroparézis kezelése: túl az alapokon. Curr kezelési lehetőségek Gastroenterol 12: 468–477
Abell T, McCallum R, Hocking M és mtsai (2003) Gyomor elektromos stimulációja orvosilag refrakter gasztroparézishez. Gasztroenterológia 125: 421–428
Abell TL, Van Cutsem E, Abrahamsson H és mtsai (2002) Gyomor elektromos stimulációja kezelhetetlen tüneti gasztroparézisben. Emésztés 66: 204–212
McCallum RW, Snape W, Brody F, Wo J, Parkman HP, Nowak T (2010) A gyomor elektromos stimulációja Enterra terápiával javítja a diabéteszes gasztroparézis tüneteit egy prospektív tanulmányban. Clin Gastroenterol Hepatol 8: 947–954
McCallum RW, Lin Z, Forster J, Roeser K, Hou Q, Sarosiek I (2011) A gyomor elektromos stimulációja 10 évig javítja a gasztroparézissel küzdő betegek kimenetelét. Clin Gastroenterol Hepatol 9: 314–319.e1
Ford AC, Suares NC (2011) A hashajtók és a farmakológiai terápiák hatása krónikus idiopátiás székrekedésben: szisztematikus áttekintés és metaanalízis. Bél 60: 209–218
Tack J, van Outryve M, Beyens G, Kerstens R, Vandeplassche L (2009) Prukaloprid (Resolor) hashajtókkal elégedetlen betegek súlyos krónikus székrekedésének kezelésében. Bél 58: 357–365
Camilleri M, Kerstens R, Rykx A, Vandeplassche L (2008) Prukaloprid placebo-kontrollos vizsgálata súlyos krónikus székrekedés esetén. N Engl J Med 358: 2344–2354
Quigley EM, Vandeplassche L, Kerstens R, Ausma J (2009) Klinikai vizsgálat: a prukaloprid hatékonysága, hatása az életminőségre, valamint biztonságosság és tolerálhatóság súlyos krónikus székrekedés esetén - 12 hetes, randomizált, kettős-vak, placebo- ellenőrzött vizsgálat. Aliment Pharmacol Ther 29: 315–328
Tack J, Stanghellini V, Dubois D, Joseph A, Vandeplassche L, Kerstens R (2014) A prukaloprid hatása a krónikus székrekedés tüneteire. Neurogastroenterol Motil 26: 21–27
Yiannakou Y, Piessevaux H, Bouchoucha M et al (2015) Randomizált, kettős-vak, placebo-kontrollos, 3. fázisú vizsgálat a prukaloprid hatékonyságának, biztonságosságának és tolerálhatóságának értékelésére krónikus székrekedésben szenvedő férfiaknál. Am J Gastroenterol 110: 741–748
Lembo AJ, Kurtz CB, Macdougall JE et al (2010) A linaclotid hatékonysága krónikus székrekedésben szenvedő betegeknél. Gasztroenterológia 138: 886–895.e1
Chey WD, Lembo AJ, Lavins BJ et al (2012) Linaclotide székrekedéssel járó irritábilis bél szindrómához: 26 hetes, randomizált, kettős-vak, placebo-kontrollos vizsgálat a hatékonyság és a biztonság értékelésére. Am J Gastroenterol 107: 1702–1712
Lacy BE, Schey R, Shiff SJ és mtsai (2015) Linaklotid krónikus idiopátiás székrekedésben szenvedő betegeknél közepes vagy súlyos hasi puffadásban: randomizált, kontrollált vizsgálat. PLoS One 10: e0134349
Bharucha AE, Low P, Camilleri M et al (2013) Randomizált, kontrollált vizsgálat a kolinészteráz gátlásnak a vastagbél működésére gyakorolt hatásáról diabetes mellitusban és székrekedésben szenvedő betegeknél. Bél 62: 708–715
Lavo B, Stenstam M, Nielsen AL (1987) Loperamid az irritábilis bél szindróma kezelésében - kettős-vak, placebo-kontrollos vizsgálat. Scand J Gastroenterol Suppl 130: 77–80
Tornblom H, Drossman DA (2015) Központilag célzott gyógyszeres kezelés krónikus hasi fájdalmak esetén. Neurogastroenterol Motil 27: 455–467
Kurlander JE, Drossman DA (2014) Narkotikus bél szindróma diagnosztizálása és kezelése. Nat Rev Gastroenterol Hepatol 11: 410–418
Brunoni AR, Lopes M, Fregni F (2008) A súlyos depresszió és a BDNF szintek klinikai tanulmányainak szisztematikus áttekintése és metaanalízise: következményei a neuroplasticitás depresszióban betöltött szerepére. Int J Neuropsychopharmacol 11: 1169–1180
Han X, Tong J, Zhang J és mtsai (2011) Az imipramin-kezelés javítja a fokozott hippocampus neurogenezissel járó kognitív eredményt egerek traumás agysérülése után. J Neurotrauma 28: 995–1007
Drossman DA (2009) A triciklikuson túl: új ötletek a fájdalmas és refrakter funkcionális emésztőrendszeri tünetekkel küzdő betegek kezelésére. Am J Gastroenterol 104: 2897–2902
Lunn MP, Hughes RA, Wiffen PJ (2014) Duloxetin fájdalmas neuropathia, krónikus fájdalom vagy fibromyalgia kezelésére. Cochrane Database Syst Rev, 1. szám, cikk. Sz .: CD003287. doi: 10.1002/14651858.CD003287.pub4
Szerzői információk
Hovatartozások
Belgyógyászati és Klinikai Táplálkozási Osztály, Orvostudományi Intézet, Sahlgrenska Akadémia, Göteborgi Egyetem, SE-41345, Göteborg, Svédország
A PubMed Google Scholar alkalmazásban is kereshet erre a szerzőre
- Az ideális étrend a neuropátia tüneteinek csökkentésére idegfájdalom kezelése
- Tizenéves pattanások okai, kezelése, étrend, kezelési dermatológiai CT
- Milyen ételeket szabad kerülnöm, ha neuropathiám és cukorbetegségem van
- Savannah epehólyag-problémái, kezelése, eltávolítása és diétás gasztroenterológiai tanácsadói
- A here fájdalma okai, tünetei, enyhítése és kezelése