Az optimális táplálkozás a mechanikus lélegeztetés időszakában csökkenti a halálozást a kritikus állapotú, tartósan akut nőbetegekben: prospektív megfigyelési kohorsz vizsgálat
Absztrakt
Bevezetés
Az intenzív terápiás betegek optimális táplálkozása az indirekt kalorimetriával meghatározott energiaellátás, és a napi fehérjeellátás legalább 1,2 g/kg felvétel előtti tömeg. Az ezeket a táplálkozási célokat alátámasztó bizonyítékok helyettesítő eredményeken alapulnak, és ezeket még nem támasztják alá betegorientált, klinikailag értelmes végpontok. Jelen tanulmányban értékeltük az optimális táplálkozás elérésének hatásait az intenzív osztályon szenvedő betegeknél a mechanikus szellőzés időszakában a mortalitásra.
Mód
Ez egy prospektív megfigyelési kohorsz vizsgálat volt egy vegyes orvosi-sebészeti, 28 ágyas ICU-ban egy akadémiai kórházban. 243 szekvenciális vegyes orvosi-műtéti beteget vontak be a felvétel után a 3–5. Napon, ha várhatóan még legalább 5–7 napos tartózkodás volt. A rutinellátás részeként közvetett kalorimetrián estek át. A táplálkozást a közvetett kalorimetria eredménye vezérelte, és arra törekedtünk, hogy legalább 1,2 g fehérje/kg/nap mennyiséget nyújtsunk. A kumulatív egyenlegeket kiszámítottuk a mechanikus szellőzés időszakára. Az eredmény paraméterei az ICU, a 28 napos és a kórházi halálozás voltak.
Eredmények
Nőknél a súly, a testmagasság, az Apache II pontszám, a diagnózis kategóriája és a hiperglikémiás index alapján korrigálva azoknál a betegeknél, akik táplálkozási céljaikat elérték azokhoz képest, akik nem, a kockázati arány (HR) 0,199 volt az ICU mortalitásánál (CI 0,048– 0,831; P = 0,027), a HR értéke 0,079 28 napos mortalitás esetén (CI 0,013–0,467; P = 0,005), és a kórházi mortalitás esetében 0,288 HR (CI 0,113–0,952; P = 0,04). Az energiacélok elérése, bár nem érte el a fehérje célokat, nem befolyásolta az ICU halálozását; a 28 napos mortalitás HR értéke 0,120 (CI 0,027–0,528; P = 0,005) és 0,318 a kórházi halálozás esetén (CI 0,107–0,945; P = 0,039). A férfiaknál nem találtak különbséget az optimális táplálkozással kapcsolatban.
Következtetések
Az optimális táplálkozási terápia javítja az ICU-t, a 28 napos és a kórházi túlélést a női ICU-betegeknél. Az energia- és fehérjetartalmat egyaránt elérő női betegeknek jobb eredményei vannak, mint azoknak, akik csak az energia célt érik el. A jelen tanulmányban a férfiak nem részesültek előnyben az optimális táplálkozásból.
Bevezetés
A táplálkozás a terápia szerves és fontos része az intenzív osztályon. A táplálkozási terápia célja a test fehérje tömegének megőrzése vagy helyreállítása, valamint megfelelő mennyiségű energia biztosítása. Hipotetikus alapon az optimális táplálkozás helyettesítő markerei az energia- és a fehérjeellátás szempontjából azt javasolták, hogy közvetett kalorimetriával mérve szolgáltassák az energiát, és kritikus betegek esetén 1,2–1,5 g fehérjét biztosítsanak a felvétel előtti súly kilogrammonként. betegek [1]. Kimutatták, hogy a nem megfelelő energiaellátás összefüggésben van a szövődmények előfordulásával, például felnőttkori légzési distressz szindróma, fertőzések, veseelégtelenség, nyomásgyulladás és műtéti igény [2, 3]. A közelmúltban Anbar és munkatársai [4] előzetes bizonyítékot szolgáltattak egy 50 betegből álló csoportban, amelynek várhatóan több mint három napos intenzív intenzitású tartózkodása volt, hogy a közvetett kalorimetria szerinti energiaellátás kumulatív pozitív energiaegyensúlyhoz vezetett, míg a kontroll 25 kcal/kg) negatív kumulatív energiamérleg volt; a kórházi morbiditás és a kórházi halálozás csökkent az intervenciós csoportban.
A táplálkozási támogatás javítására irányuló, bizonyítékokon alapuló algoritmusok alkalmazásával végzett vizsgálatok nem mutattak be jelentős pozitív hatást a túlélésre, de az optimális táplálkozás helyettesítő markereihez javasolt táplálkozási célokat nem sikerült elérni [5–7]. A táplálkozási terápia klinikailag releváns hatásaival kapcsolatos korábbi vizsgálatok eredményeinek hiánya tehát azzal magyarázható, hogy nem érjük el a megfelelő energia- és fehérjetartalmat.
Jelen tanulmányban elemezzük az energiaellátás elérésének hatásait közvetett kalorimetriával és legalább 1,2 g/kg felvétel előtti testtömeg biztosításával. Az optimális táplálkozás hatását kerestük a mortalitásra, mint eredményparamétert.
Anyagok és metódusok
A vizsgálatot prospektív módon egy vegyes orvosi-sebészeti betegek csoportjában hajtották végre egy felsőoktatási egyetemi kórházban. Az Amerikai Légzőellátási Szövetség (AARC) irányelvei szerint [8] hosszú távú akut ellátást igénylő betegeket, ismert vagy feltételezett táplálkozási hiányban szenvedő betegeket, valamint olyan táplálkozási és stressz-faktorral rendelkező alcsoportokat választottunk ki, amelyek jelentősen torzíthatják az előrejelzést Harris-Benedict-egyenlet. A tartós akut ellátású betegeket akkor vették fel, ha a harmadik-ötödik napon (a közvetett kalorimetria időzítése) a mesterséges táplálkozás előrelátható időszaka legalább további öt-hét nap volt; ha az életkor meghaladja a 18 évet, és ha a kórházi tartózkodás alatt első alkalommal vették fel az intenzív osztályt. A befogadás korlátozó tényezői a következők voltak: az inspirált oxigén töredéke több mint 0,6, a mandzsettákon és/vagy a mellkas lefolyóin átáramló légszivárgás, korlátozott rendelkezésre állás az anyagcsere-monitor vagy a két mérést végző intenzivista miatt, a készülék hibáinak javítása/javítása csak metabolikus monitor áll rendelkezésre, és a kezelés visszavonása a rossz prognózis miatt.
A tanulmányt a VU Egyetemi Orvosi Központ etikai bizottsága hagyta jóvá. A tájékoztatáson alapuló beleegyezés szükségességétől eltekintettek, mert a szokásos intenzív terápiás gyakorlaton kívül további eljárásokat nem vontak be, és az ebben a vizsgálatban felhasznált adatokat klinikai célokra kellett összegyűjteni. A holland jogszabályok nem írják elő a tájékoztatáson alapuló beleegyezést az ilyen klinikai protokollon alapuló kezeléshez és adatgyűjtéshez, feltéve, hogy az eredmények névtelenek.
Táplálkozási protokollunk a korai enterális táplálásra irányul, a befogadást követő 24 órán belül kezdődik [lásd az 1. kiegészítő adatállományt]. A nyugalmi energia-ráfordítás (REE) Harris-Benedict-féle 1.2-es számításának kiválasztása Alexander és munkatársai ajánlásából származik [9], ahol a tényleges REE-t összehasonlítják az ICU-ban használt képletekkel. Az AARC irányelvei szintén a Harris-Benedict-egyenletet használják. A 10% többlet az aktivitásért van Lanschot és munkatársai tanulmányából származik [10], ahol 24 órás közvetett kalorimetrikus méréseket hajtottak végre a teljes energiafelhasználás (TEE) meghatározására.
Így az energia célt a Harris-Benedict 1984 egyenlet plusz 30% határozza meg, amíg közvetett kalorimetriát nem hajtanak végre [11]. Közvetett kalorimetrikus méréseket végeznek a rutinellátás részeként, általában a felvételt követő harmadik és ötödik nap között, az AARC irányelveinek megfelelően [8].
A mérés után a kalóriatartalmat a mért REE-nél plusz 10% -ra állítottuk be az aktivitáshoz, és a táplálékot úgy állítottuk be, hogy az megfeleljen az új kalória-célnak. Ismételt méréseket végeztünk, amikor klinikailag indokolt volt, az AARC irányelveinek megfelelően. A kalóriatartalmat a legújabb kalorimetrikus méréshez igazították. A fehérjét 1,2-1,5 g/kg testtömeg-céllal látták el. A fehérjeellátásról szóló holland irányelvek szerint a 30 kg/m 2 -nél nagyobb BMI-vel rendelkező betegek fehérjeigényének kiszámításához korrigálják a túlsúlyt; 27,5 kg/m 2 BMI-t alkalmaztunk a megfelelő tömeg és a szükséges fehérje/kg/nap mennyiség kiszámításához [12].
Az energia és a fehérje célok elérése érdekében egy olyan algoritmust használtunk az enterális táplálkozáshoz, amely meghatározza a tápanyag-összetételt és a szükséges mennyiséget, hogy mindkét követelménynek megfeleljen [13]. Az alkalmazott enterális táplálékképletek a következők: Nutrison standard ® (1000 kcal és 40 g fehérje/1000 ml); Nutrison protein plus ® (1250 kcal és 63 g fehérje/1000 ml; mindkettő Numico, Zoetermeer, Hollandia); és Promote ® (1000 kcal és 63 g fehérje/1000 ml; az Abbott Nutrition cégtől, Hoofddorp, Hollandia). A parenterális táplálkozást a vizsgálati időszak alatt gyógyszertárunk kezdetben 1000 kcal és 47 g fehérjét tartalmazó liter-all-in-one oldatként biztosította, később pedig kereskedelemben kapható terméket használtak (Struktokabiven, Fresenius-Kabi AG, Bad Homburg vd H, Németország) literenként 1050 kcal és 50 g fehérjét tartalmaz.
A közvetett kalorimetriás mérések adatait adatkezelő rendszerünkbe (Metavision ®, IMD-soft, Tel-Aviv, Izrael) 2004 augusztusától vezettük be, és a felvétel ettől az időponttól kezdődött. Az adatok visszakeresése 2006 márciusában történt. A REE-t egy kaloriméterrel (Deltatrac ™ MBM-100 Metabolic Monitor, Datex-Engstrom Division, Instrumentation Corp. Helsinki, Finnország) mértük a lélegeztetőgéphez mechanikusan szellőztetett betegeknél. A méréseket 1–1,5 óra alatt végeztük nyugalmi körülmények között, az eszköz kalibrálása után.
Minden beteg életkora (évek), nem, súly (kg) és magasság (cm), BMI (kg/m 2), akut fiziológia és krónikus egészségi állapot (APACHE) II pontszám, diagnosztikai csoport, az intenzív osztályon való tartózkodás hossza ( ICU-LOS), a szellőzés hossza (LOV), becsült TEE (Harris-Benedict 1984 plusz 30%), mért REE, amelyből a TEE-t REE-ként számolták, plusz 10%, napi energia- és fehérjebevitel minden forrásból, kivéve orális bevitel Feljegyeztük a mechanikus lélegeztetés időtartamát és az összes vércukorértéket az ICU felvételi időszakában. Az ICU-LOS és a mortalitás adatait, amelyeket nem sikerült kinyerni a helyi ICU adatbázisból, a kórház információs rendszeréből szereztük be. Minden egyes beteg esetében a halálozás valószínűségét az APACHE pontszám alapján számolták ki, amelyből a csoportok standardizált halálozási arányát számították ki [14].
A betegek testsúlyához és testmagasságához előzetes felvételi adatokat használtunk, amelyeket az előzetes felmérő ambulanciáról, a felvétel során végzett korábbi mérésekből vagy más egészségügyi intézményekben nyert adatokból kaptunk. Ellenkező esetben a rokonoktól, vagy ha lehetséges, a betegtől kérték ezeket az adatokat. Ha ezeket az adatokat nem sikerült lekérni, megbecsülték a súlyt és a magasságot vagy megmérte, vagy megbecsülte a két tapasztalt intenzív szakember egyike, akik elvégezték az indirekt kalorimetrikus méréseket.
Táplálkozási adatok és számítások
A glikémiás kontroll megfelelőségének meghatározását a hiperglikémiás index (HGI) kiszámításával végeztük el betegenként mmol/l-ben az ICU teljes időtartama alatt. Egységünkben egy betegre jutó átlagos glükózminta napi 6,2. A HGI a görbe alatti terület, amelyet a normál felső határa (glükózszint 6,0 mmol/l) felett osztanak el, elosztva a teljes ICU-LOS értékkel [15].
Az eredményváltozók az ICU-ban bármilyen okból bekövetkezett halál, a 28 napos halálozás és a kórházi halálozás voltak.
Statisztikai analízis
A leíró adatokat átlagként és szórásként, mediánként és tartományban, vagy gyakoriságként és százalékban jelentik.
Cox regresszióanalízis a kórházi LOS-szal mint időváltozóval, az ICU, a 28 napos és a kórházi halálozás mint az eredményváltozók és az elért táplálkozási cél (igen/nem), az elért energetikai cél (igen/nem) és az elért fehérjetartalom (igen/nem) mint független változók. Mivel a nemet jelentős hatásmódosítónak találták, az adatokat külön elemeztük a férfiak és a nők esetében. Az összes bemutatott veszélyességi arányt (HR) korrigálták a súly, a magasság, az APACHE II pontszám, a diagnózis kategóriája és a HGI szempontjából. A statisztikai elemzéshez az SPSS 14-et (SPSS Inc., Chicago, IL, USA) használtuk. A P
Eredmények
Kétszáznegyvenhárom szekvenciális beteg teljesítette a felvételi kritériumokat. Ezek közül 184 beteget kizárólag enterális táplálékkal, négy beteget kizárólag parenterális táplálékkal tápláltak, 55 beteget pedig enterális és parenterális táplálékkal a mechanikus lélegeztetés ideje alatt. A közvetett kalorimetrikus mérést megelőző Harris-Benedict-képlet 13,2% -nál kevesebb, mint 10% -kal alábecsülte, a becslések 70,4% -a +/- 10% -on belül, 16,5% -ánál pedig 10% -nál nagyobbra becsülték fel; + 0,9% -os torzítás teszi az előrejelzést elfogadhatóvá egy csoport számára. A jóslat azonban erősen eltérhet az indirekt kalorimetrikus értéktől egyes betegeknél, maximális negatív hibája 23,8%, maximális pozitív hibája pedig 38,8%. A felvétel és a közvetett kalorimetria közötti medián időtartam hat nap volt.
A kumulatív táplálkozási célok elérése alapján a betegeket a négy csoport egyikébe soroltuk. A demográfiai, klinikai és táplálkozási adatokat az 1. és a 2. táblázat tartalmazza külön a férfiak és a nők esetében. A nők gyakrabban érték el a táplálkozási célokat, mint a férfiak (34/102; 33,3% vs 25/141; 17,7%).
A statisztikai elemzés eredményeit a 3. táblázat mutatja be. A Cox regressziós elemzés nem mutatott ki szignifikáns hatást a táplálkozási célok elérésének a férfiak halálozására.
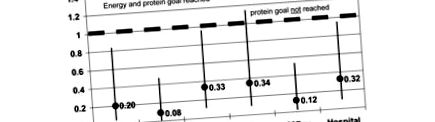
A lakosság női részénél az ICU, a 28 napos és a kórházi halálozás HR-je szignifikánsan alacsonyabb volt az energia- és fehérjetartalmat egyaránt elérő csoportnál, összehasonlítva azzal a csoporttal, amely nem érte el mindkét célt. A legerősebb hatásokat a 28 napos mortalitáson tapasztaltuk (HR = 0,079; konfidencia intervallum (CI) = 0,013-0,467; P = 0,005). Az energia és a fehérje célok elérésének hatása nyilvánvalóbb, mint amikor csak az energia célt érjük el (1. ábra). Ez utóbbi esetben az intenzív vészhelyzeti mortalitás HR-je nem érte el a jelentőségét. A kórházi halálozás HR-je ugyanakkor egyenértékű e két csoport között.
A nők veszélyességi aránya az elért energetikai cél és az elért fehérjetartalom szerint vagy sem. ICU = intenzív osztály.
A 3. táblázat a fehérje célt elért vagy nem elérő csoportok összehasonlításának eredményeit is mutatja, függetlenül az energia céltól, és az energia cél elérésének eredményeit, ha nem, a fehérje céltól függetlenül. A táplálkozási célcsoportonkénti és nemenkénti standardizált halálozási arány elemzése alacsony előre jelzett/megfigyelt halálozási arányt mutatott azoknál a nőknél, akik mind az energia, mind a fehérje célt elérték, de a férfiaknál ez a hatás hiányzott.
Vita
A táplálkozási célok elérése, ebben a tanulmányban a mért REE minimum 90% -ának plusz 10% -kal és legalább 1,2 g/kg fehérjetartalmú, a befogadás előtti testtömeg energiaellátásával definiálva a mechanikus szellőzés időszakában 80 % -kal csökkent a halálozás esélye az intenzív osztályon, és 92% -kal csökkent a 28 napos halálozás, míg a kórházi halálozás 67% -kal alacsonyabb, mint azoknál a betegeknél, akik nem érik el a fent említett táplálkozási célokat. Ezek a hatások csak az ICU populáció női részén jelentkeznek. Férfiaknál nem volt kimutatható a táplálkozás statisztikailag szignifikáns hatása az eredményre.
Csak az energiacél elérése és a napi 1,2 g fehérje elérése a nőknél kevésbé kedvező eredményeket eredményez, mint amikor mind az energia, mind a fehérje célokat elérik. Az ICU-ban való halál esélyét nem befolyásolja, ha csak az energetikai célt érjük el, de továbbra is csökken az esély a halálra 88% 28. nap után és 68% -kal csökken a kórházi halálozás.
A nők csoportja alacsonyabb testtömegű, így kevesebb energiát fogyaszt, mint a férfiak. Mivel az enterális táplálkozási formulák mennyiségének beadása korlátozó tényező a táplálkozási terápia korai szakaszában, a nők nagyobb valószínűséggel teljesítik táplálkozási céljaikat.
Az energiahiány különösen a befogadást követő első napokban jelentkezik, amikor a visszatartás, a táplálkozási mennyiség lassú növekedése a célzott mennyiség felé, a hemodinamikai instabilitás, valamint a diagnosztikai és terápiás beavatkozások miatt nem lehet beadni a megcélzott mennyiséget.
Nemrégiben Pichard és munkatársai [16] bebizonyították, hogy a befogadás első három napján 1500 kcal/nap feletti adagolás a parenterális glükóz mellett csökkenti az ICU és a kórházi halálozást. A korai energiaellátás csökkenti a kumulatív kalóriahiányt.
Tudomásunk szerint tanulmányunk az első, amelyben kimutatták az energia- és a fehérjeellátás jótékony hatását a kritikus betegek halálozására.
Így hihető, hogy a tanulmánytervek, a bevont betegek száma, a táplálkozási célok különböző meghatározása és a csoportszintű elemzések közötti különbségek az egyes betegek szintjén végzett elemzések helyett a táplálkozás különböző hatásainak megállapítását jelentik a mortalitásra.
Vizsgálatunknak vannak korlátai. Ez egy megfigyelési tanulmány. Sem a testösszetételt nem sikerült megállapítani, sem a nitrogénmérlegeket nem hajtották végre, így a nettó fehérje veszteség és a mortalitás közötti feltételezett összefüggést nem lehetett megalapozni. A hasonló vizsgálatokhoz hasonlóan a felvétel előtti súly nem minden beteg esetében volt pontosan ismert. Bár a statisztikai elemzés során korrigáltuk a súlyt, a magasságot, az APACHE-II-t, a diagnosztikai csoportot és a glikémiás kontrollt, lehetséges, hogy más tényezők is befolyásolhatják a mortalitást. Bár az optimális táplálkozás hipotézise nem veszi figyelembe a nemet, csak a nők mortalitására gyakorolt hatást tudtuk kimutatni. Ezenkívül a kritikus betegeknél az energia- és fehérjeellátás mennyiségére vonatkozó ajánlások csak korlátozott számú tanulmányból származnak, és bizonyulhat, hogy nem eléggé szabottak az ilyen sokszínű populáció egyéni szükségleteihez [19–22].
Következtetések
Összegzésként elmondhatjuk, hogy tanulmányunk fő megállapítása az, hogy mind a közvetett kalorimetria által vezérelt energetikai cél, mind a fehérje biztosítása legalább 1,2 g/kg felvétel előtti testtömegben a mesterséges táplálkozás ideje alatt, miközben mechanikusan szellőztetik, csökkenti ICU, 28 napos és kórházi halálozás a népesség női részén. A nőknek az ICU-halálozásra gyakorolt kedvező hatása nem volt kimutatható azok számára, akik elérték az energetikai célt, de nem értek el napi 1,2 g fehérjét/kg. A hímek esetében nem lehet kimutatni, hogy a mesterséges lélegeztetés ideje alatt ezek a táplálkozási célok elérése jótékony hatással lenne a mortalitásra.
Bár megállapításainkat másoknak is meg kell erősíteniük, azzal érvelünk, hogy a táplálkozás megfigyelt jótékony hatása a nőstényekben annyira kifejezett, hogy végső erőfeszítéseket kell tenni mind az energia, mind a fehérje megfelelő ellátásának biztosítására. További kutatásokra van szükség az alapmechanizmusok tisztázásához, hogy megmagyarázzuk a táplálkozás, a nem és a halálozás összefüggését az ICU-betegeknél.
Kulcsüzenetek
Optimális táplálkozás az intenzív terápiás betegeknél úgy határozható meg, mint a ténylegesen felhasznált energia és a fehérje mennyisége 1,2–1,5 g/kg a betegség előtti testtömeg/nap.
Eddig az optimális táplálkozás célja a helyettes végpont volt; ez a tanulmány azt mutatja, hogy a női betegek hosszú távú akut ellátása szempontjából az optimális táplálkozás befolyásolja a klinikailag releváns eredményeket.
Azok a női betegek, akik elérik az energia- és fehérje-céljukat, szignifikánsan alacsonyabb ICU-értékkel, 28 napos és kórházi halálozással rendelkeznek, mint azok, akik nem érik el ezeket a célokat.
A női betegek hosszú távú akut gondozásában mind az energia, mind a fehérje célok elérése előnyösebb, mint csak az energetikai cél elérése: ez utóbbi esetben az ICU halálozását ez nem befolyásolja, és a 28 napos halálozásra gyakorolt hatás kevésbé nyilvánvaló, ami arra utal, hogy a fehérje cél elérésének jótékony hatása különösen fontos a kritikus betegség korai szakaszában.
Jelen tanulmányban az optimális táplálkozás jótékony hatásait nem sikerült kimutatni népességünk férfi részén.
Rövidítések
Amerikai Légzőgondozó Egyesület
akut fiziológia és krónikus egészségi állapot értékelése
- Optimális étrend és táplálkozás a focisták számára
- Szuper táplálkozás csecsemőknek A baba etetésének helyes módja az optimális egészség érdekében Katherine Erlich
- Optimális táplálkozási programozás és coaching; Metabolikus megoldások
- Táplálkozás periodizálása az állóképességű és erőteljes sportolók számára az élet optimális táplálkozása
- Táplálkozással kapcsolatos információk a táplálkozásról - Étrend-kiegyensúlyozók a lovak számára