Helicobacter pylori fertőzés Japánban
Seiji Shiota
1 Környezetvédelmi és Megelőző Orvostudományi Tanszék, Oita Egyetem Orvostudományi Kar, 1-1 Idaigaoka, Hasama-machi, Yufu City, Oita 879-5593, Japán
2 Általános Orvostan Tanszék, Oita Egyetem Orvostudományi Kar, 1-1 Idaigaoka, Hasama-machi, Yufu City, Oita 879-5593, Japán
Kazunari Murakawi
2 Általános Orvostan Tanszék, Oita Egyetem Orvostudományi Kar, 1-1 Idaigaoka, Hasama-machi, Yufu City, Oita 879-5593, Japán
Rumiko Suzuki
1 Környezetvédelmi és Megelőző Orvostudományi Tanszék, Oita Egyetem Orvostudományi Kar, 1-1 Idaigaoka, Hasama-machi, Yufu City, Oita 879-5593, Japán
Toshio Fujioka
2 Általános Orvostan Tanszék, Oita Egyetem Orvostudományi Kar, 1-1 Idaigaoka, Hasama-machi, Yufu City, Oita 879-5593, Japán
Yoshio Yamaoka
1 Környezetvédelmi és Megelőző Orvostudományi Tanszék, Oita Egyetem Orvostudományi Kar, 1-1 Idaigaoka, Hasama-machi, Yufu City, Oita 879-5593, Japán
3 Orvosi Osztály – Gasztroenterológia, Baylor College of Medicine és Michael E. Debakey Veterans Affairs Medical Center, 2002 Holcombe Blvd. Houston, TX 77030, USA
Absztrakt
A Helicobacter pylori fertőzés prevalenciája fokozatosan csökken Japánban. Japán fő szigetén szinte az összes H. pylori izolátum erős virulenciával rendelkezik cagA-val és vacA-val. Kevésbé virulens H. pylori törzseket azonban gyakran találnak Okinawában, ahol a gyomorrák esete a legkevesebb Japánban. A japán nemzeti egészségbiztosítási rendszer jóváhagyta a peptikus fekély, az idiopátiás thrombocytopeniás purpura, a gyomornyálkahártyához kapcsolódó limfoid szöveti limfóma és a korai gyomorrák felszámolási terápiáját az endoszkópos reszekció után. A japán Helicobacter Research Society azonban nemrégiben kijelentette, hogy minden „H. pylori fertőzés ”tekinthető a felszámolás javallatának, a háttérbetegségektől függetlenül. A japán H. pylori felszámolása érdekében a japán egészségbiztosítási rendszernek jóvá kell hagynia az összes H. pylori fertőzés felszámolását.
Járványtan
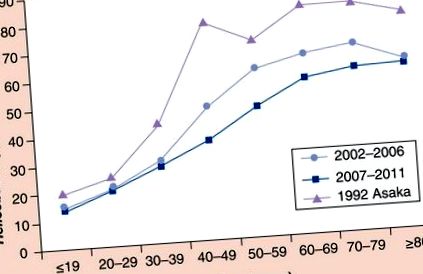
A Helicobacter pylori fertőzés prevalenciája Japánban.
A H. pylori virulencia faktorai Japánban
A gazdi tényezők és az étrend mellett a H. pylori virulencia faktorai, mint például a cagA, vacA, oipA, babA, hopQ és homA/B, bebizonyosodtak a gyomor atrófiájának, a bél metaplazia és a súlyos klinikai eredmények előrejelzőinek [8]. . Noha a gyomorrák és a nyombélfekély a betegség spektrumának ellentétes végén áll, a H. pylori fertőzés elősegíti mindkét betegség kialakulását, és a legtöbb feltételezett H. pylori virulencia faktor társult e betegségek fokozott kockázatával. Ezek a virulencia faktorok azonban nem használhatók betegségspecifikus markerekként a kelet-ázsiai országokban, például Japánban, mivel ezekben a régiókban szinte az összes H. pylori törzs rendelkezik ezen virulencia faktorokkal [8].
Például a cagA a H. pylori legtöbbet vizsgált virulenciafaktora. Bár a cagA-pozitív törzsekről beszámoltak arról, hogy súlyos klinikai kimenetelekkel járnak, különösen a nyugati országokban, nehéz kimutatni a cagA jelentőségét a klinikai kimenetelben Japánban, mert szinte az összes H. pylori törzs rendelkezik cagA-val [8]. A cagA-t tartalmazó H. pylori fertőzöttek azonban nem mindig indukálják a szérum CagA antitestet. Noha a legtöbb japán H. pylori törzs rendelkezik cagA-val, a CagA szeropozitivitás előfordulása gastritisben 53,7 és 83,3% között mozgott Japánban [9,10]. Korábban elvégeztünk egy metaanalízist, és arról számoltunk be, hogy a CagA szeropozitivitása még a kelet-ázsiai országokban is magasabb volt a gyomorrákos betegek törzseinél, mint a gyomorhurutban szenvedőknél, [11] bár az esélyarány (OR) a kelet-ázsiai országokban ennél kisebb volt a nyugati országokban. Ez arra utal, hogy az anti-CagA antitest alkalmazható biomarkerként a gyomorrák számára Kelet-Ázsia országaiban.
A teljes genom elemzések szintén hasznosak a törzsek virulencia különbségeivel kapcsolatos genetikai tényezők vizsgálatához. Kawai és mtsai. a kelet-ázsiai törzsek evolúcióját vizsgálta japán, koreai, amerikai, európai és nyugat-afrikai törzsek 20 teljes genomjának felhasználásával [25]. A filogenetikai elemzés nagyobb eltérést mutatott ki a kelet-ázsiai és az európai törzs genomjai között a gazda kölcsönhatásához kapcsolódó fehérjékben, nevezetesen a virulencia faktorokban, a külső membrán fehérjékben és a lipopoliszacharid szintézis enzimekben. A következő generációs szekvenszerek, amelyek kevesebb idő alatt és alacsonyabb költségekkel képesek elolvasni a DNS-szekvenciákat, mint a Sanger-szekvenálás, lehetővé tették nemcsak a H. pylori evolúciójának hatékony vizsgálatát, hanem új virulencia faktorokat és a gyógyszerrezisztenciával kapcsolatos genomiális változásokat is.
A H. pylori kezelése Japánban
A peptikus fekély volt az egyetlen „jóváhagyott” javallat a H. pylori felszámolási terápiára 2009-ig Japánban. 2010 júniusában a japán egészségbiztosítási rendszer elegendő bizonyíték alapján jóváhagyta a H. pylori eradikációs terápiát idiopátiás thrombocytopeniás purpura, gyomornyálkahártyával társult limfoid szövet (MALT) limfóma és korai gyomorrák után endoszkópos reszekcióval.
A japán Helicobacter Research Society (JSHR) által közzétett, a H. pylori kezelésére vonatkozó iránymutatásokat 2009 januárjában drámai módon felülvizsgálták [31]. Jóllehet az egyének csak kis hányadánál alakulnak ki H. pylori-val kapcsolatos betegségek, a fertőzés a legtöbb fertőzött betegnél hosszú ideig fennáll, spontán eltűnés nélkül. Ezért a fertőzött betegeknél nagy a kockázata a H. pylori-val kapcsolatos betegségek, különösen a gyomorrák kialakulásának. Ezenkívül a sikeres felszámolási terápia a szövettani gyulladás, az aktivitás és az atrófia jelentős javulását indukálta a 10 éves prospektív nyomonkövetési vizsgálatokban [32,33]. Így a JSHR arra a következtetésre jutott, hogy minden „H. pylori fertőzés ”a felszámolás indikációjának tekinthető, függetlenül a háttérbetegségektől. Azonban csak négy betegség, köztük a peptikus fekély, az idiopátiás thrombocytopeniás purpura, a gyomor MALT limfóma és az endoszkópos reszekció utáni korai gyomorrák felszámolási terápiáját hagyja jóvá a japán egészségbiztosítási rendszer a fent leírtak szerint. A H. pylori mielőbbi felszámolása szükséges, hogy a japán nemzeti egészségbiztosítási rendszer jóváhagyja a H. pylori felszámolását minden H. pylori fertőzés esetén.
A japán egészségbiztosítási rendszer által jóváhagyott első vonalbeli terápia a klaritromicin (CAM) alapú hármas terápia. Négy protonpumpa-gátló (PPI), beleértve a lansoprazolt, az omeprazolt, a rabeprazolt és az ezomeprazolt. Háromszoros terápia, beleértve az LPZ-t, az amoxicillint (AMPC) és a CAM-ot, egylapos tablettaként alkalmazható, amelyet a Takeda Pharmaceutical Company Ltd. (Oszaka, Japán) készített. Noha a H. pylori felszámolási terápiát csak négy betegség esetében engedélyezték, a sikeres felszámolási arány Japánban csökken. A CAM-rezisztens H. pylori a sikertelen felszámolási terápia fő oka Japánban [31]. A gyermekgyógyászati, légzőszervi és otorinolaryngológiai gyakorlatban a CAM használatának növekedését tekintik az oknak. A 2002 és 2006 között öt éven át végzett éves megfigyelés azt mutatta, hogy az átlagos országos CAM-rezisztencia arány 18,9-ről (2002) 27,2% -ra (2006) nőtt [34]. A 2007 és 2009 között végzett nagyszabású, országos, multicentrikus prospektív vizsgálat sikeres 80,7% -os felszámolási arányt mutatott, amikor az AMPC + CAM + RPZ-t alkalmazták elsőrendű felszámolási programként [35].
Mint fent említettük, a legtöbb fertőzést nem lehet felszámolni, ha a betegek nem rendelkeznek a japán egészségbiztosítási rendszer által jóváhagyott négy betegség egyikével. Ezek a betegek azonban remélik, hogy H. pylori felszámolási terápiát kapnak. Ezért néhány intézmény külön klinikát épített a H. pylori diagnosztizálására és terápiájára, ahol a fertőzés a japán nemzeti egészségbiztosítási rendszer beavatkozása nélkül felszámolható. Sok esetben a JSHR által igazolt orvosok ott kezelik ezeket a személyeket. Ha minden fertőzött személy meggyógyul, számos peptikus fekély és gyomorrák kialakulása ellenőrizhető Japánban. A gyomorrák kockázata azonban a H. pylori fertőzés meggyógyítása után is fennáll. Ezenkívül tájékoztatott beleegyezést kell adni a mellékhatások magyarázatának ezeknek a betegeknek, mivel a japán egészségbiztosítási rendszer nem hagyta jóvá az eradikációs terápiát a fertőzött személyek ezen csoportjára. Tíz évnél hosszabb endoszkópos vizsgálat szükséges a H. pylori fertőzés meggyógyítása után is.
Szakértői kommentár
Ötéves nézet
A következő 5 évben a japán H. pylori fertőzés kezelése szempontjából fontosnak tartott kérdéseket az alábbiakban tárgyaljuk.
A H. pylori fertőzés arányának folyamatos figyelemmel kísérése;
Olyan faktor (ok) meghatározása, amelyek megjósolhatják az eradikációs terápia hatékonyságát a gyomor MALT-limfóma, az idiopátiás thrombocytopeniás purpura és a korai gyomorrák ellen endoszkópos reszekció után;
Az ezomeprazolt tartalmazó CAM-alapú hármas terápia hatékonyságának értékelése első vonalbeli eradikációs terápiaként;
A CAM és/vagy az MNZ elleni rezisztencia arányának folyamatos vizsgálata és bizonyítékok gyűjtése a harmadik vonalbeli eradikációs terápia hatékonyságáról;
A kábítószer-kiterjesztés a japán nemzeti egészségbiztosítási rendszer segítségével alkalmazható.
Kulcskérdések
A Helicobacter pylori fertőzés aránya Japánban fokozatosan csökken.
Bár Japánban szinte az összes H. pylori törzs rendelkezik a legtöbb virulencia faktorral, a cagA szignifikánsan társult súlyos gastroduodenalis betegségekkel Okinawában, ahol a gyomorrák előfordulása a legkevesebb Japánban.
A japán egészségbiztosítási rendszer jóváhagyta a peptikus fekély, az idiopátiás thrombocytopeniás purpura, a gyomornyálkahártyához kapcsolódó limfoid szöveti limfóma és a korai gyomorrák felszámolási terápiáját az endoszkópos reszekció után.
A japán Helicobacter Research Society által a H. pylori kezelésére vonatkozó iránymutatások 2009-ben arra a következtetésre jutottak, hogy minden „H. pylori fertőzés ”a betegség felszámolására utaló jelzésnek tekinthető, függetlenül a háttérbetegségektől, bár a fertőzöttek csak kisebb részének vannak klinikai eredményei a japán egészségbiztosítási rendszer által elfogadott H. pylori felszámolási terápiában.
A gyomorrák a H. pylori fertőzés meggyógyítása után is kialakulhat.
A klaritromicin-rezisztens H. pylori növekedése az első vonalbeli irtás sikeres ütemének csökkenését okozta. Az eradikációs terápia sikere a klaritromicin helyett metronidazol alkalmazásával biztosítható azoknál a betegeknél, akik nem reagálnak az első vonalbeli eradikációs terápiára.
Köszönetnyilvánítás
Ez a jelentés olyan munkán alapul, amelyet részben az NIH támogatásai (DK62813), a Japán Oktatási, Kulturális, Sport-, Tudományos és Technológiai Minisztérium tudományos kutatásához nyújtott támogatások (22390085 és 22659087) támogatnak, külön koordinációs alapok a tudomány és a technológia támogatására a Japán Oktatási, Kulturális, Sport-, Tudományos és Technológiai Minisztériumtól, valamint egy kutatási alap az Oita Egyetem elnökének döntése alapján.
Ez magában foglalja a foglalkoztatást, a tanácsadást, a tiszteletdíjat, a részvénytulajdont vagy opciókat, a szakértői vallomást, a kapott vagy függőben lévő támogatásokat vagy szabadalmakat, vagy a jogdíjakat.
A kézirat elkészítéséhez nem használtak írásbeli segítséget.
Lábjegyzetek
Pénzügyi és versengő érdekek nyilvánosságra hozatala
A szerzőknek nincs más releváns kapcsolatuk vagy pénzügyi kapcsolatuk egyetlen olyan szervezettel vagy szervezettel sem, amely pénzügyi érdekeltséggel rendelkezik vagy pénzügyi konfliktusban van a kéziratban tárgyalt témával vagy anyagokkal kapcsolatban.
Hivatkozások
A külön megjegyzéseket az alábbiak szerint emelték ki:
- A Helicobacter pylori fertőzés kezelése - amerikai családorvos
- Helicobacter fertőzés kis állatokban - Emésztőrendszer - Merck Állatorvosi kézikönyv
- A magas diétás sótartalom súlyosbítja a Helicobacter pylori által kiváltott gyomor karcinogenezis fertőzést
- Helicobacter pylori fertőzés gyermekek tápláltsági állapotában és társulásai a szérum leptinnel,
- Helicobacter pylori fertőzés és bőrbetegségek DermNet NZ