Kálium-permanganát
Kapcsolódó kifejezések:
- Metkatinon
- Mangán
- Kokain
- Fehérje
- Sósav
- Amyloid
- Oxidálószer
- Myeloma
- Amyloidosis
Letöltés PDF formátumban
Erről az oldalról
Vízfertőtlenítés
Kálium-permanganát
A kálium-permanganát erős oxidálószer, bizonyos fertőtlenítő tulajdonságokkal. A hipokloritok előtt széles körben használták ivóvíz fertőtlenítőszerként. A világ egyes részein még mindig kis mennyiségben használják erre a célra, valamint gyümölcsök és zöldségek mosására is. Leggyakrabban 1–5% -os fertőtlenítő oldatként használják, és gyakran 1 g-os csomagokként értékesítik 1 liter vízhez. Ennél a koncentrációnál az oldatok mély rózsaszíntől liláig színeződnek, és elszínezhetik a felületeket. Bár a baktériumok inaktiválása mérsékelt koncentrációval és érintkezési idővel érhető el, nem ajánlható terepi használatra, mivel kvantitatív adatok nem állnak rendelkezésre a vírusokról vagy a protozoon cisztákról.
Vízfertőtlenítés
Kálium-permanganát
A kálium-permanganát erős oxidálószer, bizonyos fertőtlenítő tulajdonságokkal. A hipokloritok előtt széles körben használták ivóvíz fertőtlenítőszerként. Jelenleg is erre a célra használják, valamint gyümölcsök és zöldségek mosására a világ egyes részein. Általában 1–5% -os oldatként használják fertőtlenítésre; ezeknél a koncentrációknál az oldatok mélyrózsa vagy lila színűek és foltosak. Néhány országban 1 g-os csomagokat adnak 1 liter vízhez. A baktériumok inaktiválása mérsékelt koncentrációval és érintkezési idővel érhető el, de nem ajánlható terepi használatra, mivel kvantitatív adatok nem állnak rendelkezésre a vírusokról vagy a protozoon cisztákról, annak ellenére, hogy a vegyszert gyakran használják a világ bizonyos részein.
Öt tagú gyűrűk, két heteroatommal, mindegyik kondenzált karbociklusos származékkal
4.01.7.2.3. Karbonilcsoportok és származékai
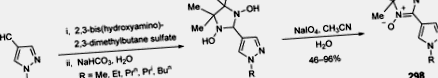
1,3-szubsztituált 1H-pirazol-4-karbaldehid N, N-dimetil-hidrazonok 314 reagált a Vilsmeier – Haack reagenssel, az aza-amin koncepció alkalmazásával, elektrofil szubsztitúciós reakcióban az azometin C-atomnál, így 1,4,5-triaza-pentadienium-sókat kaptak 315 ( 29. séma ). Ezeket hidrolizálva 2-hidrazono-2- (1H-pirazol-4-il) etanálokat kapunk 316 . Az elektrofil támadás nem a pirazolok 5'-es vinilogén helyzetében következett be.
Neurotoxikus szerek
Kezelés
A kezelés szupportív ellátásból és gyomor-bél fertőtlenítésből áll, gyomormosással kálium-permanganát (KMnO 4) 1: 5000 oldattal. A csökkent GI-mozgékonyság miatt a lemosás még a mérgezés késői szakaszában is hasznos lehet. Az aktív szén több dózisban hasznos a méreganyagok bélből történő felszívódásának csökkentésére. A következő kezelést kell alkalmazni: 0,5 mg prosztigmin SC injekció; pilokarpin-nitrát; és klóraldehid vagy lassú hatású barbiturát (ne adjon morfiumot). A fizosztigmint csak súlyos hallucinációkra és agitációs esetekre szabad fenntartani. 2 mg IV-et lassan injektáljon néhány perc alatt. Ismételje meg az adagot 10 percenként, amíg az életveszélyes állapot megszűnik. Azonban ne lépje túl a 4 mg-os dózist 30 perc alatt.
Gyűrűrendszerek legalább két kondenzált heterociklusos öt- vagy hattagú gyűrűvel, hídfő-heteroatom nélkül
10.20.7 A gyűrűs szénatomokhoz kapcsolódó szubsztituensek reaktivitása
10.20.7.1 Átrendezési reakciók
A 3-alkil-fervenulinek 5-oxo-szubsztituense 24. vizes kálium-permanganáttal reagálva az imidazo [4,5-e] -1,2,4-triazin-6-onokat kapja 66 ben javasolt gyűrűnyitási – gyűrűzárási eljárással 10. séma .
10.20.7.2. A gyűrűs szénatomokhoz kapcsolódó szubsztituensek α-szénatomjának reakciói
A 3-alkil-fervenulin-származékok 67a-c az α-szénatomon a reakciók széles skáláján megy keresztül, amint az látható 11. séma . Így a 3-metil-fervenulin reakciója 67a benzaldehiddel cink-klorid jelenlétében aldol-kondenzációt eredményez, így kapjuk a 3-sztiril-fervenulint 68 . A 3-sztiril-fervenulin enyhe oxidációja 68 permanganáttal piridin/víz jégben szobahőmérsékletre állítva megkapjuk a fervenulin-karbonsavat 69 . Figyelemre méltó, hogy ez a sav hajlamos volt dekarboxilezésre, fervenulint adva 8. vízben forraljuk, de kvantitatív módon a nyers savkloriddá alakítjuk 70 tionil-kloriddal reagáltatva. A savklorid 70, általában in situ keletkezik, könnyen átalakul fervenulin-3-karboxamidokká és karboxilátokká 71. alkoholokkal és amidokkal történő reakció után, amint azt a 7. táblázat .
7. táblázat Fervenulin-3-karboxamidok és karboxilátok szintézise 71. (lát 11. séma )
3-alkil-fervenulin-származékok brómozása 67a-c változatos eredményeket adott az alkalmazott szubsztráttól és a brómozás módjától függően. Így a 3-metil-fervenulin 67a brómmal reagáltatva ecetsavban, így kapjuk a 3-dibróm-metil-származékot 72, míg a 3-etil-fervenulin 67b csak összetett és elválaszthatatlan keverékeket adott. 3-benzilfervenulin 67c a várt módon ecetsavban lévő brómmal reagáltatva jó hozamot kapunk a 3- (1-brómbenzil) fervenulinhoz 73. . Jóllehet az ecetsavban lévő bróm reakciója nem eredményez hasznos termékeket, a 3-etil-fervenulint azonban brómozni lehet N-bróm-szukcinimid/azabiszizobutironitrillel (NBS/AIBN), így 3- (1-bróm-etil) -származékot kapni. 74a jó hozammal a megfelelő dibromszármazékkal együtt 74b alacsony hozam mellett. A 3- (bróm-metil) -fervenulin 75 nagyon alacsony hozammal képződött a 3-metil-fervenulin és NBS/AIBN reakciójából, de a legjobban a dibrommetil-vegyület redukciójával érhető el. 72 ón-bromiddal.
A dibromvegyületek reakcióképessége 72 és 74b szintén feltárták, és bebizonyosodott, hogy az etilén-glikollal végzett reakció a megfelelő ciklikus acetálokat eredményezte 76, míg a vegyület reakciója 72 hidroxil-aminnal a fervenulin-3-karbaldoximot szolgáltatta 77, amelyről kiderült, hogy ellenáll a hidrolízisnek.
A monobromo-származékok reakciója 74a és 75 ezüst-acetáttal 3- (acetoxi-metil) -fervenulint kapunk 80 és 3-acetil-fervenulin 78, kiváló hozamokban ( 11. séma ). 3-acetil-fervenulin 78 és 3- (acetoxi-metil) -fervenulin 80 megadta a megfelelő alkoholokat 79 és 81. metanolos ammóniában végzett hidrolízis után.
Érdekes, hogy a metil-alkohol 81. króm-savval oxidálva 3-acetil-fervenulint kapunk 83. jó hozammal, míg ugyanazok a körülmények az alkohol átalakulását eredményezték 79 fervenulinba 8. . Ez utóbbi átalakulás kívánt terméke, azaz a fervenulin-3-karboxaldehid 82, azonban az alkohol oxidációjával, bár alacsony hozammal, meg lehet szerezni 79 mangán-dioxiddal. Fervenulin-3-karboxaldehid 82 sokkal jobb hozamot lehet elérni a 3-sztiril-fervenulin kezelésével 68 perjodáttal ozmium-tetroxid jelenlétében vagy ugyanazon szubsztrát ozonolízisével.
Aldehid 82 rendkívül reaktív volt, és hidrátként a legjobban izolálható 84a . Valóban, az aldehid átkristályosítása 82 etanolból 3- (1-etoxi-1-hidroxi-metil) -fervenulint kapunk 84b, míg az etilén-glikollal végzett reakció ciklikus acetált eredményezett 76a . Az aldehid reakcióképessége 82 p-amino-benzoil-glutaminsavval reagáltatva könnyen Schiff-bázissal képezték ki, ezt a folyamatot redukció követte, így kapták a fervenulin-alapú folsav-analógot 85 .
Új orálisan aktív hipoglikémiás szerek felkutatása során egy Hoffmann – LaRoche-i csapat a könnyen hozzáférhető (lásd a 10.20.9.2.3. Szakaszt) klór-metil-pirimido [4,3-e] -1,2,4-triazint használta. 86 kiindulási anyagként a protein tirozin-foszfatáz inhibitorok szintéziséhez 87 (az egyes hozamok nem voltak részletesek), amint azt a (12) egyenlet mutatja .
C-7 metil szubsztituensek a 7-metilpirazino [2,3-c] [1,2,6] tiadiazinon 88 aldol-kondenzációs reakciókat hajtanak végre aril-aldehidekkel, így kapjuk a 7-sztiril-vegyületeket 89 ahogy látható 12. séma . Érdekes megjegyezni, hogy a 6-metil-analógok 90 ne reagáljanak, ami a 6-metilcsoport alacsonyabb savasságának következménye .
A 6-metil-pirazino [2,3-c] [1,2,6] tiadiazin 90 kálium-permanganáttal pH 8-on reagáltattuk, így kaptuk a 6-karbonsavakat 91., ahogy látható 13. séma . A karbonsav ezt követő reakciója 91c tionil-kloriddal, majd benzil-aminhoz kapcsolva az amidot kapjuk 92 . Ismét érdekes megjegyezni, hogy a 7-metil-analógok 88 nem voltak reaktívak a permanganáttal azonos körülmények között .
10.20.7.3 A hetero szubsztituensek reakciói
A 3-amino-5,7-dimetil-pirimido [4,5-e] -1,2,4-triazin 93 (13. egyenlet) acetilezzük piridin ecetsavanhidriddel, így kapjuk a mono-acetilezett analógot 94. o kis mennyiségű (9%) megfelelő diacetilezett származékkal együtt .
A 4-amino-6-fenil-pirazino [2,3-c] [1,2,6] tiadiazin-2,2-dioxid exociklusos aminocsoportjának alkilezése 95, A (14) egyenletben látható etil-jodiddal és acetonban lévő kálium-karbonáttal a megfelelő 4-etil-amino-származékot kaptuk. 96 tiszta és hatékony módon, bár a kutatók megjegyezték, hogy az eljárás nem általános a dialkilezett termékek versenyképes kialakulása miatt. A 10.20.6.3. Szakaszban (10. és 11. egyenlet) leírt eljárás valójában a 4-alkil-amino-pirazino [2,3-c] [1,2,6] tiadiazin-2,2-dioxid hatékonyabb bevezetését jelenti.
A 6-hidrazinopirimido [4,5-e] [1,3,4] tiadiazin 44. (lásd a 10.20.5.4. szakasz (7) egyenletet ennek a vegyületnek a szintéziséhez) visszafolyatás közben dietil-oxaláttal etanolban reagálva a triazino-kondenzált rendszert kapjuk. 97, ahogy látható 14. séma . Hasonlóképpen, etanolban lévő glioxálsavval reagáltatva vegyületet kapunk 98, klór-acetonitrillel reagáltatva acetonitrilben vegyületet kapunk 99, klór-acetonnal etanolban visszafolyatás közben végzett reakcióval vegyületet kapunk 100, és a reakciót fenacil-bromiddal etanolban forraljuk visszafolyatás közben 101 . Végül 1,2-diklór-etánnal reagáltatva etanolos kálium-hidroxid jelenlétében a triazino-kondenzált pirimido [4,5-e] [1,3,4] tiadiazint kaptuk 102 .
10.20.7.4 A gyűrűs szénatomokhoz kapcsolódó helyettesítők különféle reakciói
A piperazinnal szubsztituált pirimido [5,4-e] [1,2,4] triazin 103. benzil-halogenidekkel szelektíven reagáltatva benzil-piperazinil-analógokat kap 104 amint azt a (15) egyenlet mutatja. A termékek fehérjetirozin-foszfatáz inhibitorok.
A pirido-kondenzált piridazino [3,4-e] [1,2,4] triazinium-vegyület reakciója 105 szekunder aminokkal a piridin-rész gyűrűfelnyílását eredményezve dienil-szubsztituált piridazino [3,4-e] [1,2,4] triazinok képződnek, amelyekből a pirrolidin-vegyület 106., bemutatott 15. séma, tipikus. Összetett 106. részletes tanulmányozás tárgyát képezte, és kimutatták, hogy diénként reagál fumaronitril és N-fenil-maleinimid jelenlétében, így kapva a Diels – Alder adduktokat 107. és 108., illetőleg szintén látható 15. séma . A vegyület esetében az aromázás egyszerű volt 108., ezáltal az egyszerű toluolos melegítés elegendő volt az izoindol-2,7-dionnal szubsztituált piridazino [3,4-e] [1,2,4] triazin előállításához 110 . A fumaronitril addukt hasonló reakciója 107. szükséges oxidáció 2,3-diklór-5,6-diciano-1,4-benzokinonnal (DDQ) az aromatizált dicianobenzollal szubsztituált piridazino [3,4-e] [1,2,4] triazinszármazék előállításához 109. .
- Osteochondrosis - áttekintés a ScienceDirect témákról
- Nikotinsav - áttekintés a ScienceDirect témákról
- Búzadara - áttekintés a ScienceDirect témákról
- Statikus kerékterhelés - áttekintés a ScienceDirect témákról
- Stabil angina pectoris - áttekintés a ScienceDirect témákról