A Carica papaya levélkivonat növeli a vérlemezkeszámot? Kísérleti vizsgálat egérmodellben
Sinhalagoda Lekamlage Chandi Asoka Dharmarathna
1 Padiobiológiai Tanszék, Állatorvostudományi és Állattudományi Kar, Peradeniya Egyetem, Srí Lanka
Susiji Wickramasinghe
2 Paraditológiai Tanszék, Orvosi Kar, Peradeniya Egyetem, Srí Lanka
Roshitha Nilmini Waduge
3 Srí Lanka-i Peradeniya Egyetem Orvostudományi Kar Patológiai Osztálya
Rajapakse Peramune Veddikkarage Jayanthe Rajapakse
1 Padiobiológiai Tanszék, Állatorvostudományi és Állattudományi Kar, Peradeniya Egyetem, Srí Lanka
Senanayake Abeysinghe Mudiyanselage Kularatne
4 Orvosi Tanszék, Orvosi Kar, Peradeniya Egyetem, Srí Lanka
Absztrakt
Célkitűzés
A friss Carica papaya (C. papaya) levél kivonat potenciális szerepének vizsgálata egér modellben a hematológiai és biokémiai paramétereken és a toxikológiai változásokon.
Mód
Összesen 36 egeret használtak a kísérlethez. Friss C. papaya levélkivonatot [0,2 ml (2 g)/egér] csak a tesztcsoportnak (18 egér) adtunk. Feljegyeztük az általános viselkedést, a klinikai tüneteket és az etetési szokásokat. A vér- és szövetmintákat időközönként gyűjtöttük. A hematológiai paramétereket, köztük a vérlemezkéket, a vörösvértesteket (RBC), a fehérvérsejteket (WBC), a csomagolt sejtek térfogatát (PCV), a szérum biokémiáját, beleértve a szérum kreatinint, a szérum glutamic-oxaloecetsav-transzaminázt (SGOT) és a szérum glutamikus-piruvikus transzaminázt (SGPT). eltökélt. Megvizsgálták az esetleges szövettani elváltozások szerveit.
Eredmények
Egyik csoport sem mutatta a viselkedés megváltozását vagy az élelmiszer- és vízfogyasztás csökkenését. Hasonlóképpen, az SGOT, az SGPT és a szérum kreatinin szintekben nem észleltünk szignifikáns változást a tesztcsoportban. A hisztopatológiai szervi változásokat egyik egércsoportban sem figyelték meg, kivéve a tesztcsoport három májmintáját, amelyek enyhe fokális nekrózissal rendelkeztek. A vérlemezkeszám (11,33 ± 0,35) × 105/µL (P = 0,000 04) és a vörösvértestek száma (7,97 ± 0,61) × 106/µL (P = 0,000 03) szignifikánsan megnőtt a tesztcsoportban a a vezérlők. A fehérvérsejtszám és a PCV (%) értékei azonban nem változtak szignifikánsan a tesztcsoportban. A vérlemezkeszám a tesztcsoportban a 3. naptól kezdve szignifikánsan növekedni kezdett (3,4 ± 0,18 × 105/µL), majdnem négyszeresére emelkedett a 21. napon (11,3 × 105 5/µL), miközben 3,8 × 105/µL és 5,5 × 105/µL a 3., illetve a 21. napon a kontrollban. Hasonlóképpen, a vörösvértestek száma a tesztcsoportban 6 × 10 6/µL-ről 9 × 106/µL-re nőtt a 21. napon, miközben a kontrollcsoportban közel állandó maradt (6 × 106/µL).
Következtetések
A friss C. papaya levélkivonat szignifikánsan megnövelte a vérlemezkék és a vörösvérsejt számát a tesztcsoportban a kontrollokhoz képest. Ezért nagyon fontos azonosítani a C. papaya levelek vegyi anyagait, mivel ajánlható gyógyszerként történő alkalmazásra a thrombopoiesis és az eritropoiesis fellendítésére emberekben és olyan állatokban, amelyekben ezek a sejtvonalak sérültek.
1. Bemutatkozás
A Carica papaya (C. papaya, Caricarceae család, papaya) az egyik legnépszerűbb és gazdaságilag legfontosabb növény a világon, mivel gyümölcse gyakori csemege [1]. Ez egy puha fás, egyszárú, 2-10 m magas évelő fa, amelynek törzsének csúcsából nagy palmate levelek koronája jelenik meg. A puha, üreges, hengeres törzs az alapon 30 cm átmérőtől a koronáig körülbelül 5 cm átmérőig terjed [2]. Noha Közép-Amerikában honos, a trópusok számos részén szállították.
A papaya növény lactiferous, mivel tartalmaz egy speciális sejteket, amelyek lactifers néven ismertek, és amelyek a legtöbb szövetben előfordulnak és latexet választanak ki. A csipkék latexet választanak ki, és szétszóródnak a legtöbb növényi szövetben. A papaya-latex köztudottan a négy cisztein endopeptidáz, nevezetesen a papain, a kimopapain, a glicil endopeptidáz és a karikain gazdag forrása [3]. A levelek tartalmaznak egy carpaine nevű alkaloidot és egy carposide nevű glükozidot [4].
A papaya növények különböző részeit, beleértve a gyümölcsöt, a szárított gyümölcsöt, a leveleket, a szárított leveleket, a szárakat, a magokat és a gyökereket, már régóta használják összetevőként az alternatív gyógyászatban. Például a magokat a férgek és a gyökerek elűzésére használják, a magokat pedig abortív szerként. A leveleket (különösen a lehullottakat) különféle módon használják láz, pirexia, cukorbetegség, gonorrhoea, szifilisz, gyulladás kezelésére és szeptikus sebek kötéseként [5].
A nem tesztelt növényi gyógyszerek potenciálisan károsak lehetnek az emberi egészségre. Számos hagyományos és népi gyógyszerben használt növény potenciálisan mérgező, mutagén és rákkeltő [6] - [11]. A C. papaya növények különböző részeiből - például magvakból, gyümölcsökből, gyökerekből és levelekből - származó kivonatok toxikológiai vizsgálatait számos állatmodell alkalmazásával végezték. A C. papaya éretlen gyümölcsének akut és krónikus toxicitását dokumentálták [12].
A hagyományos hatékonysági igények egy részét, amelyeket állatkísérletekkel tudományosan vizsgáltak, és azok hatékonyságát bebizonyították [13], [14]. A legújabb tanulmányok kimutatták, hogy a C. papaya levélkivonat potenciálisan sarlóellenes (a sarlósejtek képződésének gátlása) tulajdonságokkal rendelkezik [14]. Indran és mtsai. kimutatták, hogy védőhatás van patkányok gyomorfekélyeivel szemben [13]. Ezenkívül a C. papaya virágok antibakteriális hatásúak [15]. A C. papaya magjainak fogamzásgátló hatékonyságát korábban patkányokban, egerekben és nyulakban igazolták [16] - [19]. A C. papaya mag kivonat orális beadása reverzibilis hím meddőséget indukálhat, és felhasználható férfi fogamzásgátló gyógyszerészeti fejlesztésére.
Manapság számos trópusi és szubtrópusi országot eláraszt a dengue-fertőzés, amelyet a Flaviviridae családba tartozó vírusok okoznak. A dengue kezelésére nincs specifikus terápia, annak ellenére, hogy a fertőzés jelentős halálozással jár. Srí Lanka sem kivétel, ahol a dengue-fertőzés a nemzeti egészségügyi szolgálatok prioritása a megelőzés és a halálozás csökkentése érdekében [20]. Kétségbeesésében sokan igénybe vették a papaya levélkivonat burkolt használatát. Ez még a kórházban ápolt dengue-betegek esetében is alkalmazható. A C. papaya levélkivonat ajánlása a dengue-fertőzés ellen azonban etikátlan, amíg azt tudományos kutatás nem bizonyítja.
Ezért a jelen tanulmányban megvizsgáltuk a C. papaya levelek tiszta kivonatának szájon át történő bevitelének hatásait az egér modell hematológiai/biokémiai paramétereire és toxikológiai változásaira.
2. Anyagok és módszerek
2.1. Kísérleti állatok
A hematológiai és toxikológiai vizsgálatok modelljeként 6 hetes hím fehér egereket (átlagos testtömeg 32-33 g) a Srí Lankai Orvosi Kutatóintézettől nyertek. Az állatokat a Peradeniya Egyetem Orvostudományi Karának állattartó házában tartották.
Három kísérleti kísérletet hajtottak végre 2011 májusa és 2012 májusa között három egérkészlet felhasználásával. Az egereket mindhárom vizsgálat során két csoportra osztottuk: kontroll és teszt. Az első és a második kísérlethez 48 egeret használtunk (minden kísérlethez 12 egér/kontroll és 12 egér/teszt), a harmadik kísérlethez 36 egeret (18 kontroll és 18 teszt). Valamennyi egérnek szokásos kereskedelmi étrendet adtak, vízhez való szabad hozzáféréssel. A teszt- és a kontrollcsoport összes egerét fültetoválással számoztuk meg. Az első kísérlet egy pilot vizsgálat volt egy megfelelő vizsgálat megtervezése céljából, ahol a következő változókat tekintették a C. papaya levél kivonat dózisának, a vérmintavételezés időzítésének és a máj hisztopatológiai változásainak. A második vizsgálat finomította a módszertant, a harmadik pedig az itt bemutatott eredményeket szolgáltatta. Az etikai engedélyt a Srí Lanka-i Peradeniya Egyetem Állatorvos-állattudományi és Állattudományi Kar Etikai Felülvizsgálati Bizottságától kapta.
2.2. C. papaya levél kivonat elkészítése
Friss, középkorú C. papaya leveleket naponta szedtünk 7 napig. Használat előtt a leveleket megmossuk, és a szárakat eltávolítjuk. Mérés után a leveleket víz vagy más folyadék hozzáadása nélkül összekeverték. Ezután az elegyet leszűrjük, így tiszta C. papaya levél kivonatot kapunk. Végül megmértük az extraktum térfogatát, és az extraktumokat felhasználásig 4 ° C-on tároltuk. Minden alkalmazáshoz friss kivonatokat készítettünk.
2.3. A C. papaya levélkivonat adagolása
Az első kísérletben 0,5 ml (5 g)/egér/nap, a második és a harmadik kísérletben 0,2 ml (2 g)/egér/nap mennyiséget használtunk. Az első vizsgálatot egérenként megfelelő napi dózis meghatározására végeztük. A harmadik kísérletben a tesztcsoport egereit friss egymást követő napon, C. papaya levél kivonattal etettük (0,2 ml (2 g/egér/nap)), ezek közül az első napot a vizsgálat első napjának tekintettük. Hasonlóképpen a kontrollcsoport vizet kapott.
2.4. kísérleti eljárás
Az egerek testtömegét feljegyeztük az etetés megkezdése előtt, és a mérést minden második napon megismételtük a vizsgálati időszak alatt. A viselkedési tevékenységeket naponta egyszer rögzítették.
Vérkeneteket készítettünk a vérlemezkék és a vörösvérsejtek (RBC) számának értékelésére mind a teszt, mind a kontroll csoportból alternatív napokon és áldozati napokon (a 8., 14. és 21. napon azonos számú egeret áldoztak fel minden csoportból biokémiai és szövettani vizsgálat). A vérlemezkék és a vörösvértestek számát 10 vagy több mezőben számoltuk meg olajmerítés alatt (× 100). Az eljárást a film vékony vagy vastag területein megismételtük, ha az eloszlás egyenetlen volt. Ezután a vérlemezkék és a vörösvérsejtek átlagos számát úgy határoztuk meg, hogy a teljes számot elosztottuk a megtekintett mezők számával. Végül a vérlemezkék és a vörösvértestek átlagos számát megszoroztuk a megállapított területi tényezővel a becsült szám meghatározásához.
Minden csoportból (egér és kontroll) hat egeret feláldoztunk a 8., 14. és 21. napon. Vért gyűjtöttünk. Megmértük a sejtek térfogatát (PCV). A szérumot elválasztottuk és felhasználásig -80 ° C-on tároltuk. A szérum glutamikus-oxaloecetsav-transzaminázt, a szérum glutamikus-piruvikus transzaminázt és a kreatininszintet is mértük. Ezenkívül mintákat (máj, tüdő, vese, szív, belek és lép) gyűjtöttünk a szövettani és toxikológiai vizsgálatokhoz.
2.5. Szövettani vizsgálat
A mintákat pufferolt formalinban rögzítettük (10%). Paraffin szövetmetszeteket készítettünk (2-7 um vastagság). A metszeteket paraffinmentesítettük és újra hidratáltuk. A mintákat hematoxilinnal és eozinnal (H&E) festettük és fénymikroszkóp alatt figyeltük meg.
2.6. Statisztikai analízis
Asztal 1
| Paraméterek | 1. nap | 7. nap | 14. nap | 21. nap | ||||
| Ellenőrző csoport | Tesztcsoport | Ellenőrző csoport | Tesztcsoport | Ellenőrző csoport | Tesztcsoport | Ellenőrző csoport | Tesztcsoport | |
| Trombocita szám (× 10 5/µL) | 3,67 ± 0,16 | 3,36 ± 0,16 | 4,52 ± 0,15 | 9,00 ± 0,35 | 5,21 ± 0,13 | 10,86 ± 0,38 | 5,53 ± 0,12 | 11,33 ± 0,35 |
| RBC (× 106/µL) | 6,23 ± 0,17 | 5,87 ± 0,19 | 5,95 ± 0,18 | 6,63 ± 0,32 | 6,61 ± 0,28 | 7,95 ± 0,59 | 6,00 ± 0,31 | 7,97 ± 0,61 |
| WBC (× 10 3/µL) | 7,45 ± 0,23 | 7,61 ± 0,13 | 7,16 ± 0,21 | 7,62 ± 0,32 | 7,34 ± 0,15 | 7,71 ± 0,61 | 7,52 ± 0,11 | 8,01 ± 0,42 |
| SGOT (U/L) | 88,67 ± 7,60 | 118,67 ± 25,91 | 96,17 ± 40,00 | 110,17 ± 23,00 | 90,00 ± 16,47 | 90,00 ± 13,40 | ||
| SGPT (U/L) | 28,50 ± 2,70 | 24,17 ± 3,70 | 17,83 ± 4,90 | 27,67 ± 9,97 | 47,50 ± 7,40 | 42,83 ± 3,32 | ||
| Szérum kreatinin (mg/dl) | 0,12 ± 0,12 | 0,12 ± 0,02 | 0,03 ± 0,04 | 0,1 ± 0,62E-18 | 0,1 ± 6,2E-18 | 0,10 ± 0,12 | ||
| PCV (%) | 41,8 ± 0,48 | 40,83 ± 1,85 | 43,7 ± 2,72 | 40,83 ± 1,19 | 41,00 ± 4,32 | 44,83 ± 1,79 | ||
3.4. Hematológiai vizsgálat
A tesztcsoportban nem figyeltünk meg szignifikáns változást a PCV-ben a kontrollcsoportéhoz képest. Az értékek mindig a normál tartományon belül maradtak (39% -49%).
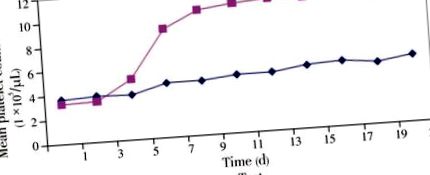
A teszt és a kontroll csoport átlagos vérlemezkeszáma a kísérlet előtt (3,36 ± 0,16) × 105/µL, illetve (3,67 ± 0,16) × 105/µL volt a kísérlet előtt. Az első 3 napban egyik csoportban sem volt szignifikáns különbség a vérlemezkeszámban. A vérlemezkeszám a tesztcsoportban azonban a 3. nap után folyamatosan emelkedni kezdett, és a 13. napon elérte a csúcsszintet (10,94 × 105/µL). Ezt követően a vérlemezkeszám viszonylag állandó maradt a 10x105 és 11x105/pl közötti tartományban. A tesztcsoport vérlemezkeszáma (11,33 ± 0,35) × 105/µL volt a kísérlet végén, összehasonlítva a kontrollcsoportéval (5,53 ± 0,12) × 105/µL (1. ábra).
A kontroll és a vizsgálati csoportok majdnem hasonló RBC-számmal rendelkeztek [6,23 ± 0,17) × 106/µL és (5,87 ± 0,19) × 106/µL a kontroll és a teszt egerekben] az 1. napon (közvetlenül az etetés megkezdése előtt). Az átlagos vörösvérsejtszám a kontrollcsoportban kisebb (6,00 ± 0,31) × 106/µL szinten maradt, kisebb ingadozásokkal. Ezzel szemben az átlagos vörösvérsejt-szám a tesztcsoportban az első két hétben folyamatosan növekedett (6.63 ± 0.32) × 106/µL-vel a 8. napon és (7.95 ± 0.59) × 106/µL-vel a 14. napon. Ezt követően állandó szinten maradt 7,97 × 106/µL körül (1. táblázat).
Eredményeink egyértelműen jelezték, hogy jelentős növekedés volt tapasztalható (P 1. táblázat). A vörösvértestek száma szintén szignifikánsan (P 5/µL és (3,67 ± 0,16) × 105/µL, illetve (11,33 ± 0,35) × 105/µL, illetve (5,53 ± 0,12) × 105/µL volt a vizsgálat végén. kísérlet: A C. papaya levél kivonat szájon át történő beadásával a vérlemezkeszámra gyakorolt hatás statisztikailag szignifikáns (P Ong H, Chua S, Milow P. A temuani falusiak által Kampung Jeram Kedah-ban (Negeri Sembilan, Malajzia) alkalmazott etno-gyógynövények. Med. 2011; 5: 95–100. [Google Tudós]
- Hízik-e a fogyókúra Egy iker tanulmány, az International Journal of Obesity
- A gyom miatt fogysz? Hogyan váltotta ki egy tanulmány a vitát - bennfentes
- A zsírszégyenítés nem segíti az embereket a fogyásban
- Növeli-e a derékméretet az igazság kibontásával
- A tej zsugorítja-e a gyomrát, vagy növeli-e a zsír egészséges táplálkozását az SF kapu