Orrödéma
Kapcsolódó kifejezések:
Letöltés PDF formátumban
Erről az oldalról
A nyugtalan láb szindróma dopaminerg terápiája
Michael H Silber, Richard P Allen, nyugtalan láb szindrómában, 2009
Gyakori káros hatások
A dopaminerg kezelés szokásos káros hatásai: hányinger, fejfájás, szédülés, orrdugulás és perifériás ödéma. Az émelygés a leggyakoribb mellékhatás, amely a kezelési utakon tesztelt alanyok 40% -ánál jelentkezik. Általában rövid életű, csak ritkán okozza a gyógyszerek abbahagyását. A fejfájás, a szédülés, a szédülés és az orrdugulás sokkal ritkábban fordult elő, és a kezelés befejezéséhez vezető problémák is ritkán fordultak elő. Ismert, hogy ezeknél a gyógyszereknél perifériás ödéma fordul elő, bár ezekben a többnyire rövid távú vizsgálatokban általában nem számoltak be róla, ahol a betegeket gondosan átvilágították az orvosi problémák minimalizálása érdekében. A többi szokásos káros hatással ellentétben a perifériás ödéma néha hónapokkal vagy évekkel jelentkezhet a kezelés megkezdése után, és ezután gyógyszeres beállítást igényelhet. A pramipexol klinikai környezetben történő alkalmazásának hosszabb távú értékelése, a perifériás ödéma beszámolt beszámolásakor, a betegek 17% -ánál fordult elő, főleg nagyobb dózisú betegeknél. 67 Ennek a káros hatásnak a késleltetett megjelenése tükrözheti más tényezők, például a csökkent aktivitás kialakulását, amelyek kölcsönhatásba lépnek a gyógyszerrel a perifériás ödéma kialakulásához.
A Parkinson-kór dopaminerg kezelésével összefüggő olyan mellékhatások, amelyekről az RLS-betegek kezelésében nem számoltak be, többek között az ortosztatikus hipotenzió, a hallucinációk és a dyskinesiák. Ha RLS-betegek dopaminerg kezelésében fordulnak elő, akkor azok sokkal ritkábban fordulnak elő, mint a Parkinson-kór kezelésében, és nyilvánvalóan ritkán okoznak jelentős klinikai problémát.
Allergiás nátha és kötőhártya-gyulladás
Szisztémás kortikoszteroidok
A szisztémás szteroidok szerepe a rhinitis kezelésében korlátozott, káros hatásaik és a betegség korlátozott morbiditása miatt. Legelőnyösebbek bármilyen típusú rhinitisben szenvedő betegek számára, akiknél kezdetben súlyos orrdugulás jelentkezik. Egy rövid orális prednizon kúra, napi 30 mg 3-5 napig, általában jelentősen csökkenti az orrödémát és lehetővé teszi az INS fokozott behatolását.
A kortikoszteroidok intramuszkuláris injekciói népszerű terápiát jelentenek, sok évre visszamenőleg. A hatékonyságot igazoló adatok azonban korlátozottak. A depószteroidok intramuszkuláris injekcióit általában el kell kerülni a szezonális allergiás nátha kezelésében a ritka, de potenciálisan katasztrofális mellékhatások, különösen a combcsont fejének aszeptikus nekrózisa miatt. Ezen túlmenően, mivel a szezonális rhinitis általában egy egész életen át tartó betegség, azoknál a betegeknél, akik ezt a kezelést évente többször igénylik és kapják sok éven át, nagyobb lehet a szisztémás kortikoszteroidok, például szürkehályog és csontritkulás hosszú távú hatásainak kockázata.
Gyermekgyógyászati középtörések
Clement Qaqish, John F. Caccamese Jr., a jelenlegi terápia száj- és szájsebészeti műtétjében, 2012
Orrtörések
Influenza
Klinikai szolgáltatások
Tünetek
Az influenza és más légúti kórokozók tünettana nagy átfedést mutat. Az influenza szindróma általában hirtelen jelentkezik, lázzal, fejfájással, köhögéssel, torokfájással, myalgiával, orrdugulással, gyengeséggel és étvágytalansággal társulva. 16,17 Az influenzaszerű betegségben szenvedő serdülők és fiatal felnőttek retrospektív vizsgálatában az influenza fertőzések legjobb előrejelzői a köhögés és a láz voltak, pozitív prediktív értékük 79% volt. 18 A kisgyermekek kevésbé klasszikus megjelenésűek, mint a felnőttek, és általában magasabb a lázuk, kevésbé kiemelkedő légzőszervi tüneteik és több gyomor-bélrendszeri tünetük, például hasi fájdalom, hányás, hasmenés és csökkent étvágy. 16,19,20 Az influenza fertőzés szintén fontos oka a lázas rohamoknak. 21
A kisgyermekek alsó légúti megnyilvánulásai gyakorlatilag nem különböztethetők meg más vírusfertőzések következtében jelentkezőktől. Az influenza, a többi légzőszervi vírushoz hasonlóan, bronchiolitist, interstitialis tüdőgyulladást, laryngotracheitist (krupit), hörghurutot, asztma súlyosbodását, zihálást és tüdőgyulladást okozhat. 22 Az extrapulmonáris megnyilvánulások közé tartozik a szívizomgyulladás, a hepatitis, az encephalitis, a myositis, a veseelégtelenség, a Guillain-Barré-szindróma, a rhabdomyolysis és a multiorganikus rendszer elégtelensége. 23–28
Fizikai eredmények
A vizsgálat eredményei között szerepel a tachypnea, a kötőhártya erythema, az orr injekciója, az ödéma, az orrfolyás és a nyaki adenopathia. A kiütés az influenza nem gyakori megnyilvánulása, de amikor előfordul, általában egy általánosított makulopapuláris kiütés kíméli a tenyerét és a talpát. Az influenza fertőzéssel járó egyéb kiütéseket petechialis, makula, papuláris, retikuláris vagy purpurikus jellegűek; lokalizálódhatnak, viszkethetnek vagy nem viszkethetnek. 29–34
Radiográfiai eredmények
Az influenza tüdőgyulladás mellkasi radiográfiai jellemzői nem különböztethetők meg más organizmusok által okozott tüdőgyulladástól. 35,36 A leggyakoribb radiográfiai leletek a kétoldalú, szimmetrikus, perihilaris és peribronchialis opacitások, de fokális opacitások és aszimmetrikus betegségek is előfordulhatnak (27.2. Ábra). 36 A nyirokcsomó megnagyobbodása előfordulhat, de a pleura effúziók ritkák. A nem specifikus eredmények miatt a vírus és a bakteriális tüdőgyulladás megkülönböztetése egyedül a radiográfiai megjelenés alapján válik nehézkessé. Az influenzás tüdőgyulladásban szenvedő fiatalabb gyermekeknél kétoldali foltos homálya lehet, ami valószínűleg a nyálka visszatartását tükrözi. 35 A tüdőgyulladás előrehaladása diffúz légtérbetegséghez vezethet ARDS képpel és akut légzési elégtelenséggel. Enyhe betegséget követően normális mellkasi röntgenfelvételre várható teljes felbontás.
Bonyodalmak
Nemi különbségek a tüdő anatómiájában és fiziológiájában
Venkatachalem Sathish, Y.S. Prakash, az élettani nemi különbségekről, 2016
Nemi szteroid hatások a hámban
A nemi szteroid szignalizáció az egész életen át jelentős szerepet játszik a légúti epithelium fenntartásában és működésében. A légúti hám a tüdő környezeti és gyulladásos ingereinek első védelmi vonala, és részt vesz a tüdőbetegségek, például asztma, COPD és fibrózis patofiziológiájában. Az ER-ek és a PR-ek az orrnyálkahártyában expresszálódnak, és a női nemi szteroidoknak szerepet játszanak az orrhám működésének modulálásában [101]. Például tanulmányok azt mutatják, hogy a menstruációs ciklus különböző szakaszaiban fokozott az orrödéma és a váladék szekréciója [102–104]. Néhány más tanulmány azt sugallja, hogy az orrnyálkahártyában az ösztrogén jelátvitel jelentősége áll fenn a rhinitis összefüggésében, amelyet az orális fogamzásgátlót alkalmazó nőknél fokozott rhinitis tüneteket mutató klinikai adatok is alátámasztanak [105]. Kísérleti állatkísérletek kimutatták, hogy megvastagodott az orrnyálkahártya exogén ösztrogénkezelés után [106,107], és a női nemi szteroidok fokozhatják a hisztamin receptorok expresszióját az emberi orrhámsejtekben és a nyálkahártya mikrovaszkuláris endothelsejtjeiben [108] .
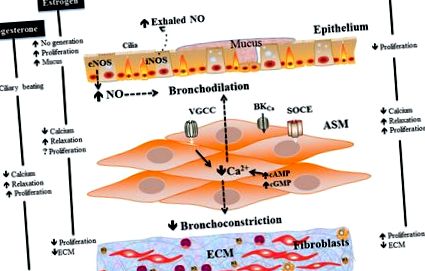
6.1. Ábra Vázlatos összefoglalás a pulmonalis fiziológia nemi különbségeiről sejtszinten, valamint a nemi szteroidok (ösztrogén, progeszteron és tesztoszteron) különböző sejttípusokra gyakorolt hatásáról.
A nemi szteroid hatások különbségeit az alveoláris hámsejtekben is megfigyelték. Például az androgének részt vesznek az alveoláris II-es típusú hámsejtek érésében és az ebből következő felületaktív anyag termelésében hím magzatokban [118–120]. Az ER-ek expresszióját, valamint PR-t és AR-t a tüdőbiopsziák alveoláris epithelialis rétegében figyeltek meg [70,121,122]. Ezenkívül az aromatáz és a 17b-hidroxi-szteroid-dehidrogenáz enzimeket az alveoláris hámban is megfigyelik [123,124], bemutatva a nemi szteroidok és metabolitjaik helyi hatásait az alveoláris hámban.
Az alveoláris folyadék clearance fenntartja a gáz (O2 és CO2) cseréjét az alveoláris epitheliumon. Számos olyan állapot és betegség, amely befolyásolja az alveoláris folyadék clearance-ét (pl. Cisztás fibrózis, tüdőödéma és akut tüdőkárosodás), szintén a különbségeket mutatja a férfiak és a nők között [2,125-130]. Például a férfiak nagyobb gyakorisággal és súlyossággal mutatják a koraszülöttek légúti distressz szindrómáját [131–133], és tanulmányok kimutatták, hogy az E2 és P4 kezelés csökkenti a csecsemők nemi egyenlőtlenségeit [134,135] .
A megfelelő folyadékszint fenntartása az alveoláris epitheliumban a Na + reabszorpció és a Cl-szekréció erőteljes szabályozását igényli, amely nélkül a pulmonalis kapillárisokon áteső hidrosztatikus nyomás perceken belül elárasztaná az alveoláris teret. Patkányokban az alveoláris folyadék clearance a nőstényekben meghaladja a hímekét, és érzékeny az amiloridra, amely a hám nátriumcsatornájának (ENaC) gátlója [136]. Számos tanulmány kimutatta, hogy az E2 növeli a Na + reabszorpciót az ENaC-n és a hozzá kapcsolódó nem szelektív kationcsatornákon (NSC) keresztül az alveoláris hámsejtekben, és hogy az E2 csökkenti a Cl-szekréciót a cisztás fibrózis transzmembrán receptorán (CFTR) keresztül [115,137–143], ami arra utal, hogy a nem a hormonok felelősek az alveoláris folyadék clearance-ben megfigyelt nemi különbségekért.
Az E2 fiziológiás koncentrációban + szelektív ENaC és az amilorid-érzékeny NSC percek alatt 0,7 nM E2-re reagálva növekedett, és ezt a hatást G-1, egy G-fehérjéhez kapcsolt ER antagonista gátolta [139]. Más vizsgálatok kimutatták, hogy az E2 (1–3 nM) a CFTR és más Cl-szekréciós csatornák gátlásával csökkentette az alveoláris felszíni térfogatot az emberi felnőtt légúti epitheliális monorétegekben, és még nagyobb hatást fejtett ki CF-betegek sejtjeiben [137, 140]. Ezeknek az eredményeknek megfelelően a CF-ben szenvedő nőstények a tüdőfunkció változását mutatják a menstruációs ciklus alatt [144] .
A szexuális szteroid hatások vizsgálata más betegségekben, például emphysemában, korlátozott. Néhány állatkísérlet azt sugallta, hogy a progeszteron vagy a medroxi-progeszteron beadása képes visszafordítani a tüdő légterében az emfizematikus változásokat [145, 146]. Más vizsgálatok szintén a progeszteron hasonló pozitív hatásáról számoltak be a papain által kiváltott emfizémára [147,148]. Az emfizémában szenvedő betegek progeszteron beadása szintén javította a tüneteket és csökkentette a hypercapniát [149]. Érdekes módon az e hatások hátterében álló mechanizmusokat nem sikerült megállapítani, ezért nem ismert, hogy ezek a hatások tulajdoníthatók-e önmagában az alveoláris epitheliumban található nemi szteroid jelzésnek.
Középfülgyulladás
Terápiás szempontok
Kezelési célok: az ET átjárhatóságának és vízelvezetésének biztosítása az okozó tényezők azonosításával és kezelésével; támogassa az immunrendszert (Tankönyv, „Immun támogatás”). Palackozás: a visszatérő fülfertőzés a korai palacktápláláshoz kapcsolódik. A szoptatás (minimum 3-4 hónap) védő, valószínűleg a tehéntej allergia és az emberi tej fertőzés elleni védő hatása miatt. A palacktáplálás, miközben a gyermek a hátán fekszik (palacktartás), a palack tartalmának visszaforgatásához vezet a középfülbe. Az emberi tej magas antitesttartalma miatt védő, gátolja a mikrobákat. A szoptatott csecsemők csecsemőmirigyei 20-szor nagyobbak, mint a tápszerrel táplált csecsemők.
Ételallergia: az allergia, mint a krónikus OM fő oka, szerepét a kutatási szakirodalom szilárdan megalapozta. A középső és a belső fül immunológiailag reagál, beleértve az étel túlérzékenységre való reagálást is. Az OM-ben szenvedő gyermekek 85% -tól 93% -áig allergiás: 16% csak inhaláló szerekre, 14% csak ételre, 70% mindkettőre. A hosszan tartó szoptatás megakadályozhatja az OM-t az ételallergének elkerülésével, különösen, ha az anya terhesség és szoptatás alatt kerüli az érzékenyítő ételeket (azokat, amelyekre allergiás). Értékes az olyan ételek kizárása vagy korlátozása is, amelyekre a gyermekek általában allergiásak (búza, tojás, szárnyasok, tejtermékek), különösen az első 9 hónapban. A gyermek emésztőrendszere átjárja az antigéneket, különösen az első 3 hónapban. Ellenőrizze az étkezési szokásokat (bármely étel ritka megismétlése, kerülje a gyakori allergén ételeket, és kontrollált módon vezessen be ételeket - egyenként, egyenként figyelve a reakciókat).
Allergiás reakció: az ET blokkolását okozza - az ET nyálkahártya gyulladásos ödémája és az orrödéma Toynbee-jelenséget okoz (lenyelés csukott szájjal és orrral egyaránt, levegőt és váladékot kényszerítve a középfülbe).
Krónikus OM: mindig vegye figyelembe az allergiát. A tesztelt gyermekek 93,3% -a allergiás volt az élelmiszerekre, az inhaláló szerekre vagy mindkettőre. Az OM-ben szenvedő gyermekek 92 százaléka javul, ha sorozatos hígítási titráló terápiával kezelik az inhalánsokat és az eliminációs étrendet az ételallergének esetében. Statisztikailag szignifikáns összefüggés van az ételallergia és a visszatérő OM között a betegek 78% -ában. Az eliminációs étrend a betegek 86% -ában enyhíti a krónikus OM-t. Kihívásos étrend gyanúsan sértő ételek (ek) miatt a betegek 94% -ában a szerosus OM megismétlődését idézi elő.
A leggyakoribb ételallergének (gyakorisági sorrendben): tehéntej, búza, tojásfehérje, földimogyoró, szója, kukorica, paradicsom, csirke, alma.
Reflux: kapcsolat lehet a gyomor-nyelőcső reflux betegség között csecsemőknél és kisgyermekeknél OM-vel. Az OM-ból eredő betegségterhelés és a halláskárosodás csökken a savgátló gyógyszerekkel. Dózis: 15 mg lanzoprazol adag reggel és az életkortól függően ranitidin (4 mg/kg naponta) vagy nizatidin (5 mg/kg naponta) lefekvés előtt. A Pediatric Reflux Finding Score, amely a szoptoptikus laryngoscopiával értékeli az extraesophagealis refluxot, javulást mutatott. Magas volt a lemorzsolódás aránya, talán mellékhatások miatt. Naturopátiás szempontból az emésztési funkció szerepe fontos az OM és általában az egészség szempontjából. A korábban említett gyógyszerek nem ajánlottak, mert károsítják az emésztési funkciókat és növelik az ételallergiák, valamint az egészségtelen bélflóra kockázatát. Használjon ételallergén-kerülést, az egészséges ételekre való összpontosítást és az emésztőrendszer egészségét támogató intézkedéseket.
Csecsemőmirigy-kivonat: a thymus kiválasztja a fehérvérsejtekre ható hormonokat a megfelelő fejlődés és működés biztosítása érdekében. A gyermekeknek szánt borjú csecsemőmirigy-kivonatok javítják az immunrendszert, csökkentik az ételallergiát és javítják a krónikus légúti fertőzésekkel szembeni ellenállást. Különösen előnyösek lehetnek krónikus OM esetén (tankönyv, „Élelmiszer-allergiás tesztek”).
Naturopátiás gyógynövényes fülcseppek: Az otalgia (fülfájás) a javulás időszakában is fennmaradhat, és motiválja az aggódó szülőket felesleges antibiotikumok igénylésére. A naturopátiás botanikus fülcseppek ugyanolyan hatékonyak, mint az antibiotikum vagy az érzéstelenítő cseppek, sokkal kevésbé mérgezőek. Gyógynövényes fülcsepp kombináció: Calendula officinalis virágok (körömvirág, 28%), Hypericum perforatum teljes gyógynövény (orbáncfű, 30%) és Verbascum thapsus virágok (mullein, 25%) olívaolajban illóolajokkal, Allium sativum (fokhagyma) 0,05% olívaolajban (10%), Lavandula officinalis (levendula, 5%) és tokoferol-acetát olajban (E-vitamin, 2%). Dózis: 5 csepp t.i.d.
Echinacea: hatékony a felső légúti fertőzés esetén és stimulálja a citokin kaszkád összetevőit. Monoterápiaként az Echinacea hatékonysága nem világos. Tekintettel az Echinacea előnyeinek hosszú múltjára, hasznos lehet más természetes kezelésekkel kombinálva.
Xilit: antikariogén tulajdonságú, általánosan használt édesítőszer. Ez egy nyírból és más keményfából származó cukoralkohol. Gátolja a S. pneumoniae-t. A xilit 40% -kal csökkenti az akut OM előfordulását. Xylitol (8,4 g/nap) rágógumiként vagy pasztillaként adható, hogy csökkentse az OM előfordulását a napközi központokban és iskolákban. A xilit adagolásának naponta négyszer vagy ötször kell lennie, ami csökkentheti a megfelelőséget és az általános hatékonyságot. A mellékhatás a hasmenés.
Sinupret: Németországból származó gyógynövénykeverék, amely sóska (légi) (Rumex acetosa), 36 mg; Európai bodza (virág) (Sambucus nigra), 36 mg; tehénlepke (virág csészével) (Primula veris), 36 mg; Európai vervain (légi) (Verbena officinalis), 36 mg; és gentian (gyökér) (Gentiana lutea), 12 mg. A Sinupret antibiotikumokkal működik, és hatékonyabb antibiotikus tulajdonságokkal bírhat, mint az amoxicillin az OM esetében. Csökkentheti a szövődmények gyakoriságát is. A Sinupret ésszerű választás lehet a már antibiotikummal kezelt gyermekek számára.
A-vitamin: segít megelőzni az oxidatív szövetkárosodást, támogatja az immunműködést és fenntartja a nyálkahártya integritását. Bár gyermekeknél nem vizsgálták, állatokban az A-vitaminnal végzett előkezelés a S. pneumoniae beoltása előtt védelmet nyújtott az antioxidáns enzimaktivitás növelésével, valamint a malondialdehid és a nitrogén-oxid képződésének csökkentésével.
Párásítók: az OM és a gyermekek felső légúti fertőzésének népszerű kezelési módjai. Lényegesen több effúziót (folyadék ET-ben) figyelnek meg az alacsony páratartalmú környezetben tartott laboratóriumi állatok, mint a mérsékeltebb környezetben tartott állatok. Az alacsony páratartalom orrduzzanatot okozhat és csökkentheti az ET szellőzését, vagy kiszáríthatja az ET bélést, ami képtelen a folyadék tisztítására és fokozott szekrécióra. Az ET nyálkahártya hízósejtjei felszabadíthatják a hisztamint és ödémát okozhatnak. A páratartalom növelése párásítóval fontos mód lehet az OM effúzióval történő kezelésére.
Osteopátiás manipuláció: csökkentheti a visszatérő OM gyakoriságát gyermekeknél. Az oszteopátia elismeri a rendellenes szerkezeti dinamikát, amely hozzájárulhat a funkció megváltozásához. Ezeket a dinamikákat koponyaűri manipulációval lehet modulálni. Strukturális diszfunkciójú fiatal betegeknél ez más terápiákkal együtt előnyös lehet.
- RNS Binding Protein FUS - áttekintés a ScienceDirect témákról
- Parietális sejt antitest - áttekintés a ScienceDirect témákról
- Protein Sparing - áttekintés a ScienceDirect témákról
- Fehérje intolerancia - áttekintés a ScienceDirect témákról
- Formák (gombák) - áttekintés a ScienceDirect témákról