Az extrinsic allergiás alveolitis (túlérzékenységi pneumonitis) diagnózisának reflektorfénye
Absztrakt
Ismételt inhalációs expozíció antigén anyagoknak különböző forrásokból, főleg penészgombákból, termofil Actinomycetes, a madarak, illetve az extrém allergiás alveolitis (EAA) vagy a túlérzékenységi pneumonitis klinikai képével indukálhatnak immunválaszt. Az évek vagy akár évtizedek késése a diagnózis felállításáig nem ritka; a gyakori téves diagnózisok közé tartozik az allergiás asztma, a COPD, a visszatérő füstgáz és más fertőzések. Itt megadjuk a legkorszerűbb referenciákat, az eset részletes leírását, és ajánlunk egy aktuális diagnosztikai sémát.
Az extrinsic allergiás alveolitis (EAA) vagy a túlérzékenységi pneumonitis egy immunológiailag közvetített betegség, amelyet különféle forrásokból származó penészes széna, penészes fakéreg, baktériumokkal szennyezett fémmegmunkáló folyadék vagy párásító víz eredő antigén szerves anyagok ismételt belélegzésének érzékenysége okoz (ábrák) 1, 2, 3 és 4), a madárvirágzás fehérjéi, de vegyi anyagok, például izocianátok is okozhatják ezt a rendellenességet [1-8] (1. táblázat). Az EAA túlnyomórészt foglalkozási betegség, a leggyakoribb termofil antigénekkel Actinomycetes fajok, különféle penészgombák és madárfehérjék. Az extrinsic allergiás alveolitis előfordulása az éghajlattól, a földrajzi viszonyoktól, a foglalkozási és ipari tényezőktől függően változik, és többnyire 0,1-3 [9-11] százalék közötti tartományban van, a gazda tüdeje vagy a madárkedvelő tüdeje az uralkodó a legtöbb esetben régiók. Az érzékeny alanyoknál akut, szubakut (szakaszos) és krónikus progresszív lefolyás alakulhat ki, a szenzibilizáció mértékétől, az expozíció intenzitásától és időtartamától függően.
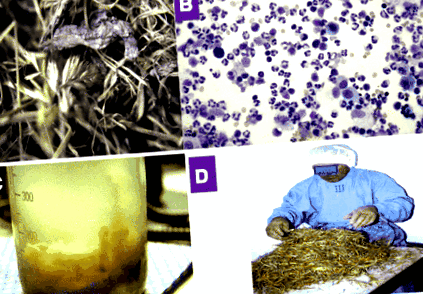
Extrinsic allergiás alveolitist okozó szerek, specifikus inhalációs teszt és bronchoalveoláris mosósejtek. A. A penészes széna okozza a gazda tüdőbetegségét az 1D. És a 4. ábrán bemutatott alanyban B. Bronchoalveoláris átfolyás kiterjedt neutrofíliával hat órával a fertőzés után jelentkezik egy galambtenyésztő tüdőben szenvedő alanyban. C. Nyomda párásító vízének vize és üledéke (a 3. ábrán látható tárgy). A mikroszkópos vizsgálatok számos baktériumot és penészgombát mutattak ki ebben a mintában. D. Foglalkozási típus specifikus inhalációs teszt penészes szénával (1A. Ábra).
Akut extrinsic allergiás alveolitis a penészes széna indikatív behatását követően. Az ábra a páciens 1. esetként leírt klinikai diagnosztikai eredményeinek összefoglalását mutatja. Klinikai bizonyítékok: Néhány órával a fertőzés után láz, rossz közérzet, köhögés, korlátozó szellőztetési mintázattal társulva, és károsodott a gázcsere. Az adatok a tüdőfunkciót és más klinikai eredményeket mutatnak a kiváltás utáni idősávban [h]: f: Vital kapacitás VC [L], e: Pa, O2 artériás oxigénnyomás [mmHg], d. Diffúziós kapacitás/átviteli együttható szén-monoxid (TL, CO) faktorhoz [ml/perc * kPa], c: Fajlagos légúti ellenállás (sRaw) teljes test pletizmográfiával mérve [kPa * s]; A további paraméterek a következők: b: Hőmérsékletprofil gradáció [° C], a. A vér leukocitáinak száma * 1000/mm 3].
Mellkas röntgenfelvétel egy nyomdában, szubakut párásító tüdőbetegségben szenvedő 33 éves dolgozótól. A részleteket lásd a szövegben. Foltos infiltrátumok vannak túlnyomórészt az alsó és a középső tüdőmezőkben.
Specifikus IgG antitestek jelenléte 23 izocianát alveolitisben szenvedő alany vérszérumában. Megjegyezzük, hogy öt kivételével mindegyiknél jelentős az ilyen antitestek szintje. A humán szérumalbuminhoz (HSA) kötött diizocianát-toluilén-dizocianátot (TDI), metilén-difenil-diizocianátot (MDI) és hexametilén-diizocianátot (HDI) használtuk az immunabszorpciós vizsgálathoz (CAP immunoanalízis) a leírás szerint. Módszertani részletekért lásd Baur [4], Budnik et al. [18]. Specifikus IgG antitestek a vér szérumában olyan betegtől, aki párásító tüdőben szenved, szennyezett párásító víznek való kitettség miatt (1C. Ábra). Az ELISA-teszt anti-IgG antitestekkel látható, amelyek felismerik a dózis-specifikus reakciókat a munkahelyi párásító víz antigének különböző koncentrációira. A negatív és pozitív kontrollok laboratóriumi pozitív és negatív mintákat mutatnak olyan betegekből, akiknek erős a szignálja (pozitív reakció), és egészséges alanyokból származó szérumot, nedvesítő aeroszollal való érintkezés nélkül (negatív kontroll, nem specifikus kötődés).
Az EAA szenzibilizált egyéneknél a tüdő parenchima és a légutak diffúz gyulladásával társul, ideértve a nem köpenyes intersticiális granulomákat és a peribronchiális mononukleáris sejtek infiltrációját óriássejtekkel. Bár a legtöbb érintett alanyban általában magas a keringő immunglobulin G antitest koncentrációja, amely specifikus az okozó antigén (ek) re, a diagnózis nehéz lehet, mivel a tünetek gyakran nem specifikusak, jellemzően több órás késési periódusúak vagy alkotmányosnak tűnhetnek rossz közérzet és fogyás; gyakran fokozatosan progresszívek az évek során, végül tartós légzési nehézségekkel, függetlenül a kiváltó expozíciótól (1., 2., 3. és 4. ábra). Az évek vagy akár évtizedek késése a diagnózis felállításáig nem ritka, a téves diagnózisok közé tartozik az allergiás asztma, a COPD, a visszatérő füstgáz és egyéb fertőzések. A következő diagnosztikai sémát javasoljuk a betegség mintázatához.
Diagnosztika (2. táblázat) [4,12]
Kórtörténet: A felbujtó szerrel való súlyos expozíció után 4-8 órával a betegeknél láz, hidegrázás, rossz közérzet, köhögés, nehézlégzés, fejfájás (akut lefolyás) alakul ki. Bizonyos esetekben nem alakulnak ki akut tünetek, inkább alattomosan jelentkeznek ezek a tünetek. Különösen alacsonyabb expozíció esetén a betegek fokozatosan produktív krónikus köhögést, nehézlégzést okoznak, fáradtságot, étvágytalanságot, súlycsökkenést (szubakut vagy időszakos lefolyás) (2. táblázat). Ezek a megállapítások olyan betegeknél is jelen lehetnek, akik ismételt akut rohamokat tapasztalnak.
Fizikális vizsgálat: Az akut roham során láz, tachypnea és diffúz finom bibasilaris end-belégző repedések hallatszanak. További gyakori megállapítások az izomsorvadás, a súlycsökkenés, krónikusan kifejezett formában az edzés, a tachypnea, a légzési zavarok is.
Tüdőfunkció teszt: Az előrehaladott krónikus lefolyás tipikus jellemzői a korlátozó ventilációs mintázat (azaz csökkent a teljes tüdőkapacitás, az életfontosságú kapacitás és a tüdőmegfelelőség) és a káros gázcsereparaméterek (csökkent diffúz kapacitás, hipoxémia edzés közben vagy akár nyugalmi állapotban). Vegyes obstruktív és korlátozó szellőztetési minta is kialakulhat.
IgG antitestek és egyéb laboratóriumi eredmények: A kauzális antigénekre specifikus IgG antitestek magas szérumkoncentrációi a c. Az érintett betegek 70% -a (2. ábra). A diagnosztikai szempontból problémásabb, hogy az uralkodó kitett egészséges egyének több mint 50% -a mutathat ilyen antitesteket, az okozó antigén (ek) és az alkalmazott laboratóriumi vizsgálat érzékenységétől és specifitásától függően. Eddig a legtöbb ok-okozati antigén esetében nem állnak rendelkezésre validált laboratóriumi vizsgálatok a piacon. Az immunokomplex által közvetített folyamat mellett a sejtek által közvetített immunitás nyilvánvalóan fontos patofiziológiai szerepet játszik. Ennek a sejtválasznak a megjelenítésére azonban még nem áll rendelkezésre rutin diagnosztikai teszt. Az akut és szubakut tanfolyamok során fellépő egyéb rendellenes laboratóriumi eredmények között szerepel a leukocytosis, a neutrophilia, a megnövekedett eritrocita ülepedési sebesség, valamint a megnövekedett mennyiségi immunglobulinok és a C-reaktív fehérje szintje.
Radiológiai leletek: A tipikus képek a centrilobuláris mikronoduláris (HRCT), foltos vagy retikuláris opacitások, amelyek leginkább az alsó tüdőzónákban jelennek meg (3. ábra). Az akut rohamok során az alsó és a középső tüdőzónában az alap-opacitás és az interstitialis tüdőgyulladás-szerű mintázat jelen lehet. A krónikus lefolyás végső szakaszát fibrózis jellemzi, sőt a méhsejtek is túlsúlyban vannak a tüdő alsó részeiben. Emphysema is előfordulhat [13].
Soros tüdőfunkciós vizsgálat antigén-expozíciós időszakokban és szabadnapokon (a SIC-ben ismertetett változásokat mutatva, valamint a tünetek helyreállítása és a károsodott tüdőfunkció a szabadnapokon).
Specifikus inhalációs provokációs teszt (SIC): Ez egy fáradságos és időigényes diagnosztikai vizsgálat a feltételezett kórokozó alkalmazásával. Csak jól tapasztalt orvosok végezhetik. Ha helyesen történik, akkor ez egy nagyon érzékeny és specifikus diagnosztikai módszer. Lásd a 2. táblázatot és az ábrák példáját. Az 1. ábrán a módszertani módszereket másutt publikálták [14,15], az SIC-vel foglalkozó európai munkacsoport kiegészítő anyaga online asztma-kiegészítő kézikönyvet tett közzé a speciális inhalációs kihívásvizsgálatokra vonatkozó kezelési kézikönyvben. /2014/03/07/09031936.00180313.DC1/Final_Handbook.pdf
Bronchoalveoláris mosás: A bronchoalveoláris átmosás leukocitózist (neutrophilia) mutat az alveolusokban és a kis légutakban az akut lefolyásban, majd mononukleáris sejtek beáramlása következik (1D ábra). Szubakut és krónikus lefolyásokban limfocitózis megnövekedett CD8 + sejtekkel és 9 CD4 +/CD8 + aránnyal.
Tüdő szövettana: Az invazív diagnosztikára, azaz a tüdőbiopsziára általában nincs szükség. Akut lefolyásban a leukocita gyulladás dominál. A szubakut és krónikus lefolyásokra a limfocita-domináns intersticiális gyulladásos sejtek beszivárgása, a jól formált interstitialis epitheliod sejtek óriássejtekkel nemrotrotizáló granulómái jellemzőek. Celluláris bronchiolitis és bronchiolitis obliterans és intra-alveoláris fibrózis gócai is előfordulhatnak. A krónikus lefolyás tartalmaz egy interstitialis (szervező) tüdőgyulladás-szerű mintát sub pleurális patchy fibrózissal, fibroblasztikus gócokat centrilobularis fibrózissal, végül alveoláris destrukciót (méhsejt) [16,17].
Integrált diagnosztikai megközelítés: Az 1–5. Lépés felett az alapvető rutindiagnosztika található. Ha mindegyikük egybehangzó pozitív eredményt mutat, az extrin allergiás alveolitis diagnózisa kellően valószínű. Ha a megfelelő 6 paraméter közül egy vagy több negatív vagy egyértelmű, akkor legalább egy további diagnosztikai eljárásra van szükség, azaz soros tüdőfunkciós vizsgálatra antigén-expozíciós időszakokban és szabadnapokon (kombinálva a klinikai tünetek követésével) vagy specifikus inhalációs kihívással teszt, bronchoalveoláris mosás vagy tüdőbiopszia (3. táblázat).
Esetpéldák
1. eset (a gazdák tüdeje)
Kórtörténet: Az 53 éves gazda öt éven át köhögéstől, fokozódó légszomjatól szenvedett az erőfeszítések során, hidegrázástól és láztól késő este és éjszaka a téli hónapokban. 40 tehenét mindig eteti, amely gyakran penészes volt.
Fizikális vizsgálat: Belégzési ropogás a bazális tüdőmezőkön.
Tüdőfunkciós teszt: Korlátozó szellőztetési mintázat (azaz csökkent a teljes tüdő kapacitás, a vitális kapacitás és a tüdő megfelelősége) és a károsodott gázcsere paraméterek.
IgG antitestek: Az IgG antitestek magas szérumkoncentrációja aspergillus fajok és.
Specifikus inhalációs provokációs teszt (1D. Ábra) ennek a gazdák tüdejétől szenvedő betegének penészes szénájának szondájával (1A. Ábra); az eredményt lásd a 4. ábrán.
Radiológiai leletek: Foltos homályosságok mind az alsó, mind a középső tüdőmezőkön.
Bronchoalveoláris mosás: A bronchoalveoláris átöblítés leukocitózist (neutrophilia) mutatott ki az alveolusokban és a kis légutakban az akut fázisban, majd mononukleáris sejtek beáramlása következett be.
2. eset (párásító tüdő)
Az 1C. Ábra egy nyomda nedvesítő vizét mutatja, ahol több erősen mikrobiálisan szennyezett párásítót telepítettek, és 33 éves betegünket alkalmazták. A mellkas röntgen megállapításait lásd a 3. ábrán.
Kórtörténet: Több mint 6 éve panaszkodott influenzaszerű tünetekre és krónikus produktív köhögésre, szezonális eltérések és növekvő légszomj nélkül.
IgG antitestek: A szérum IgG antitest elemzés (2B. Ábra) rendkívül magas koncentrációkat mutatott az 1C. Ábrán bemutatott szonda kivonatában, és alacsonyabb koncentrációkat különféle penész és baktériumok esetén.
Specifikus inhalációs provokációs teszt: Ezt a párásító vízszondával, amelyet 4 órás látencia után állítottak elő, növekvő köhögés, nehézlégzés, láz, az életképesség jelentős csökkenése és az artériás oxigén parciális nyomása 3 órán keresztül.
Megelőzés és kezelés
A legjobb eredményt a korai felismerés és a további kitettségek következetes megelőzése nyújtja. A kórokozó (k) elkerülése az egyetlen hatékony intézkedés a visszaesések, a tipikusan progresszív rendellenesség és a tartósan károsodott tüdőfunkció megelőzésére. Kortikoszteroidokra lehet szükség súlyos akut lefolyású esetekben (kezdve 0,5-1 mg prednizonnal/kg). A kevésbé súlyos akut kúrák kezelés nélkül enyhülnek.
Hivatkozások
Blatman KH, Grammer LC. 19. fejezet: Túlérzékenységi tüdőgyulladás. Allergia Asztma Proc. 2012; 33 1. kiegészítés: S64–6.
Lacasse Y, Girard M, Cormier Y. A túlérzékenységi pneumonitis legújabb fejleményei. Mellkas. 2012; 142: 208–17.
Selman M, Pardo A, King Jr TE. Túlérzékenységi pneumonitis: betekintés a diagnózisba és a patobiológiába. Am J Respir Crit Care Med. 2012; 186: 314–24.
Baur X. Izocianátok által kiváltott túlérzékenységi pneumonitis (extrinsic allergiás alveolitis). J Allergy Clin Immunol. 1995; 95: 1004–10.
Robertson W, Robertson AS, Burge CB, Moore VC, Jaakkola MS, Dawkins PA és mtsai. Alveolitis és asztma kitörésének klinikai vizsgálata egy autómotorgyárban. Mellkas. 2007; 62: 981–90.
Weiss W, Baur X. Porított gyöngy-kagylóhéj antigénjei túlérzékenységi tüdőgyulladást okoznak. Mellkas. 1987; 91: 146–8.
Baur X, Behr J, Dewair M, Ehret W, Fruhmann G, Vogelmeier C és mtsai. Párásító tüdő és párásító láz. Tüdő. 1988; 166: 113–24.
Fox J, Anderson H, Moen T, Gruetzmacher G, Hanrahan L, Fink J. Fémmegmunkáló folyadékkal összefüggő túlérzékenységi pneumonitis: járványvizsgálat és esetkontroll-tanulmány. Am J Ind Med. 1999; 35: 58–67.
Lacasse Y, Cormier Y. Túlérzékenységi pneumonitis. Orphanet J Ritka Dis. 2006; 1: 25.
C rózsa, Jr. Király TE. Viták túlérzékenységi tüdőgyulladásban. Am Rev Respir Dis. 1992; 145: 1–2.
Dalphin JC, Debieuvre D, Pernet D, Maheu MF, Polio JC, Toson B és mtsai. A krónikus hörghurut és a farmer tüdejének elterjedtsége és kockázati tényezői a francia tejtermelőknél. Br J Ind Med. 1993; 50: 941–4.
Lacasse Y, Selman M, Costabel U, Dalphin JC, Ando M, Morell F és mtsai. A túlérzékenységi pneumonitis klinikai diagnózisa. Am J Respir Crit Care Med. 2003; 168: 952–8.
Hanak V, Golbin JM, Hartman TE, Ryu JH. A parenchymás fibrózis nagy felbontású CT-megállapításai korrelálnak a túlérzékenységi pneumonitis prognózisával. Mellkas. 2008; 134: 133–8.
Munoz X, Sanchez-Ortiz M, Torres F, Villar A, Morell F, Cruz MJ. Specifikus inhalációs kihívás diagnosztikai hozama túlérzékenységi pneumonitis esetén. Eur Respir J. 2014; 44: 1658–65.
Vandenplas O, Suojalehto H, Aasen TB, Baur X, Burge PS, De Blay F és mtsai. Specifikus inhalációs kihívás a foglalkozási asztma diagnózisában: konszenzusos nyilatkozat. Eur Respir J. 2014; 43: 1573–87.
Lima MS, Coletta EN, Ferreira RG, Jasinowodolinski D, Arakaki JS, Rodrigues SC és mtsai. Szubakut és krónikus túlérzékenységi tüdőgyulladás: hisztopatológiai minták és túlélés. Respir Med. 2009; 103: 508–15.
Takemura T, Akashi T, Ohtani Y, Inase N, Yoshizawa Y. A túlérzékenységi pneumonitis patológiája. Curr Opin Pulm Med. 2008; 14: 440–54.
Budnik LT, Preisser AM, Permentier H, Baur X. Lehetséges-e specifikus IgE antitest elemzés a metiléndifenil-diizocianát által kiváltott foglalkozási asztma diagnosztizálására? Int Arch Occup Environ Health. 2013; 86: 417–30.
Közzététel
XB tanúbizonyságot tett a foglalkozási megbetegedésekkel kapcsolatos perekben az itt leírt felperesek nevében, és független szakértői véleményt adott a szociális bíróságokhoz vagy a törvényes biztosításokhoz.
Szerzői információk
Hovatartozások
Munkaegészségügyi Intézet, Charité Egyetem Orvostudomány, Berlin, Berlin, Németország
Xaver Baur és Axel Fischer
Foglalkozási toxikológiai és immunológiai osztály, Munkaügyi és Tengeri Orvostudományi Intézet (ZfAM), Hamburg-Eppendorf Egyetemi Orvosi Központ. Hamburgi Egyetem, Hamburg, Németország
Európai Környezetvédelmi és Munkaorvosi Társaság, EOM, Berlin, Németország
Xaver Baur, Axel Fischer és Lygia T Budnik
A PubMed Google Scholar alkalmazásban is kereshet erre a szerzőre
A PubMed Google Scholar alkalmazásban is kereshet erre a szerzőre
A PubMed Google Scholar alkalmazásban is kereshet erre a szerzőre
Levelezési cím
További információ
Versenyző érdekek
A szerzők kijelentik, hogy nincsenek versengő érdekeik, akár egy termékkel foglalkozó céggel, akár egy lobbicsoporttal.
A szerzők hozzájárulása
XB, LTB, AF elvégezte az irodalom áttekintését, XB megvizsgálta a betegeket és átadta az esetek klinikai adatait; Az LTB felügyelte a laboratóriumi elemzéseket; XB, LTB elkészítette a kéziratot; XB, AF, LTB szerkesztette és átdolgozta a kéziratot. Minden szerző elolvasta és jóváhagyta a végleges kéziratot.
- A rovarcsípés allergiás reakciójának jelei - Oak Brook allergiások
- Prenatális Omega-3 zsírsavak áttekintése és ajánlások - Jordánia - 2010 - Journal of Midwifery;
- Aláír téged; újra allergiás reakció és mikor kell orvoshoz fordulni - bennfentes
- A petefészek fájdalma 5 A petefészek fájdalmának okai, diagnosztizálása, kezelése
- A kedvtelésből tartott patkányok allergiás reakcióinak leküzdése A kedvtelésből tartott patkányokról