Sugárzási proctitis: A menedzsment jelenlegi stratégiái
1 vastagbél- és végbélsebészeti osztály, Beth Israel Deaconess Medical Center, Harvard Medical School Boston, 330 Brookline Avenue, Stoneman 9, Boston, MA 02215, USA
Absztrakt
A sugárzási proctitis ismert szövődmény a kismedencei rosszindulatú daganatok sugárkezelését követően. Az esetek többségét nem sebészeti úton kezelik, és e betegek kezelésében elengedhetetlen a rendelkezésre álló módok megértése. Ebben a cikkben a sugárzási proktitis jelenlegi kezeléseire összpontosítunk.
1. Bemutatkozás
A sugárzás mind az apoptózist, mind a sejthalált másodlagos módon okozza a DNS, a fehérjék és a lipidek károsodásában, és általában a gyorsan szaporodó sejteket érinti, például a rákban találhatóakat [1]. Ma a medencébe történő sugárzás fontos alkotóelem a kismedencei rosszindulatú daganatok kezelésében, és neoadjuváns vagy adjuváns terápiaként alkalmazzák. Kezdetben úgy vélték, hogy a sugárterápia (RT) nem nyújt hasznot a betegek számára, különösen a rektális rákban szenvedő betegek számára, mivel ezek a rákok sugárzással szemben ellenállóak. Csak később fedezték fel, hogy nagyobb dózisokra van szükség az ellenállás leküzdéséhez. Nagyobb sugárzási dózisok azonban a sugárzás területén vagy annak környékén lévő szervek járulékos károsodását eredményezték. Jelenleg a sugárterápia leggyakoribb szövődménye, a nagyobb dózisok alkalmazása után a prosztatarák kezelése utáni proctitis [2].
A brachyterápiának kétféle módja van, amelyek megkísérlik elérni a célszövet lokalizált expozíciójának ugyanazt a célját. A leggyakoribb megközelítés miatt radioaktív pelletek (általában jód 125 vagy palládium 103) beültetése szükséges a célszövetbe, fokozatos felszabadulással az idő múlásával [6]. Egy alternatív módszer olyan üreges katéterek használatát foglalja magában, amelyeket az idő múlásával fokozatosan meg lehet tölteni növekvő mennyiségű radioaktív pellettel. A brachyterápia csökkenti a környező szövetek expozíciójának károsodását a beültetett pelletek gondos elhelyezése alapján [6]. A brachyterápiás kolorektális szövődmények aránya általában alacsonyabb, mint a külső sugárzás. Lesperance és munkatársai tanulmánya. csökkenést mutat mind a brachyterápiás akut (6% versus 43%), mind krónikus (2% versus 21%) szövődményeknél, összehasonlítva a külső sugárzással [7, 8].
A sugárzási proktitist általában akutnak vagy krónikusnak minősítik, általában a tünetek kezelési időkerete, valamint a tünetek és jelek alapján határozzák meg.
2. Akut proctitis
Az akut sugárzással járó proctitis olyan gyulladásos folyamat, amely csak a felszíni nyálkahártyát veszi részt [2], és amely szinte előfordul közvetlenül a kezelés megkezdése után vagy legfeljebb 3 hónappal a kezelés megkezdése után [16]. A hasmenés, az émelygés, a görcsök, a tenesmus, a sürgősség, a nyálkahártya kisülése és a kisebb vérzés a betegek 20% -ában is kialakulhat, ami miatt meg kell szakítani a kezelést [17]. Nagyjából a sugárzási proktitis a végbél nyálkahártyájának gyulladásos folyamata, amely ödémásnak, húsos vörösnek tűnik, és fekélye vagy nyálkahártyája lehet. Mikroszkóposan a mikrovillus architektúrájának elvesztése vagy torzulása tapasztalható hiperémiával, ödémával és fekélyesedéssel [2]. A gyulladásos végbélnyálkahártya kolonoszkópos biopsziája általában nem ajánlott a vérzés és a fistula kialakulásának fokozott kockázata miatt. Az akut sugárzási proktitis nem növeli a krónikus sugárzási proktitis kockázatát [2], és általában önkorlátozó a sugárterápia leállításával.
3. Krónikus proctitis
A krónikus sugárzási proktitis időkerete korán megkezdődhet, még a sugárzási proktitis akut fázisában is, de a tünetek csak hónapokkal vagy évekkel később válhatnak nyilvánvalóvá. abbahagyása terápia (medián 8–12 hónappal a terápia befejezése után) [2]. A krónikus proctitis tünetei közé tartozhat az akut sugárzásos proctitis, de súlyos vérzés, szűkület, perforáció, fistula és bélelzáródás is. A kóros folyamat eltér az akut fázistól, és végső soron magában foglalja a végbélfal vérellátásának kompromisszumát, amely teljes vastagságú iszkémiát és fibrotikus változásokat eredményez [2]. A belek súlyosan halványak, nem felelnek meg a telangiectasiáknak, és szűkületük, fekélyük, fistulájuk vagy erős vérzésük lehet [18]. Mikroszkóposan fokális torzulás és intim fibrózisú artériák és arteriolák pusztulása van [18]. A krónikus sugárzással járó proctitis jelentősen nagyobb hatást gyakorol a szövődmény által érintett egyének életminőségére, mint az akut proctitisben szenvedő betegeknél [2].
Míg a HIV kezelése és nyomon követése olyan mértékben javult, hogy ma már krónikus állapotnak tekinthető, számos HIV/AIDS-szel összefüggő rosszindulatú daganat nőtt. Ezen rosszindulatú daganatok egy része magában foglalja a méhnyakrákot, az anális rákot és a limfómákat, amelyek mindegyike sugárterápiát igényelhet, amely befolyásolhatja a végbelet. Számos jelentés számolt be arról, hogy az AIDS-es betegeknél magasabb a szövődmények aránya a sugárterápia után. Az etiológia nem világos, de felmerült, hogy a HIV-betegeknél tapasztalt szisztémás glutationhiány a radioprotektív tiolok kimerüléséhez és fokozott oxidatív sérüléshez vezet. Anális rákban szenvedő HIV-pozitív betegeknél, akiknek CD4-száma kevesebb, mint 200, Hoffman és mtsai. [22] fokozott toxicitásról (vérzés és mucositis) és csökkent toleranciáról számol be, ezáltal alacsonyabb kezelési dózisok szükségességére utal. Más vizsgálatok hasonló toxicitási profilt javasolnak [23], és nem javasolják a kezelés dózisának módosítását. Jelenleg nem állnak rendelkezésre meggyőző adatok a HIV/AIDS-ben és prosztatarákban szenvedő betegek sugárzási proktitiséről.
4. Diagnózis
Sugárzási proktitisz gyanúja merül fel minden olyan betegnél, aki medencei sugárterhelésnek volt kitéve és a fent említett tünetekkel jár. A többséget kolonoszkópia vagy sigmoidoszkópia után diagnosztizálják, olyan tulajdonságokkal, amelyek sápadtságot, törékenységet és telangiectasiakat mutatnak. Egyéb okokat általában ki kell zárni, például fertőzést vagy gyulladásos bélbetegséget. A fistulizáló betegség, beleértve a rectovaginalis, rectourethralis és rectovesicularis fistulákat, későn mutathatja ki a sugárzási proctitis tüneteit, de általában más tünetek előzik meg őket.
5. Megelőző intézkedések
Noha a sugárzási technikák és dózisok módosítását folyamatosan tanulmányozzák a sugárzási proktitis előfordulásának csökkentése érdekében, a megelőző módszereket vizsgáló kísérletek eddig csalódást okoztak. Kis, kettős-vak, randomizált kontroll vizsgálatok nem mutattak különbséget a krónikus sugárzási proctitis arányában vagy súlyosságában a végbél alkalmazásával (200 μg) misoprostol és orális (3 g b.i.d.) vagy rektális (napi 3 gm) szukralfát [24–27]. Az intravénásan beadott amifosztin (napi 340 mg/m2) kisméretű vizsgálatokban ígéretet tett az akut proctitis tüneteinek megelőzésére, valamint a krónikus proctitis tüneteinek súlyosságának csökkentésére. Az utánkövetési időszak azonban viszonylag rövid volt [28–30]. Összességében a megelőző intézkedések nem járultak hozzá jelentősen a sugárproktitis előfordulásának csökkentéséhez.
6. Kezelések
6.1. Akut Proctitis
Míg az akut proctitis önkorlátozó, a külső sugárzáson áteső betegek legfeljebb 20% -ának rövid megszakításokra van szüksége a tünetek javítása érdekében. A támogató orvosi kezelés általában az egyetlen szükséges kezelés, amely magában foglalja a hidratálást, a hasmenés elleni gyógyszereket és esetleg a szteroid- vagy 5-amino-szalicilát-beöntéseket. A terápia abbahagyása általában a végleges kezelés, és ritkán van szükség műtéti beavatkozásokra.
6.2. Krónikus Proctitis
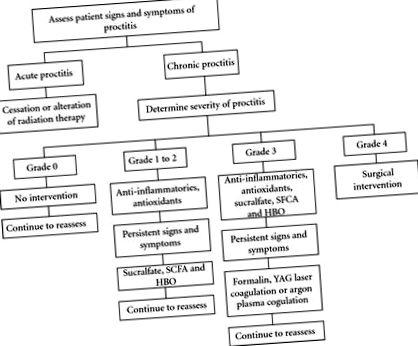
A krónikus proctitis kezelése felosztható neminvazív kezelésekre (gyulladáscsökkentők, szukralfát, rövid láncú zsírsavak, hiperbarikus, antioxidánsok) és invazív kezelésekre (abláció és műtét). Bár a krónikus proctitis kezelési stratégiáiban jelentős eltérések tapasztalhatók, általában van egy olyan stratégia, amely a legkevésbé invazív beavatkozásokat alkalmazza először fokozatosan, a tünetek és jelek súlyosbodásával (1. ábra).
6.3. Nem invazív kezelések
A krónikus sugárzási proktitis noninvazív terápiája orális, rektális vagy gáznemű szerek alkalmazásával kezdődik. Ezek a szerek nem szteroid gyulladáscsökkentőkből, szukralfátból, rövid láncú zsírsavakból (SCFA), hiperbarikus oxigénből (HBO) és antioxidánsokból állnak.
6.3.1. Gyulladáscsökkentő szerek
Az OXO-K993 hatóanyagot tartalmazó, intravénásan beadott újabb kloritalapú gyulladáscsökkentő szert, a WF10-et nemrégiben tanulmányozták sugárzás okozta proctitis kezelésére. Kezdetben az AIDS kiegészítő terápiájaként fejlesztették ki, és antiretrovirális és opportunista fertőzés-profilaxisokkal kombinálva alkalmazták [2]. Hatásmechanizmusa feltehetően a sejtek által közvetített immunrendszer modulációján keresztül valósul meg, a fagocitózis stimulálásával és az antigén megjelenésének csökkentésével az immunaktiváció csökkentése érdekében [38]. Csak Európában használták sugárzás okozta hólyaghurut, proktitis és mucositis kezelésére. Az előzetes tanulmányok azt mutatják, hogy a vérzéses tünetek kontrollja évekig (a medián követési idő 55 hónap) két adag (napi 0,5 ml/testtömeg-kg) után történt; a hatékony eredmények fenntartása évente 1-2 alkalommal végzett ismételt kezeléssel történt [38]. Ezt a gyulladáscsökkentőt az FDA nem hagyta jóvá az Egyesült Államokban történő alkalmazásra.
6.3.2. Szukralfát
A gyulladáscsökkentő szerekkel, például 5-ASA-val öt hónapnál hosszabb kezelés után fennálló tünetek szukralfáttal vagy pentozán-poliszulfáttal (PPS) történő kezelést tesznek szükségessé. A szukralfát egy erősen szulfatált polianionos diszacharid (szulfatált szacharóz és alumínium-hidroxid komplex) [39], amelyről azt gondolják, hogy serkenti a hám gyógyulását és egy védő gát kialakulását [40]. Néhány jelentés, köztük egy randomizált, placebo-kontrollos vizsgálat, mind a klinikai, mind a nyálkahártya kimenetelének előnyeit mutatta a rektális szukralfáttal (2 g naponta) [15]. A rektális szukralfát (3 gm) a sugárzási proctitis kezelésében is jobbnak bizonyult a gyulladáscsökkentő kezeléseknél [41], és a betegek 75% -ánál tünetek enyhülését eredményezheti [21]. Úgy gondolják, hogy a pentozán-poliszulfát (PPS, a glikozaminoglikán szintetikus származéka, amely a hólyag, az erek és a gyomor-bél traktus bélésében van) csökkenti a hámpermeabilitást és megakadályozza a szukralfáthoz hasonló tapadást [42].
6.3.3. SCFA
A rövid láncú zsírsavak (SCFA) a vastagbél nyálkahártyájának fő oxidatív tüzelőanyagai, és a vastagbél nyálkahártya proliferációjának serkentését is szolgálják [43]. Úgy gondolják, hogy a vastagbél anaerob baktériumai nem felszívódó szénhidrátokból állítják elő őket. Az SCFA legjelentősebb terméke a vajsav [44]. Az SCFA értágító hatást fejt ki az arteriole falaira is a véráramlás javítása érdekében [45]. A sugárzás okozta sérülés iszkémiát és a mikrovillus architektúra elvesztését eredményezi, ami az SCFA felszívódásának károsodását eredményezheti, hozzájárulva ezáltal a krónikus sugárzási proctitisnél észlelt változásokhoz [3]. Az SFCA beöntéssel történő kiegészítés felgyorsíthatja a gyógyulást a vastagbélsejtek által tapasztalt hiány javításával. Két randomizált vizsgálat a butirát beöntéseket (40 mM butirát) vizsgálta, és a tünetek és a tünetek jelentéktelen javulását állapította meg, ellentétben az esetleges jelentésekkel, amelyek némi előnyre utalnak. Mindkét tanulmány azonban erősen alulteljesített [46–48]. További vizsgálatokra van szükség az SCFA krónikus proctitisben rejlő lehetséges előnyeinek értékeléséhez.
6.3.4. HBO
A hiperbarikus oxigénterápia (HBO) az ischaemia kóros folyamatából ered, amely magában foglalja a végbélfal véráramlásának kompromisszumát. Az HBO előnye elméletileg a szöveti hipoxia csökkenésével, esetleg angiogén és antibakteriális hatásával érhető el [49, 50]. Az HBO krónikus sugárzási proctitisben történő alkalmazására vonatkozó adatok korlátozottak. Bennett et al. Áttekintése. [51] megnövekedett esélyt jelent a javulásra a hiperbarikus oxigénkezeléssel (RR 1,75, a kezeléshez szükséges szám = 5). Az előnyök mértéke, a kumulatív hatások vagy a válasz időtartama azonban nem számszerűsíthető az adatok módszertana és minősége miatt. Clarke egy randomizált, kontrollált vizsgálatában összehasonlították azokat a betegeket, akiket 90 perc 100% -os oxigénnel kezeltek 2 atmoszférában, és azokat a betegeket, akiket 90 percig kezeltek 21% oxigénnel, körülbelül 1 atmoszférában. Az eredmények 30 tünetjavulás után némi előnyt jelentettek a tünetek javulásával [52]. A legtöbb tanulmány azt mutatja, hogy az HBO drága, és a legtöbb területen nem érhető el, kivéve a magasan specializált központokat, a többszörös kezelések és a speciális felszerelések követelménye miatt.
6.3.5. Antioxidánsok
Úgy gondolják, hogy az oxidatív stressz a krónikus sugárzási proktitis kialakulásának fő mechanizmusa; antioxidáns tulajdonságú szereket alkalmaztak a szövetkárosodás korlátozására a sugárkárosodás során. Kennedy és munkatársai tanulmányában, amelyben csak 10 beteg vett részt, az E- és C-vitamin használata jelentősen csökkentette a hasmenés és a sürgősség arányát [19]. Az A-vitamin előnyeit önmagában és más terápiákkal kombinálva vizsgálták. Ehrenpreis által végzett kettős-vak vizsgálatban az A-vitamin alkalmazása jelentősen csökkentette a proktitis tüneteit, és a hatás a crossover után a placebo csoportba tartozó betegekre is kiterjedt [53]. Patel beszámolt arról, hogy az A-vitamin hozzáadása a 8% -os formalinnal történő kezeléshez növelte a formalin sikerességi arányát és lerövidítette a javulás eléréséhez szükséges időt [54].
6.4. Invazív kezelések
6.4.1. Ablatív eljárások
Az ablatív technikák az orvosi kezelésre nem megfelelő tünetek kezelésére vannak fenntartva, és magukban foglalják a formalint, az endoszkópos koagulációt és az argonplasma koagulációt. Ezek a technikák társulhatnak olyan szövődményekkel, amelyek magukban foglalják a vérzést, a perforációt, a sipolyokat és a szűkületet.
6.4.2. Formalin
6.4.3. Endoszkópos koaguláció
Számos endoszkópos koagulációs eszköz hatékony a sugárzás okozta vérzés szabályozására a fokális vérzéses telangiectasias koagulációja révén. A jelenleg rendelkezésre álló vizsgálatok többsége retrospektív, és a tünetek javulását és a recidívák csökkenését mutatja YAG lézeres koagulációval vagy argon plazma koagulációval végzett kezelést követően [2]. Mindkét módszer a termikus koaguláció leadásán alapul, és jelentős hemorrhagiás proctitisben szenvedő betegek számára kell fenntartani [59]. Gyakran több kezelési alkalomra van szükség.
Az argon plazma koaguláció nagyfrekvenciás energiát (monopoláris diatermiát) használ fel a szövetbe egy ionizált gázon keresztül, érintkezés nélküli módon [59]. Bebizonyosodott, hogy képes szabályozni a vérzést a gyomor-bél traktusban, és nagyon korlátozott a szöveti behatolása, ami vonzóvá teszi a felszíni vérzés kezelését. A rendelkezésre álló tanulmányok retrospektívek, és kevés betegen vesznek részt [60, 61]. Azonban minden tanulmány magasabb hemoglobint és kevesebb tünetet mutatott vérzéses proktitisben szenvedő betegeknél, akiknek nem sikerült az orvosi terápia. Beszámoltak arról, hogy az egyszeri kezelések jelentősen javítják a tüneteket [62], de átlagosan két-három kezelésre van szükség az eredmény eléréséhez. A javulás a terápia befejezése után néhány hónapig fennmaradt [2, 63]. A jelentett szövődmények többsége enyhe volt, és görcsöket, nyálkahártya váladékot és szűkületet jelentett [2]. Jelentős szövődményekről, köztük nagy fekélyekről, perforációkról, valamint rectourethralis és rectovaginalis fistulákról számoltak be.
A YAG lézerek ugyanolyan elméleti haszonnal járnak, mint az argon plazma koaguláció, korlátozott behatolási mélységgel és a pontos alkalmazás lehetőségével. Alkalmazásuk bizonyítékai hasonlóak az argon plazma koagulációhoz, csak néhány tanulmány áll rendelkezésre, köztük 10-nél kevesebb betegnél. [64, 65]. A jelenleg rendelkezésre álló vizsgálatok alapján a YAG lézerek hasznosak lehetnek a sugárzási proktitis kezelésében, de az adatok nem elég erősek széleskörű használatuk alátámasztására. Mind az argon plazma koagulációs, mind a YAG lézerek esetében a költség és a rendelkezésre állás szintén jelentős akadályokat jelenthet.
6.4.4. Sebészet
Súlyos és kezelhetetlen vérzés esetén a műtéti lehetőségek nagyon korlátozottak, mivel az elterelés ritkán fogja teljesen szabályozni a vérzést. A hurok kolosztómiájának elterelését egy tanulmányban a vérzés szabályozásának sikeres módjaként írták le [67], de sok esetben a proctectomia lehet az egyetlen lehetőség. Amikor a szigorítás kérdés, a székletáram eltérése gyakran a tünetek jelentős javulását eredményezi. További lehetőségek közé tartozik a reszekció rekonstrukcióval, amikor a szűkület magasabb a végbélben, vagy egy előrehaladó fedél (nyálkahártya vagy bőr), amikor a végbél szűkület a végbélnyílásban van. A szövetek gyenge minősége miatt minden esetben legalább átmeneti eltérítést kell fontolóra venni. Ha műtéti kezelésre van szükség, a legtöbb tanulmány gyenge eredményeket mutat magas komplikációs arány mellett (15% –80%) és 3–9% -os halálozást [66, 68–70].
7. Következtetés
Hivatkozások
- A vese angiomyolipoma kezelésének legújabb stratégiái A diagnosztikai és terápiás áttekintés
- A koszorúér-angiográfián áteső diabéteszes beteg periprocedurális kezelése jelenlegi gyakorlat
- A szabadtéri tevékenységek, mint a túlsúly és az elhízás kezelésének eszköze a gyermekeknél 78523
- A normál szervi sugárzási dózis és az ezzel járó bizonytalanságok a nukleáris orvostudományban, hangsúlyt fektetve a
- A testmozgás metabolikus hatása a gyermekkori elhízásra egy jelenlegi nézet - ScienceDirect