Új fluor-szubsztituált (-) epigallocatechin-3-gallát analógok tumorellenes aktivitása
Huanjie Yang
1 Megelőzési program, Barbara Ann Karmanos Rák Intézet és Patológiai Tanszék, Orvostudományi Kar, Wayne Állami Egyetem, Detroit, Michigan, USA
Dong Kui Sun
2 Tengeri Kábítószer-laboratórium, Oktatási Minisztérium, Orvostudományi és Gyógyszerészeti Iskola, Kínai Óceán Egyetem, Qingdao, Kína
Di Chen
1 A megelőzési program, Barbara Ann Karmanos Rák Intézet és Patológiai Tanszék, Orvostudományi Kar, Wayne Állami Egyetem, Detroit, Michigan, USA
Qiuzhi Cindy Cui
1 Megelőzési program, Barbara Ann Karmanos Rák Intézet és Patológiai Tanszék, Orvostudományi Kar, Wayne Állami Egyetem, Detroit, Michigan, USA
Yan Yan Gu
2 Tengeri Kábítószer-laboratórium, Oktatási Minisztérium, Orvostudományi és Gyógyszerészeti Iskola, Kínai Óceán Egyetem, Qingdao, Kína
Tao Jiang
2 Tengeri Kábítószer-laboratórium, Oktatási Minisztérium, Orvostudományi és Gyógyszerészeti Iskola, Kínai Óceán Egyetem, Qingdao, Kína
Wei Chen
3 Biostatisztikai alap, Karmanos Cancer Institute és Belgyógyászati Klinika, Wayne State University, Detroit, Michigan, USA
Sheng Biao Wan
2 Tengeri Kábítószer-laboratórium, Oktatási Minisztérium, Orvostudományi és Gyógyszerészeti Iskola, Kínai Óceán Egyetem, Qingdao, Kína
K. Ping Dou
1 Megelőzési program, Barbara Ann Karmanos Rák Intézet és Patológiai Tanszék, Orvostudományi Kar, Wayne Állami Egyetem, Detroit, Michigan, USA
Absztrakt
Az epidemiológiai vizsgálatok alátámasztják a zöld tea és fő alkotóeleme (-) - epigallocatechin-gallát [(-) - EGCG] rákmegelőző hatását, azonban (-) - az EGCG fiziológiai körülmények között instabil. Itt arról számolunk be, hogy két új fluor-szubsztituált (-) - EGCG analóg gátolta a tumor növekedését, hasonló hatáserősséggel, mint a Pro-EGCG (1), amely javította a szülői vegyület (-) - EGCG-vel szembeni potenciáját az emberi emlőrákban MDA-MB- 231 xenográf. Az egyes fluorszubsztituált (-) - EGCG analógokkal kezelt MDA-MB-231 daganatok proteaszóma-gátlást és apoptotikus sejthalált mutattak ki, ami arra utal, hogy a proteaszóma lehet a fluor - (-) - EGCG-k egyik sejtcélja, és hogy a proteaszóma-gátlás részben felelős a megfigyelt daganatellenes aktivitásért.
1. Bemutatkozás
A Greaen teát az egész világon széles körben fogyasztják, és bőségesen tartalmaz polifenolokat, beleértve (-) - epigallocatechin-gallátot (EGCG), (-) - epikatechin-gallátot (EKG), (-) - epigallát-katechint (EGC) és (-) -epikatechin (EC) [1]. A (-) - EGCG, a leginkább bioaktív tulajdonságú teafehérje - rákmegelőző és rákellenes aktivitásáért felelős molekuláris mechanizmusokat alaposan tanulmányozták, és meghatározták az érintett többféle molekuláris utat, beleértve a mitogénnel aktivált protein-kinázok gátlását ( MAPK-k), a növekedési faktor szignalizációjának gátlása, a nukleáris faktor-κB (NF-κB) útvonal elnyomása és a proteaszóma gátlása [2,3].
A prosztatarákos betegekkel végzett klinikai vizsgálatok kimutatták, hogy a zöld tea fogyasztása ígéretes hatást váltott ki a rák kialakulásával szemben anélkül, hogy jelentős toxicitást váltott volna ki [4,5]. A zöld tea kivonatok klinikán történő kemoterápiás alkalmazásából nyert adatok, mivel a megállapított szilárd daganatok kezelése nem lenyűgöző, korlátozott hatékonysággal figyelhető meg [6–8], ami arra utal, hogy (-) - az EGCG nem tudta elérni a magas koncentrációt és hatékonyságot a daganat helyén . Fiziológiai körülmények között (-) - Az emberi test abszorpciója után az EGCG gyorsan metabolizálódhat [9]. Ezenkívül az (-) - EGCG hidroxilcsoportjai biotranszformációs reakciók révén módosíthatók, ideértve a metilezést, a glükuronidálást és a szulfátképződést, ami az (-) - EGCG biológiai aktivitásának csökkenését eredményezi [10,11].
Az (-) - EGCG stabilitásának és hatékonyságának javítása céljából szintetizáltuk az (-) - EGCG prodrugját, Pro-EGCG (1), az összes reaktív hidroxilcsoportot peracetátcsoportok védve. Kimutattuk, hogy a Pro-EGCG (1) képessége javult az apoptózis kiváltásában emberi emlő-, prosztata- és leukémiás rákban a (-) - EGCG-hez képest [12,13]. Az új, erős tea-polifenol-analógok, mint proteaszóma-gátlók felfedezése érdekében számos új fluor-szubsztituált (-) - EGCG-analógot terveztünk és szintetizáltunk úgy, hogy a D-gyűrűből eltávolítottuk az –OH csoportokat és egy vagy két fluorral helyettesítettük őket F-EGCG-k [14]. In vitro szűrésünk azt mutatja, hogy a fluor-szubsztituált (-) - EGCG prodrug a metil-helyzetben a fenilgyűrűn (Pro-F-EGCG2, 1A. Ábra) vagy difluor-szubsztituált (-) - EGCG mind meta-, mind para -fenilgyűrűn (Pro-F-EGCG4, 1A. ábra) a Pro-EGCG-vel (1) (1A. ábra) hasonló vagy még nagyobb potenciál volt az apoptózis kiváltásában a tenyésztett emberi emlőrákos sejtekben [14]. A jelenlegi tanulmányban eme rák-xenograft modell segítségével megvizsgáltuk ezen fluor-szubsztituált (-) - EGCG analógok in vivo hatásait daganatellenes és proteaszóma-gátló aktivitásuk szempontjából.
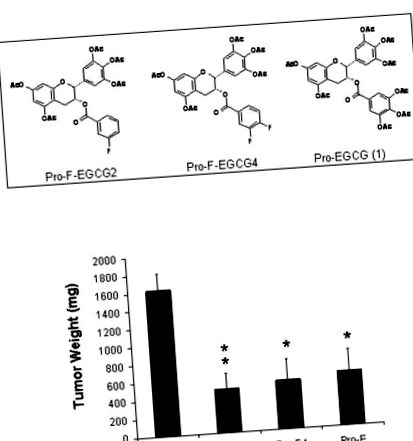
A, Fluorszubsztituált EGCG két új prodrogjának kémiai szerkezete. A Pro-F-EGCG2, a Pro-F-EGCG4 és a peracetáttal védett EGCG kémiai szerkezete [(Pro-EGCG (1)] bemutatásra került. B, Az MDA-MB-231 tumor növekedésének gátlása. A meztelen egereket sc emberi emlőrák MDA-MB-231 sejtjei (5 × 106). Amikor a daganatok kimutathatók voltak, a meztelen egereket naponta sc-ben kezeltük vagy gyógyszeres hordozóval (n = 9), vagy 50 mg/kg Pro-F-EGCG2-vel (Pro -F2) (n = 9), Pro-F-EGCG4 (Pro-F4) (n = 9) vagy kontroll peracetáttal védett EGCG (Pro-E) (n = 6), a Anyagok és metódusok. A 31 napos kezelés végére az egereket elpusztítottuk, és a tumorokat lemértük. Pontok, a tumor súlyának átlaga; bárok, SE. **, p6) 0,1 ml szérummentes RPMI 1640-be szuszpendálva, s.c. minden egér jobb szélén. A whentumorok elérték a méretét
120 mm 3, az egereket véletlenszerűen csoportosítottuk, és napi s.c. injekció 50 mg/kg Pro-F-EGCG2 vagy Pro-F-EGCG4 (csoportonként kilenc egér). Kontrollként [20% DMSO és 80% kremofor/etanol (3: 1)] (kilenc egér) és azonos dózisú Pro-EGCG (1) (hat egér) kezelést használtunk [13]. A daganat méretét minden második nap féknyereggel mértük, és térfogatukat standard képlet szerint számítottuk: szélesség 2 × hosszúság/2. Az egereket 31 napos kezelés után feláldoztuk, amikor a kontroll daganatok elérték
1500 mm 3. A daganatokat lemértük, és a tumorszöveteket különböző vizsgálatokhoz gyűjtöttük.
2.4. A terminális nukleotidil-transzferáz által közvetített nick end jelölés (TUNEL), a p27 és a Hematoxylin és Eosin (H & E) immunfestése tumorszövetek alkalmazásával
A terminális nukleotidil-transzferáz-mediált nick end jelölés (TUNEL) tesztet in situ apoptózis detektáló készlet alkalmazásával és a p27 immunfestését a korábban leírtak szerint végeztük [15]. A H & E festést a daganatos szövetekben a gyártó protokolljai szerint végeztük.
2.5. Proteasome aktivitási vizsgálat
Az MDA-MB-231 daganatok teljes szövetkivonatait (10 μg) inkubáltuk Suc-Leu-Leu-Val-Tyr-AMC (20 μmol/L) fluorogén szubsztráttal 37 ° C-on, 100 μL vizsgálati pufferben (50 mmol/1). L Tris-HCl, pH 8,0) 2 órán át. Inkubálás után a hidrolizált 7-amino-4-metil-kumarin (AMC) csoportok termelését Victor 3 Multilabel Counter alkalmazásával mértük 380 nm-es gerjesztőszűrővel és 460 nm-es emissziós szűrővel (Perkin-Elmer).
2.6. Western blot elemzés
A daganatszöveti kivonatokat (40 μg) SDS-PAGE-vel elválasztottuk és nitrocellulóz membránra vittük, majd ezt a korábban ismertetett továbbfejlesztett kemilumineszcens készlet (Amersham Biosciences) felhasználásával tettük láthatóvá [16].
2. 7. Statisztikai elemzés
120 mm 3), az egerek s.c. naponta kezelõanyagként kontrollként vagy 50 mg/kg Pro-F-EGCG2, Pro-F-EGCG4 vagy Pro-EGCG (1) kezeléssel összehasonlításképpen. A 31. nap végén a kontrolldaganatok átlagosan 1620,6 ± 562,6 mg-ra nőttek (1B. Ábra). A Pro-EGCG (1) kezelt daganatok 597,9 ± 603,1 mg-ra nőttek, ami 63% -os daganatnövekedés gátlást mutatott (p = 0,015), ami hasonló a korábbi jelentésünkhöz (54% tumor növekedésgátlás) [13]. Hasonlóképpen, a Pro-F-EGCG4-vel kezelt daganatok 537,4 ± 706,7 mg-ra nőttek (1B ábra),
A tumor növekedésének 67% -os gátlása statisztikailag eltér a kontroll kezeléstől (p = 0,03). A Pro-F-EGCG2-vel kezelt tumorok 480,5 ± 517,6 mg-ra nőttek, ami azt mutatja
A tumor növekedésének 70% -os gátlása, amely jelentősen eltér a vivőanyag-kezeléstől (p 0,3). Ezek az eredmények azt mutatják, hogy a fluorszubsztituált (-) - EGCG analóg, a Pro-F-EGCG2 és a Pro-F-EGCG4 prodrugja hasonló a Pro-EGCG (1) daganatnövekedés gátlásához az MDA-MB-231 melldaganat modellben . Az egerek 50 mg/kg/nap Pro-F-EGCG kezeléssel szemben tarthatónak bizonyultak a 31 napos periódus alatt. Súlycsökkenést és csökkent aktivitást nem figyeltek meg mind a Pro-F-EGCG2, mind a Pro-F-EGCG4 kezelt állatoknál.
3.2. A fluorszubsztituált EGCG analógok apoptózist indukálnak az emlődaganat xenograftjában
A fluor-szubsztituált EGCG e két új prodrugja in vitro apoptózist indukált [14]. Annak megállapítására, hogy elérhetik-e a tumorsejteket és in vivo kiválthatják-e az apoptózist, többszörös vizsgálatot végeztek tumorszöveti minták felhasználásával. A PARP-hasítást, az apoptózis indikátorát [17] nagyobb mértékben detektáltuk a Pro-F-EGCG2-vel vagy a Pro-F-EGCG4-vel kezelt daganatok kivonataiban, mint a vivőanyaggal kezeltek (2A. Ábra). Ezenkívül a TUNEL-pozitivitással jelzett apoptotikus sejteket figyelték meg Pro-F-EGCG2-vel vagy Pro-F-EGCG4-vel kezelt állatok daganataiban (2B. Ábra). Apoptotikus magokat, amint azt H&E festéssel végzett magkondenzáció mutatja, Pro-F-EGCG2-vel vagy Pro-F-EGCG4-vel kezelt állatok daganataiban figyeltük meg (2B. Ábra). Összehasonlításképpen, a kontroll tumorokat a sejtproliferáció jó állapotában figyelték meg, amint azt több mag, mitotikus kromoszóma mutatja (2B. Ábra). Hasonló eredményeket figyeltünk meg minden csoport több daganatmintájában.
A tumorszöveteket vivőanyaggal (V) vagy Pro-F-EGCG2-vel (Pro-F2) vagy Pro-F-EGCG4-vel (Pro-F4) kezeltük. A fehérjéket a tumorszövetekből extrahálták, majd Western-blot-analízist követtek PARP (A) elleni antitest alkalmazásával. A PARP teljes hossza 116 kDa, míg a PARP hasított formája 65 kDa. B, a tumorszöveteket metszettük, majd TUNEL vizsgálatot és H&E festést végeztünk. A Pro-F-EGCG-vel kezelt tumorok TUNEL pozitív sejteket mutattak barna színnel és kondenzált magokkal a H&E festés során. Nagyítások, × 400.
3.3 A fluorszubsztituált EGCG analógok gátolják a proteaszómát a tumorszövetekben
A daganatokat vivőanyaggal (V) vagy Pro-F-EGCG2-vel (Pro-F2) vagy Pro-F-EGCG4 (Pro-F4) kezeltük az 1. ábrán leírtak szerint, és szöveteket használtunk. A, Proteasomális kimotripszin-szerű aktivitásvizsgálat. A fehérjéket a tumorszövetekből extrahálták, és proteaszóma aktivitás vizsgálatnak vetették alá Suc-LLVY szubsztrát alkalmazásával a kimotripszinszerű aktivitáshoz, amint azt a Anyagok és metódusok. Az ubiquitinnated protein fehérje szintjét, valamint a p27 és Bax proteaszóma célpontokat Western-blot-analízissel elemeztük (B). A p27 ubiquitinizált formáját (70 kDa) nyíllal jelöltük. Bax, mind a p21, mind a p18 formát bemutattuk. Az aktint használták terhelés kontrollként. C, immunkémia p27 antitesttel. A tumorszöveteket immunkémia céljából p27 antitest alkalmazásával szekcionáltuk. Nagyítások, × 400.
Összefoglalva, eredményeink azt mutatják, hogy a fluor-szubsztituált EGCG analógok prodrugjai proteaszóma-gátlást és apoptózis-indukciót indukáltak in vivo, amint azt in vitro megfigyelték [14], és hasonlóak a Pro-EGCG-hez (1), a fluor-szubsztituált (- ) -EGCG analógjainak erős anti-emlőrák aktivitása volt in vivo.
4. Megbeszélés
A proteasoma-gátlót, a Bortezomib-et klinikai vizsgálatokban hematológiai rosszindulatú daganatok kezelésére alkalmazták [21], támogatva, hogy a proteasoma megcélzása hatékony stratégia. A bortezomib-kezeléssel összefüggő gyakori toxikus mellékhatásokat azonban megfigyeltek [21]. Ezenkívül a Bortezomib korlátozott hatást mutatott a szilárd daganatokkal szemben [21], ami arra ösztönzi a kutatókat, hogy fejlesszenek ki új proteaszóma inhibitorokat a szilárd daganatok, köztük az emlőrák kezelésére.
(-) - Az EGCG, a zöld tea fő összetevője egy erős proteaszóma inhibitor [22]. Gátolta a megtisztított 20S proteaszómát, amelynek IC50-értéke 0,2–0,6 μmol/L volt. Mindazonáltal mindig nagy koncentrációra van szüksége a sejtes proteázóma gátlásához, ami arra utal, hogy az (-) - EGCG sejtereje csökkent. Valójában a (-) - EGCG gyors lebomlásnak és számos biológiai módosításnak van kitéve, ami a (-) - EGCG aktivitásának csökkenését eredményezi [23]. Az (-) - EGCG-hez képest prodrugja, a fenolgyűrűk összes reaktív hidroxilcsoportján peracetátvédelemmel rendelkező Pro-EGCG (1) fokozott tumorellenes aktivitást mutatott, amely a proteaszóma gátlásának fokozott aktivitásával és az apoptózis indukciójával társult [13].
Ebben a tanulmányban két új szintetizált fluor-szubsztituált (-) - EGCG prodrug tumorellenes aktivitását teszteltük. Észrevesszük, hogy bár a legtöbb kezelt egérben a Pro-F-EGCG2 és a Pro-F-EGCG4 hatásos daganatellenes aktivitást mutatott, a Pro-F-EGCG2-vel vagy a Pro-F-EGCG4-vel kezelt csoport egyik egere a kontrollhoz hasonló daganatot növesztett, ami azt sugallja, hogy a fluor-szubsztituált (-) - EGCG-kezelésre adott válasz változó volt. Ennek ellenére a statisztikai elemzés azt sugallja, hogy a fluorszubsztituált (-) - EGCG analógok a Pro-EGCG-hez hasonlóan (1) hasonlóan szignifikánsan gátolták az emlődaganat növekedését (1. ábra).
A vizsgált dózisban (50 mg/kg/d) mind a mono-, mind a difluor-szubsztituált EGCG-analógok hatékony koncentrációt értek el, amelynél a PARP hasítás, a TUNEL-pozitivitás és a kondenzált sejtmagok által bizonyított tumorokban apoptózist váltottak ki (2. ábra), és gátolták a sejtes proteaszóma, amint azt a csökkent proteazomális kimotriptiás aktivitás és a megnövekedett proteaszomális szubsztrátok, például a p27, a Bax, valamint az ubiquitinált fehérjék szintje mutatja (3. ábra).
A fluorszubsztituált (-) - EGCG prodrogjai indukáltak
A tumor növekedésének 67–70% -os gátlása (1. ábra). Mindazonáltal 33–42% -os gátlást okoztak a proteasomális kimotriptiás aktivitásban (3. ábra), ami arra utal, hogy a proteaszóma csak egyike lehet a fluorszubsztituált (-) - EGCG produgok sejtcéljainak, és hogy a proteasoma gátlás részben felelős lehet a tumor növekedésének gátlása. A jövőben fel kell fedezni a megfigyelt daganatnövekedés gátlásában részt vevő más molekulákat.
Meztelen egérmodellünkben a fluor-szubsztituált (-) - EGCG-vel kezelt egerekben a 31 napos kezelés alatt nem figyeltek meg súlycsökkenést és csökkent aktivitást, ami arra utal, hogy a fluor-szubsztituált (-) - EGCG tolerálja az egerek modelljét.
A meztelen egereken végzett in vivo megfigyelésünk együttvéve összhangban áll az in vitro eredményeinkkel, amelyek azt mutatják, hogy a fluorral szubsztituált EGCG prodrogjai hatékonyan gátolják az emlőrák növekedését az egerek számára tolerált dózisban, ami részben társul a proteaszóma gátlásával a tumorban szövet. Hogy a fluorszubsztituált (-) - EGCG és prodrogjaik biotranszformálódhatnak-e, a jövőben határozzák meg.
Köszönetnyilvánítás
Ezt a kutatást részben támogatja a Wayne Állami Egyetem Karmanos Cancer Institute (QP Dou-nak), National Cancer Institute/NIH (1R01CA120009; 3R01CA120009-04S1 - QP Dou) és a National Cancer Institute/NIH Cancer Center Támogatási támogatás (Karmanos Cancer számára) Intézet). Köszönetet mondunk a Karmanos Rák Intézet Patológiai Alapkezelőjének a TUNEL és az immunhisztokémiai vizsgálatokban való közreműködésért.
Lábjegyzetek
Összeférhetetlenség
Megerősítettük, hogy az „Új fluor-helyettesített (-) - epigallokatechin-3-gallát-analógok” című kéziratunk benyújtásával és közzétételével kapcsolatban nincs potenciális összeférhetetlenség. Az összes szerző elolvasta és jóváhagyta a Cancer Letters elküldését.
Összeférhetetlenség
Az összes szerző megerősíti, hogy a publikációval kapcsolatban nincs potenciális összeférhetetlenség.
Kiadói nyilatkozat: Ez egy szerkesztetlen kézirat PDF-fájlja, amelyet kiadásra elfogadtak. Ügyfeleink számára nyújtott szolgáltatásként a kéziratnak ezt a korai változatát biztosítjuk. A kézirat átmásolásán, szedésén és a kapott bizonyíték felülvizsgálatán átesik, mielőtt a végső hivatkozható formában közzétennék. Felhívjuk figyelmét, hogy a gyártási folyamat során olyan hibákat fedezhetnek fel, amelyek befolyásolhatják a tartalmat, és a naplóra vonatkozó minden jogi felelősségvállalás vonatkozik.
- Egy újszerű indolin származék enyhíti a cukorbetegség által kiváltott krónikus vesebetegséget azáltal, hogy csökkenti
- Újszerű MFSD8 mutáció egy esetleges 7. típusú neuronális ceroid lipofuscinosisban szenvedő orosz betegben
- Visszatérés a fogyáshoz - újszerű megközelítés - Healthwise
- Súlyának értékelése Egészséges testsúly, táplálkozás és fizikai aktivitás CDC
- Az aszpartám megakadályozhatja, és nem elősegítheti a súlycsökkenést azáltal, hogy blokkolja a bélenzim aktivitását