Új stratégia a leptin elhízási terápiában történő alkalmazásához
Absztrakt
Bevezetés
Az elhízás krónikus betegség, és jelentős globális egészségügyi kihívás. A költséges és nem kockázat nélküli bariatri műtéten kívül jelenleg nincsenek sikeres elhízási kezelési lehetőségek. Az elhízás farmakológiai szereinek története turbulens volt, számos példa a gyógyszerek jelentős mellékhatások miatt történő eltávolítására a piacról. Az orlisztát és a szibutramin (a legújabb gyógyszerek a piacon) csak mérsékelt fogyást eredményeznek, és mindkettőjükhöz az elviselhetetlen mellékhatások miatt magas kopási arány társul. Ezenkívül a sibutramint nemrég kivonták a piacról. Szükség van az elhízás biztonságos és hatékony gyógyszeres kezelésének kifejlesztésére.
Fedett területek
A leptin-terápia mint ritka betegségek gyógyszere, a leptin-szubsztitúciós terápia, mint elhízás kezelése, preklinikai vizsgálatok, amelyek bemutatják a leptin/amylin kombináció hatékonyságát, és végül a nagyon ígéretes korai klinikai eredmények, amelyek pramlintid/meteleptin kombinációs terápiát alkalmaznak túlsúlyos, elhízott egyéneknél.
Szakértői vélemény
Az elhízás kezelésére szolgáló kombinált farmakológiai terápia, mint például a pramlintid/metreleptin, nagyon ígéretes, és a korai fázisú klinikai vizsgálatok során ösztönözni kell a fogyás eredményeit és az anyagcsere-készítők javulását. A pramlintid/metreleptin legújabb, randomizált klinikai vizsgálatát azonban nemrégiben leállították biztonsági okokból.
1. Bemutatkozás
Az elhízás kezelésére szolgáló új gyógyszerek farmakológiai fejlesztése során a termék biztonsága kiemelt fontosságú, és figyelembe kell venni az elhízás által az egyén számára jelentett kockázatok és a kábítószer-kezelés során felmerülő lehetséges problémák mérlegelésével. Sajnos az elhízás farmakológiai kezelésének története nagyrészt a biztonsági aggályok miatt turbulens volt [1,2]. Az elhízás krónikus betegség, amelynek számos oka van, és mindez tartós egyensúlyhiányhoz vezet az energiafogyasztás és az energiafelhasználás között. Az így létrejövő zsírszövet-felesleg számos betegség, köztük a 2-es típusú cukorbetegség és a szív- és érrendszeri betegségek, egyes típusú rákos megbetegedések, fogyatékosságok, tüdő- és gyomor-bélrendszeri szövődmények, valamint depresszió magasabb kockázatához kapcsolódik [3]. Amint az várható egy ilyen komplex betegségtől, amely a környezet és számtalan érzékenységi gén kölcsönhatásából származik, a gyógyulás ritka, ezért a kezelés pallérozásra irányul. Bármi legyen is a farmakológiai szer elsődleges hatáshelye, a nettó hatásnak az élelmiszer-bevitel csökkenésének és/vagy az energia-ráfordítás növekedésének kell lennie.
Az egyedüli szerek általában nagyon megtévesztettek, és az orvosoknak ma már szinte nincsenek hosszú távú farmakológiai eszközei a betegség kezelésére. Mivel azonban a Fen-Phen, a fenfluramin és a fentermin kombinációja népszerű sikert aratott az 1980-as években [4], világossá vált, hogy gyógyszerek kombinációjára lesz szükség az elhízás sikeres kezeléséhez annak ellenére, hogy a fenfluramint kivonták a piacról 1996 halálos pulmonalis hipertónia miatt. Tekintettel az étrendi beavatkozások hosszú távú gyenge sikerére, valamint az anorektikus kismolekulákhoz kapcsolódó szerény hatékonyságra és elhúzódó biztonsági aggályokra, sürgős szükség van olyan új megközelítésekre, amelyek a tudományos előrehaladást innovatív terápiákká alakítják, amelyek tartós, klinikailag értelmes fogyást kínálnak minimális mértékben mellékhatások. Ezek a célok számos gyógyszeripari és biotechnológiai vállalatot arra késztettek, hogy randomizált, kettős-vak klinikai vizsgálatokat indítsanak az elhízás kezelésére létező gyógyszerek kombinációival. Nemrégiben javasolták egy racionális és ígéretes kombinatorikus neurohormonális megközelítés alkalmazását olyan peptid hormonok alkalmazásával, amelyek fiziológiás szerepet játszanak a táplálékfelvétel és a testtömeg szabályozásában, és potenciálisan mentesek a céltól eltérő toxicitásoktól.
1. doboz. Kábítószer-összefoglaló
| Gyógyszer neve | Pramlintide-acetát | Metreleptin (rekombináns-metionil humán leptin) |
| Fázis | Az FDA jóváhagyta, 2005. március | A III. Szakaszban |
| Jelzés | 1-es típusú cukorbetegség: 30 vagy 60 fenntartó dózis (tolerálva), 15 mg-os adagtól titrálva Inzulint használó 2-es típusú cukorbetegség: 120 μg fenntartó dózis (tolerálva), 60-as adagtól titrálva | Veleszületett leptinhiány, lipodystrophia, hypothalamus amenorrhoea és leptin helyettesítő terápia a testsúly fenntartása érdekében |
| Farmakológiai leírás | A 2-es és az 1-es típusú inzulint használó betegeknél végzett klinikai vizsgálatokban a pramlintide beadása az étkezés utáni átlagos glükózkoncentráció csökkenését, a glükózingadozások csökkenését és az ételfogyasztás csökkenését eredményezte. Csúcs: 15 perc [50] Felezési idő: 20 - 50 perc [50,51] | A nem klinikai és klinikai vizsgálatok eredményei alapján a metreleptin hatásmechanizmusa a következő: • A leptinhiány miatt másodlagos hyperphagia korrekciója, valamint a kalória- és zsírbevitel egyidejű csökkentése [52,53] • A zsírsav oxidációjának stimulálása az egész testben, valamint a plazma, a máj és a myocellularis lipidszint csökkentése, ami fokozott inzulinérzékenységet és jobb glikémiás kontrollt eredményez [54-61] • A máj glükóztermelésének inzulinszuppressziójának javulása és az izom által stimulált perifériás glükózfelvétel növekedése az izomban [20,54,62] Ezért a leptin több mechanizmuson keresztül hat a triglicerid és más lipid intermedierek csökkentésére lipodisztrófiás betegeknél, csökkentve azok felhalmozódását olyan szövetekben, mint a máj és az izom, és enyhíti a súlyos inzulinrezisztenciát, javítva ezáltal a hiperglikémiát és a hipertrigliceridémiát Csúcs: 4 óra [63] Felezési idő: 2 - 5 óra [63,64] |
| Az alkalmazás módja | Szubkután a combba vagy a hasba, az inzulin injekció helyétől elkülönítve, közvetlenül a fő étkezések előtt (≥ 250 kcal vagy ≥ 30 g szénhidrát) | Szubkután a hasba |
| Kémiai szerkezet | Lys-Cys-Asn-Thr-Ala-Thr-Cys-Ala-Thr-Gln- Arg-Leu-Ala-Asn-Phe-Leu-Val-His-Ser-Ser- Asn-Asn-Phe-Gly-Pro-Ile-Leu-Pro-Pro-Thr- Asn-Val-Gly-Ser-Asn-Thr-Tyr-NH2-acetát (só) diszulfid híddal a két Cys maradék között [65] | NH2-Met-Val-Pro-Ile-Gln-Lys-Val-Gln-Asp-Asp-Thr-Lys- Thr-Leu-Ile-Lys-Thr-Ile-Val-Thr-Arg-Ile-Asn-Asp-Ile-Ser- His-Thr-Gln-Ser-Val-Ser-Ser-Lys-Gln-Lys-Val-Thr-Gly-Leu- Asp-Phe-Ile-Pro-Gly-Leu-His-Pro-Ile-Leu-Thr-Leu-Ser-Lys- Met-Asp-Gln-Thr-Leu-Ala-Val-Tyr-Gln-Gln-Ile-Leu-Thr- Ser-Met-Pro-Ser-Arg-Asn-Val-Ile-Gln-Ile-Ser-Asn-Asp- Leu-Glu-Asn-Leu-Arg-Asp-Leu-Leu-His-Val-Leu-Ala-Phe- Ser-Lys-Ser-Cys-His-Leu-Pro-Trp-Ala-Ser-Gly-Leu-Glu- Thr-Leu-Asp-Ser-Leu-Gly-Gly-Val-Leu-Glu-Ala-Ser-Gly- Tyr-Ser-Thr-Glu-Val-Val-Ala-Leu-Ser-Arg-Leu-Gln-Gly- Ser-Leu-Gln-Asp-Met-Leu-Trp-Gln-Leu-Asp-Leu-Ser-Pro- Gly-Cys-COOH |
| Pivotális vizsgálat (ok) | 1-es típusú cukorbetegség: [66-68] 2-es típusú cukorbetegség: [69-71] | Veleszületett leptinhiány [18] Lipodisztrófia: [20] Hypothalamicus amenorrhoea: [22] Elhízás: [26,48] Súly fenntartása: [38] |
2. A pramlintid és a metreleptin összefoglalása
A pramlintide-acetátot, az amilin szintetikus analógját, szubkután injekcióval adják be a fő étkezések előtt, hogy csökkentse az étkezés utáni glükózszintet az 1. és 2. típusú cukorbetegeknél. Az amylin egy 37 aminosav peptid hormon, amelyet hasnyálmirigy β-sejtek inzulinnal együtt szekretálnak. Az inzulinhoz hasonlóan a plazma amilinkoncentráció is gyorsan növekszik az étkezés hatására, étkezés után körülbelül 30 perccel éri el a csúcsot, és kb. 2 óra elteltével tér vissza az alapvonalra [11]. Az éhomi amilinszinteket egészséges egyéneknél 3 - 25 pmol/l tartományban jelentették [12]. Az étkezés bevitelére adott amilin-válasz hiányzik az 1-es típusú diabetes mellitusban (T1DM), túlzott az elhízás és csökken a 2-es típusú diabetes mellitusban (T2DM).
A humán amilin általában oldhatatlan és hajlamos az aggregálódásra, kizárva a natív peptid terápiás alkalmazását. Ennek leküzdése érdekében az emberi amilin oldható, nem aggregálódó, ekvipotens analógját, a pramlintidot fejlesztették ki és hagyta jóvá az FDA 2005-ben. A pramlintidet a szintetikus 37 aminosav-polipeptid acetát-sójaként forgalmazzák, amely aminosav-szekvenciában különbözik. humán amilinnel prolinnal történő helyettesítéssel a 25. (alanin), 28. (szerin) és 29. (szerin) pozícióban, molekulatömege 3949,4 Da. Farmakokinetikai vizsgálatok kimutatták, hogy az 1-es típusú cukorbetegségben szenvedő betegek 30 és 60 μg-os, a 2-es típusú cukorbetegségben szenvedő betegek esetében pedig 120 μg-os pramlintid dózisa olyan plazma pramlintid-koncentrációt eredményez, amely megközelíti az élettani betegek fiziológiai amilinkoncentrációját. A pramlintide-használók leggyakoribb mellékhatásai a gyomor-bélrendszeri eseményekhez kapcsolódnak, beleértve a hányást, émelygést és hasi fájdalmat. Emellett a pramlintid kiegészítő kezelésként étkezési inzulinterápiát alkalmazó betegeknél, valamint a pramlintide inzulinnal történő együttes alkalmazása növelheti az inzulin által kiváltott hipoglikémia kockázatát, különösen az 1-es típusú cukorbetegségben szenvedő betegeknél [13]. A pramlintid farmakokinetikáját és farmakodinamikáját jól ismertették a korábban publikált áttekintések [14,15].
A rekombináns metionil humán leptin néven is ismert metreleptin az emberi leptin hormon analógja. A metreleptin Escherichia coliban történő expresszálásához az emberi leptin érett fehérjét (146 aminosav) kódoló szekvenciát kémiailag szintetizálták optimális E. coli kodonok felhasználásával. Ennek a szintézisnek a részeként az ATG (metionint kódoló) nukleotidokat hozzáadták a humán leptin génjének 5 ’végéhez. Ezért az e szekvencia által kódolt metreleptin fehérje 147 aminosav hosszúságú, kezdve a metioninnal, és a kiszámított molekulatömege 16 156 Da. A metreleptin-kezelést nagyrészt veleszületett leptinhiányban, lipodystrophiában és hypothalamus amenorrhoában szenvedő betegeknél alkalmazzák.
3. A leptin, mint ritka gyógyszer az embereknél
Az első bizonyíték, amely rámutatott a leptin-helyettesítő kezelés elhízás esetén történő alkalmazására, 1997-ben történt, amikor O'Rahilly és munkatársai két súlyosan elhízott gyermeket találtak, akik mutációt hordoztak a leptin génben [16]. Ez a két gyermek unokatestvér volt egy pakisztáni származású, nagyon rokonokból álló családban, akiknek mindkettőjük homozigóta kereteltolódási mutációval rendelkezett, amely egyetlen guanin nukleotid delécióját tartalmazta a leptin gén 133. kodonjában. Ennek eredményeként nagyon alacsony a keringő leptinszint, extrém hyperphagia és súlyos elhízás volt [16]. Ezek a kutatók azt mutatták, hogy a rekombináns humán leptin napi négy éven át végzett szubkután injekciói enyhíthetik a hiperfágia kialakulását, a korai életkorban tapasztalható túlzott súlygyarapodást és ezen gyermekek súlyos elhízását [17]. Esettanulmány-tanulmányban napi szubkután rekombináns leptin (0,028 mg/kg) injekciókat 12 hónapig adtak be egy 9 éves, veleszületett leptinhiányos lánynál. A kiinduláskor a beteg súlya 94,4 kg volt (életkor szerint> 99,9. Percentilis), a magasság a 91. percentilisnél volt (ha a csontkorhoz igazítottuk), a szérum leptinszintje pedig a kimutatási határ alatt volt. A leptin-kezelés után a beteg 16,4 kg-ot fogyott (
A leptinpótló terápia biztonságos és hatékony terápiának bizonyult a hipotalamusz amenorrhoea (HA) kezelésében is. Ez a rendellenesség a menstruációs ciklusok megszűnésével jellemezhető, amelyet általában a megerőltető testmozgás és/vagy a csökkent ételfogyasztás okozta krónikus energiahiány okoz. anorexia nervosa-ban szenvedő betegeknél [22,23]. A HA-ban szenvedő nők hajlamosak a hipoleptinémiára [24,25], a koncepció bizonyítékú tanulmányával, amely azt mutatja, hogy a 3 hónapos leptin-helyettesítő terápia nemcsak az ösztrogén, a pajzsmirigyhormonok és az IGF-1 szintjét normalizálta, de ami a legfontosabb, helyreállította az ovulációs menstruációt [22 ]. Egy ezt követő randomizált, kettős-vak, placebo-kontrollos vizsgálat, 36 héten át tartó humán rekombináns leptin (metreleptin) helyettesítő terápiával HA-ban szenvedő nőknél hasonló javulást mutatott az ivarmirigy, a pajzsmirigy, a növekedési hormon és a mellékvesék tengelyében, de javult a csontanyagcsere markereiben is, csontképződésre utaló [23].
4. A leptin alkalmazása elhízás klinikai vizsgálatokban
Ezzel szemben a leptin ígérete, mint önálló varázslövedék az elhízás kezelésére, rövid életű volt. 1999-ben randomizált, kontrollált dózis-válasz vizsgálatot végeztek napi szubkután rekombináns leptin injekcióval 54 sovány és 73 elhízott alanyon. A 4 hétig tartó vizsgálat kezdeti szakaszában a sovány és elhízott alanyok hasonló mennyiségű testsúlycsökkenést szenvedtek a leptin-kezelés során, ami statisztikailag szignifikáns volt a kiindulási értékhez képest (p = 0,02) [26]. Az elhízott alanyokat további 20 hétig tanulmányozták. A vizsgálatot befejező 47 beteg közül a legmagasabb leptin-dózist kapó 8 beteg 7,1 kg-ot fogyott (p = 0,01 a kiindulási értékhez képest), míg a placebót kapó betegek 1,3 kg-ot. A hatások a betegek körében nagyban változtak, a 15 kg-os fogyástól az 5 kg-os súlygyarapodásig a legnagyobb dózissal kezelt csoportban. Ezenfelül ezek az adagok a bőr 62% -ában bőrirritációt és duzzanatot, a betegek felében pedig fejfájást váltottak ki. Annak reménye, hogy a leptin terápia lesz az elhízás gyógyszere, a vizsgálat után eltűnt annak ellenére, hogy az Amgen Pharmaceuticals számos kísérletet folytatott a hormon további tanulmányainak folytatására, amelyet sok kutató úgy gondolt, hogy az elhízás kezelésének csodaszere.
5. Leptinpótló stratégia az elhízás terápiájához
A csökkent testsúly fenntartása metabolikus reakcióval jár, amelynek célja a további fogyás elleni védekezés. Ezt a választ az energiafogyasztás csökkenése jellemzi, amely meghaladja a testösszetétel változásait [27-29], a tompa neuroendokrin funkciókat (a pajzsmirigy és a reproduktív tengely elnyomott, a szimpatikus aktivitás csökken és a parasimpatikus aktivitás megnövekszik), valamint a keringő leptin szintet. növelik. Ez az anyagcsere-alkalmazkodás a kalóriakorlátozáshoz, legalábbis részben megmagyarázza a fogyott testsúly időbeli visszanyerését, és összefüggésbe hozhatónak tűnik a fogyáskor bekövetkező leptincsökkenéssel [30-32]. Azt javasolták, hogy a leptin elsődleges élettani szerepe nem a jóllakottság jele, hanem a testzsírkészletek védelme a hosszan tartó energiahiánnyal szemben [33-35].
A reproduktív, a pajzsmirigy és a mellékvese tengelyének exogén leptin-indukálta helyreállítása, valamint a másodlagos amenorrhoában és hipoleptinémiában szenvedő nőknél a csontképződés markereinek növekedése (azaz krónikus energiahiány miatt) támogatná a központi leptin-érzékenység helyreállításának hipotézisét [22, 23]. Ezzel egyetértésben a metreleptin csak akkor fordította meg a korlátozott kalóriatartalmú egyének metabolikus fenotípusát, amikor a keringő leptin jelentősen, 30% -kal csökkent és több héten keresztül fennmaradt [38,39], és nem azoknál, akiknél a keringő leptin a mérsékelt kalóriatartalom miatt megnőtt. korlátozás [40]. Ha egy ilyen hipotézis igaz lenne, a metreleptin alkalmazása a testsúly-csökkentő terápiában csak akkor lenne hatékony, ha más leptin-szenzibilizáló kezelések kiegészítéseként alkalmaznák, megakadályozva ezzel a kalória korlátozás által kiváltott metabolikus adaptációt és elősegítve a testsúly fenntartását.
6. Preklinikai vizsgálatok leptin/amylin kombinációval rágcsálókon
Amint azt a fentiekben leírtuk, úgy tűnik, hogy az elhízással kapcsolatos leptin-rezisztenciát a hipotalamusz leptin-működésének hibái okozzák [41,42].
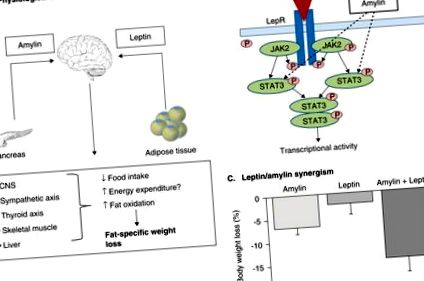
Az amilin/leptin kombinált terápia javasolt fiziológiai hatása az, hogy az amilin, egy neuroendokrin hasnyálmirigy-peptid, amely hozzájárul a rövid távú energiaszabályozáshoz, és a leptin, egy jól bevált hormon, amely hozzájárul a hosszú távú energiaszabályozáshoz, szinergikusan hat a központi idegrendszerben azáltal, hogy csökkenti az élelmiszer-bevitelt. és az energiafelhasználás növelése (A). Az íves magban az amilin növeli a leptin jelátviteli útvonal jelátalakítójának és a 3 transzkripció aktivátorának (STAT3) foszforilációját, ami a központi leptin érzékenység növekedését vagy helyreállítását eredményezi [9,47] (B), és ezért a fogyás szinergikus hatásait, összehasonlítva az önmagában alkalmazott amilinnel vagy leptinnel [10] (C).
LepR: Leptin receptor.
- A teljes rendszerek ájurvédikus orvostudomány és jógaterápiás kezelés eredményei az elhízás kísérleti tanulmányában
- Reflexológia Hagyományos thai masszázs fa relaxációs spa terápia teljes test masszázs eszköz (# 5)
- Miután alultápláltak, Brazília szegényeinek új problémája van az elhízással - a Washington Post
- A genetikai elhízással küzdő gyerekek stimulálása segít a BMI és az étvágy csökkentésében, tanulmányi eredmények
- Tapasztalatom a méhméreg-terápiával - Rebecca Hayward - Lyme Disease UK