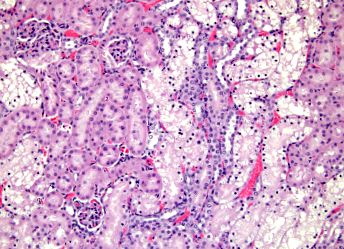
Vese tubulusok
A vesetubulusok számos fontos funkciót hordoznak, amelyek megmagyarázhatják számos szabályozó fehérje, beleértve a CSN – CRL útvonal komponenseinek felhalmozódását ezekben a szövetekben.
Kapcsolódó kifejezések:
- Parathormon hormon
- Újrafelszívódás
- Kiválasztás
- Hámsejtek
- Fehérjék
- Nephrons
- Vizelet
- Proximális tubulusok
Letöltés PDF formátumban
Erről az oldalról
Vese
John Curtis Seely,. Brad Blankenship, Boorman Patkánya a patkányról (második kiadás), 2018
4.3 Degeneratív változások
A vesetubulus degeneráció szintén gyakran megfigyelt elváltozás, amely nem vezet szükségszerűen tubulus nekrózishoz. A vakuolizáció a degeneráció közös jellemzője (11.35. Ábra). A vese tubulusokban végzett vakuolizáció azonban számos citoplazmatikus komponens, például az endoplazmatikus retikulum, a mitokondrium, a lizoszómák vagy más sejtalkotók változását tükrözheti.
11.35. Ábra. Vakuoláris degeneráció több tubulusban, amelyek kiemelkedő citoplazmatikus vakuolákat és piknotikus magokat tartalmaznak.
A degeneráció nem specifikus formája, amelyet basofil tubulusnak neveznek, a CPN korai eseteiben gyakran előfordul, és a toxikus tubulus károsodásának gyakori megnyilvánulása patkány vizsgálatokban (11.36. Ábra). Mivel a tubulus bazofília biokémiai zavarokat jelenthet, sérülés vagy helyrehozás bizonyítéka nélkül, a bazofil tubulus kifejezést nem szabad felcserélni a tubulus regenerációjával, a tubulus hipertrófiájával vagy a tubulus hiperpláziájával. Jelentős bazális membrán megvastagodás hiánya segít megkülönböztetni a toxikus sérüléssel járó bazofil tubulusokat a CPN-hez kapcsolódó bazofil tubulusoktól.
11.36. Ábra A bazofil tubulusok fókusza. Vegye figyelembe az alapmembrán megvastagodásának hiányát.
A lipofuscin (ceroid) pigment a patkányok veséjében gyakori, és az állatok öregedésével egyre hangsúlyosabbá válik, megközelítve a 2 éves patkányok 100% -os előfordulását. A lipofuscin sárga, szemcsés citoplazmatikus pigment, amely a vesetubulusokban és az interstitiumban található. A hemosiderin pigment a proximális tekercselt tubulusok citoplazmájában fordul elő, különösen immunmediált hemolitikus anaemia esetén (11.37. Ábra). Speciális foltokat, például Perl és Schmorl foltokat használnak a vas, illetve a lipofuscin megkülönböztetésére. Krónikus gyulladás vagy vérzés esetén időnként hemoglobin kristályokat és koleszterin hasadékokat észlelnek.
11.37. Ábra Tubulus pigmentáció, valószínűleg hemosiderin, Fischer F344 patkányban mononukleáris sejt leukémiában (nagy szemcsés limfocita limfóma).
A képek az Egyesült Államok Nemzeti Toxikológiai Programjának jóvoltából.
A mineralizáció kicsi, véletlenszerűen elosztott gócai gyakoriak a kéregben, a medullában és a vese papillájában. Apró, lamellás betonok vagy mikrolitok általában társulnak a tubulusokhoz, de lehetnek intersticiálisak, mindkét típus általában alig vagy egyáltalán nem okoz szöveti választ. Az ásványosított mikrolitok általában pozitívan festenek alizarin-vörös kalcium és von Kossa foszfát esetében, a mátrix pedig pozitívan fest a PAS reakcióval.
A vese mineralizációja általában félszintetikus táplálékkal etetett nőstény patkányokban tapasztalható, de rendszeres laboratóriumi takarmány esetén is megfigyelhető (11.38. Ábra). A kalcium, a foszfor (az étrendben lévő túl sok foszfor), a klorid, a magnézium, a fehérje és a lipid egyensúlyhiányáról beszámoltak, vagy kimutatták, hogy vese mineralizációt okoz. Az mineralizáció súlyossága nemtől és törzstől függ; az ovariectomia megakadályozza a vese mineralizációját, míg az ösztradiol-benzoátot kapó gonadectomizált hímek és nőstények gyorsan kialakulnak a vese mineralizációjában. Mineralizáció figyelhető meg a vesebetegségek egyéb formáival, beleértve a hyalin csepp nephropathiát, a dystrophiás meszesedést és a végstádiumú CPN-betegséget (11.39. És 11.40. Ábra).
11.38. Ábra Tipikus mineralizációs gócok egy nőstény patkányban a külső medulla külső és belső csíkjának találkozásánál.
11.39. Ábra. A papilla lineáris mineralizációja hyalincsepp nephropathia esetén.
A képek az Egyesült Államok Nemzeti Toxikológiai Programjának jóvoltából.
11.40. Ábra. A tubulusok és a GBM-ek ásványosítása egy olyan állatban, amely a CPN végstádiumában pusztult el.
A vesében fokális csontos metapláziát figyeltek meg, amely nem függ össze a vese mineralizációjával (11.41. Ábra). Az inklúziós testeket gyakran megfigyelik a vesében a toxikológiai vizsgálatok során, ahol patogenezisük sokféle lehet. A 110 hetes kezeletlen Wistar Hannover patkányok proximális tubulusaiban a felhalmozódott d-aminosav-oxidáz (DAO) kerek, eozinofil intranukleáris és citoplazmatikus zárványairól számoltak be. A kortikális tubulusokban lévő intracitoplazmatikus és intranukleáris zárványtestekről szintén beszámoltak a noradrenalin/szerotonin újrafelvétel gátlójának Sprague – Dawley patkányokban történő beadását követően. Ezek a zárványok pozitívan festettek a DAO számára. Nyilvánvalóan fajspecifikusak voltak, reverzibilisek, nem nefrotoxikusak és nem relevánsak az emberi biztonsági kockázat értékelésében. A citoplazma magokba történő bekapcsolódása szintén hasonlíthat az intranukleáris zárványokra.
11.41. Ábra. A csontos metaplázia fókusza.
A prozimális tubulus citoplazmában megnövekedett, változó méretű, hialinszerű szerű eozinofil cseppek láthatók, amelyek a lizoszómákat képviselik, és összefüggésbe hozhatók hyalin csepp nephropathiával, CPN-vel, histiocytás szarkómával vagy más neoplazmákkal.
A vese urolithiasis vagy fogkő ritkán fordul elő a patkány medencéjében, bár kisebb, mineralizált konkretiók (vagy mikrolitok) gyakoriak az előrehaladáskor az életkor előrehaladtával (11.42. Ábra). Az urolithiasissal járó veseváltozások közé tartozik a kismedencei urothelium reaktív hiperpláziája, gyulladás, vakuoláris degeneráció és cisztaszerű terek kialakulása az urotheliumban, vérzés és esetenként hidronephrosis. A vese amyloidosis ritka a patkányban.
11.42. Ábra. Egy kis mineralizált kalkulus a vesemedencében a fogak közelében.
Szőlő és mazsola
Michelle S. Mostrom DVM, MS, PhD, DABVT, DABT, a kisállat-toxikológiában (harmadik kiadás), 2013
Bruttó és szövettani elváltozások
Az intakt bazális membránhoz társuló proximális vesetubulus-degenerációt vagy nekrózist, valamint a disztális tekercselt tubulusok kevésbé súlyos degenerációját írják le kutyáknak mazsola és szőlő lenyelését követően. 4-6 A proximális és disztális tubulus regenerációt több esetben figyelték meg, a tubulusos törmelékkel vagy a tubulusokban lévő szemcsés vagy fehérjetartalmú öntvényekkel és a gyűjtőcsatornákkal együtt. A vese tubulusokban bekövetkezett minimális mineralizációról is beszámoltak. Számos mérgezési esetben intracelluláris és intraluminális pigmentet észleltek, amelyek szabálytalan alakúak és aranybarna színűek voltak. Ez a pigment nem festett Von Kossa (kalciumfolt) vagy epefoltokkal, hanem változóan reagált a porosz kékkel (vasfolt). 6 A mérgezett kutyák több esetben vaszkuláris elváltozásai voltak arteritisben, a vastagbél lamina propriában, a szívizomban és az aorta adventitiában. 6.
A húgyúti rendellenességek
Harold C. Schott II. Warwick M. Bayly, a lovak belgyógyászatában (negyedik kiadás), 2018
Enzymuria
A vesetubulusok metabolikusan aktívak, felelősek az anyagok széles körének felszívódásáért vagy kiválasztásáért. Ezeknek a vegyületeknek a transzportját számos enzim segíti elő, amelyek nagy mennyiségben találhatók meg a lizoszómákban a tubuláris hámsejtek belsejében vagy a kefe határain belül. Ezeknek a sejteknek a rendszeres cseréje, valamint az endocitotikus vezikulák és lizoszómák felszabadulása a tubuláris lumenbe az enzimek aktivitását eredményezi a vizeletben (enzymuria). 291 Számos olyan anyagot, amelyet a glomeruluson szűrnek (ideértve az epesavakat, az aminoglikozidot és a cefalosporin antibiotikumokat, a mannitot, a dextránokat, a radiográfiai kontrasztanyagokat és a nehézfémeket), endocitózis útján veszik fel a proximális tubuláris hámsejtekbe. Az endocitotikus vezikulák lizoszómákkal kombinálódnak, és azokat az anyagokat, amelyeket a lizoszomális enzimek nem bontanak le, ezt követően a maradék testek kiürítésével extrudálják a tubulus lumenébe.
A tubuláris hámsejtek gyulladása vagy nekrózisa a lizoszomális és a kefe határ enzimek megnövekedett vizeletaktivitását eredményezi. Mivel a proximális tubuláris hámsejtek metabolikusan a legaktívabbak az összes vesesejt közül, különösen érzékenyek ischaemiás sérülésekre. Továbbá hasonlóan megsérülhetnek a glomeruláris szűrletben lévő nagy mennyiségű nefrotoxin hatásának kitéve. Ennek eredményeként bizonyos vizeletenzimek aktivitásának meghatározása néhány nappal az azotemia kialakulása előtt tubuláris károsodásra utalhat. A megnövekedett vizeletenzim-aktivitás további hozzájárulói közé tartoznak (1) alacsony molekulatömegű enzimek, például amiláz, amelyeket általában a glomerulusok szűrnek és a proximális tubulusokban reabszorbeálnak, (2) postrenalis genitourinary traktus epitheliái, amelyek általában elhanyagolható mértékben járulnak hozzá a vizelet enzimének általános aktivitása (hacsak nem válnak neoplasztikussá), és (3) váladék a kiegészítő nemi mirigyektől. Ez utóbbiak hozzájárulása magyarázza, hogy az intakt hímek miért rendelkeznek nagyobb vizeletaktivitással a laktát-dehidrogenáz (LDH) és az N-acetil-β-d-glükózaminidáz (NAG).
Bár több mint 40 enzimet detektáltak a különböző fajok vizeletében, csak néhánynak tűnik diagnosztikai jelentősége. A klinikai felhasználás érdekében a vizeletenzimnek mérhető aktivitással kell rendelkeznie a vesében; tevékenységének szűk tartományban kell lennie az egészséges állatok vizeletében; elég nagynak kell lennie (molekulatömege nagyobb, mint 60 000), hogy ne szűrődjön szabadon a glomeruluson; és aktivitásának elég korán meg kell nőnie a vesekárosodás során, hogy lehetővé tegye a korrekciós kezelés megkezdését. Végül a vizeletenzim aktivitásának a vizeletben néhány napig meglehetősen stabilnak kell maradnia, különösebb feldolgozás nélkül. Emberekben és kutyákban számos enzim, köztük a NAG, az LDH, a β-glükuronidáz, az alanin-amino-peptidáz, az alkalikus foszfatáz (ALP), a leucin-aminopeptidáz, a γ-glutamil-transzferáz (GGT) és a kallikrein bizonyítottan érzékeny veseműködési indikátorok. kár. A lovak vonatkozásában a GGT, az ALP, a NAG, az LDH és a kallikrein aktivitására vonatkozóan normális értékeket állapítottak meg. 298-302 Az aszpartát-aminotranszferáz és az alanin-aminotranszferáz aktivitásának vizsgálata sikertelen volt a ló normál vizeletében. 299
Elméletileg a kiválasztott enzimek vizeletaktivitásának változásainak értékelése segíthet a klinikusnak abban, hogy azonosítsa a nephron legnagyobb diszfunkciót vagy károsodást szenvedő szegmensét. Bár a NAG, a GGT és az ALP elsősorban a proximális tubuláris hámhoz kapcsolódik, az LDH általában disztális tubuláris hámsejtekhez társul. A vizelet GGT és ALP aktivitásának növekedését kísérleti úton indukálták azokon a lovaknál, akik gentamicint és neomicint kaptak 5-10 napig. 315 316 növekedést mértek hasmenéses, akut hasi krízisekkel és endotoxikus sokkkal járó lovaknál is. Ez utóbbi esetekben az enzimuria feltételezték, hogy az ischaemia után tubuláris károsodást mutat. Öt egymást követő napon a furoszemid beadása a GGT és az ALP aktivitásának mérsékelt növekedését is eredményezte, az ALP gyorsabban növekedett. 311 A 48 órás vízhiány azonban nem váltott ki semmilyen változást a GGT, az ALP vagy az LDH aktivitásában. 302 Hasonlóképpen, a vizelet LDH-aktivitásának változását nem figyelték meg azoknál a lovaknál, akik fenilbutazont (8,8 mg/kg PO) kaptak naponta 6 napon keresztül. 302
Bár a vizelet enzim aktivitásának növekedése általában akut tubulus károsodást jelez, gondosan kell értelmezni a vizelet enzim/Cr arányát. Azokat a küszöbértékeket, amelyek felett a magasság jelentős, még nem dokumentálták jól, bár egy tanulmány arról számolt be, hogy a 25 NE/g-nál nagyobb GGT/Cr-érték tubuláris károsodást jelzett. 298 Ezzel szemben a gentamicin által kiváltott nephrotoxicitás póni kancákban végzett vizsgálatában Hinchcliff és munkatársai 315 a Cr koncentráció növekedésének mérése előtt néhány nappal a 100 IU/g értéket meghaladó GGT/Cr értékeket mértek. Ezenkívül gyakran meg lehet mérni 25 és 100 NE/g közötti GGT/Cr értékeket azoknál a lovaknál, akik gentamicint kapnak ajánlott adagokban. A gentamicin farmakokinetikájához hasonlóan ezeknél a lovaknál is nagyon változó volt az enzimuria; ezeknél a lovaknál nem ismerték az akut veseelégtelenség kialakulásának kockázatát. Bár az enzymuria valószínűleg a tubuláris károsodás bizonyos fokát tükrözi ezeknél a betegeknél, óvatosan kell értelmezni a GGT/Cr értékek 25 és 100 NE/g közötti növekedését, míg a 100 NE/g feletti növekedés nagyobb valószínűséggel klinikailag jelentős.
A krónikus vesebetegségben szenvedő lovak normális vagy csökkent enzimaktivitást mutathatnak, amelyek a nefronban krónikus gyulladásra válaszul bekövetkező sejtszintű változásokat tükrözik. Ahogy a BUN és a Cr koncentrációja normális lehet a vesebetegség korai szakaszában; a vizeletenzim-aktivitás nem feltétlenül tükrözi pontosan a veseműködési rendellenességet a betegség későbbi szakaszában, amikor a vérvizsgálatok és a vizeletvizsgálat eredményei valószínűleg kórosabbak. Ennek a jelenségnek egyik lehetséges oka az, hogy a tubuláris hám jelentős megsemmisülése a betegség korai szakaszában kevesebb hámsejtet eredményez, amely az enzimaktivitás fokozott aktivitásának folyamatos forrása lehet. Alternatív megoldásként a regeneráló tubuláris hámsejtek jobban ellenállhatnak a toxin hatásainak.
- Nem fertőző betegség - áttekintés a ScienceDirect témákról
- Prosztata Adenoma - áttekintés a ScienceDirect témákról
- Hasnyálmirigy-lé - áttekintés a ScienceDirect témákról
- Csipkebogyó - áttekintés a ScienceDirect témákról
- Paralytic Ileus - áttekintés a ScienceDirect témákról