Az étkezési gyakoriság csökkentése kalóriakorlátozás nélkül a glükózszabályozásra egészséges, normál testsúlyú, középkorú férfiaknál és nőknél
Olga Carlson
1 Diabetes szekció, Klinikai Vizsgálati Laboratórium, Országos Öregedési Intézet Intramural Research Program, Baltimore, MD
Bronwen Martin
2 Idegtudományi Laboratórium, Országos Öregedési Intézeti Kutatási Program, Baltimore, MD
Kim S. Stote
3 Beltsville Humán Táplálkozási Kutatóközpont, Amerikai Mezőgazdasági Minisztérium, Mezőgazdasági Kutatási Szolgálat, Beltsville, MD
Erin Golden
2 Idegtudományi Laboratórium, Országos Öregedési Intézet Intramural Research Program, Baltimore, MD
Stuart Maudsley
2 Idegtudományi Laboratórium, Országos Öregedési Intézet Intramural Research Program, Baltimore, MD
Samer S. Najjar
4 Szív- és érrendszeri tudomány laboratórium, Országos Öregedési Intézet Intramural Research Program, Baltimore, MD
Luigi Ferrucci
5 Klinikai kutatási részleg, Országos Öregedési Intézet Intramural Research Program, Baltimore, MD.
Donald K. Ingram
6 Kísérleti gerontológiai laboratórium, Országos Öregedési Intézet Intramural Research Program, Baltimore, MD
Dan L. Longo
7 Immunológiai Laboratórium, Országos Öregedési Intézet Intramural Research Program, Baltimore, MD
William V. Rumpler
3 Beltsville Humán Táplálkozási Kutatóközpont, Amerikai Mezőgazdasági Minisztérium, Mezőgazdasági Kutatási Szolgálat, Beltsville, MD
David J. Baer
3 Beltsville Humán Táplálkozási Kutatóközpont, Amerikai Mezőgazdasági Minisztérium, Mezőgazdasági Kutatási Szolgálat, Beltsville, MD
Josephine Egan
1 Diabetes szekció, Klinikai Vizsgálati Laboratórium, Országos Öregedési Intézet Intramural Research Program, Baltimore, MD
Mark P. Mattson
2 Idegtudományi Laboratórium, Országos Öregedési Intézeti Kutatási Program, Baltimore, MD
Absztrakt
1. Bemutatkozás
A glükóz intolerancia és az inzulinrezisztencia a 2-es típusú cukorbetegség kiemelkedő jellemzője [1], és a glükóz tolerancia finomabb romlása növelheti a cukorbetegség, a szív- és érrendszeri betegségek és a stroke kockázatát [2, 3]. Az egyébként egészséges egyének ilyen „pre-diabéteszes” állapotait az éhomi vércukorszint és az inzulinszint mérsékelt emelkedése, valamint az orális glükóztolerancia tesztben (OGTT) a plazma glükóz- és inzulinszintjének időbeli profilja jellemzi, a glükózszint és késleltetett inzulinválasz [4–6]. A csontvázizomsejtek csökkent inzulinérzékenysége és a hasnyálmirigy béta-sejtjeinek csökkent reakciókészsége hozzájárul a glükóz tolerancia romlásához [7].
Az adipokinek a zsírsejtek által táplálkozásra vagy éhgyomorra termelt hormonok, amelyek fontos szerepet játszhatnak az elhízás és a cukorbetegség kialakulásában [1]. Például a keringő leptin szintje megnövekszik elhízott és cukorbetegeknél, és a leptin rezisztencia a hipotalamusz sejtekben, amelyek általában elnyomják a táplálékfelvételt, valószínűleg hozzájárul a túlevéshez ilyen körülmények között [8, 9]. Elhízott és inzulinrezisztens személyeknél a keringő adiponektin szintje alacsony, az ellenállás szintje pedig megemelkedik [10]. Az adipokinek változásainak szerepe a glükóz metabolizmus károsodásában azonban nem világos. Az inzulin és az adipokinek mellett az agyból származó neurotróf faktor (BDNF) közelmúltban felvetődött, hogy szerepet játszik a glükóz metabolizmusában. A BDNF heterozigóta knockout egerek [11], elhízott és cukorbeteg állatok, akiknek BDNF-et adtak [12, 13] és a 2-es típusú cukorbetegségben szenvedő emberek [14] vizsgálata arra utal, hogy a BDNF jelátvitel fokozza az inzulinérzékenységet. A BDNF antidiabetikus hatását emberben javasolja egy nemrégiben készült tanulmány, amely fordított összefüggést mutatott ki az éhgyomri plazma BDNF-szint és a glükózszint között, de nem az inzulinszint között [14]. Az étrendi energiafogyasztás variációinak hatása a BDNF szintre emberben azonban nem ismert.
2. Tantárgyak és módszerek
Tantárgyak és tanulmánytervezés
A tantárgy jellemzőinek és a tanulmány tervezésének részleteiről korábban beszámoltunk [29]. Röviden: az alanyok egészséges, 40-50 éves férfiak és nők voltak, testtömeg-indexük 18 és 25 kg/m 2 között volt, és a szokásos étkezési szokásuk napi háromszori étkezés volt. A tanulmányba való belépést orvos jóváhagyta kórtörténet, vér- és vizeletvizsgálati eredmények szűrése, valamint fizikális vizsgálat alapján. A protokollt a Johns Hopkins Egyetem Humánkutatási Bizottsága és a MedStar Kutatóintézet Intézményi Felülvizsgálati Testülete hagyta jóvá. Valamennyi alany megadta a tájékozott beleegyezését, és kompenzációt kapott a vizsgálatban való részvételükért. Minden alany két 8 hetes ellenőrzött étrenden esett át, amelyek során az összes kalóriát elfogyasztotta a testsúly fenntartása érdekében, napi 3 étkezés (reggeli, ebéd és vacsora) vagy 1 étkezés/nap (kora este 4 órás időszak alatt); 16:00 - 20:00 óra), randomizált keresztezéssel, 11 hetes diétán kívüli periódussal a két kontrollált étrendi időszak között. A kísérleti étrendben a reggeli és ebéd ételeket helyettesítették a hagyományos esti ételekkel; a diéták összetételéről korábban beszámoltak (28). Az energiafogyasztást szükség szerint módosították az állandó testsúly fenntartása érdekében a vizsgálat során.
Glükóz tolerancia teszt és hormonszint mérések
Az inzulinérzékenység kiszámítása
Számszerűsítettük az inzulinérzékenységet az inzulinrezisztencia homeosztatikus modelljének (HOMAIR) kiszámításával, az éhomi plazma glükóz- és inzulinszintek felhasználásával [31]. Kiszámítottuk az inzulinérzékenységi indexet (ISI), a metabolikus clearance sebességét (MCR), a β-sejt funkcióját az első fázis szekréciója során (β-sejt funkció, első fázis) és a második fázis szekrécióját β-sejt funkció, a második fázis). mint orális glükóz-inzulin érzékenység (OGIS: 0, 90 [a 80 és 100 perc átlagának átlaga] és 120) [32–35].
Statisztikai analízis
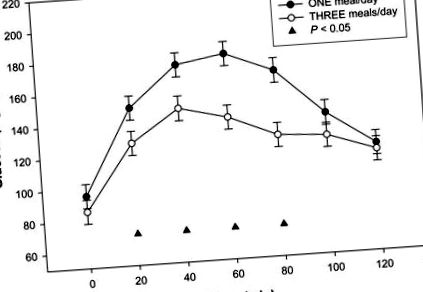
Plazma glükózkoncentrációk az orális glükóz tolerancia tesztek során minden vizsgálati időszakban. Az adatokat úgy mutatjuk be, hogy a legkisebb négyzetek átlagai ± SEM, n = 15 (10 nő, 5 férfi), egy ismételt ANOVA-mérés alapján. Jelentős kezelési hatás volt az 1 étkezés/nap (●) és a 3 étkezés/nap (○) között az OGTT esetében 20, 40, 60 és 80 percnél, ▲ P ¹
| Glükóz mg/dl | 95,9 ± 1,7 | 85,4 ± 1,7 | 0,0002 |
| ΜU/ml inzulin | 5,0 ± 0,7 | 5,8 ± 0,7 | 0,4329 |
| Glükagon pg/ml | 66,5 ± 7,7 | 62,1 ± 7,4 | 0,6878 |
| HOMA-IR | 1,2 ± 0,2 | 1,3 ± 0,2 | 0.8718 |
| OGIS | 403,4 ± 14,0 | 458,8 ± 13,9 | 0,0114 |
| ISI | 0,1 ± 0,004 | 0,1 ± 0,004 | 0.6552 |
| MCR | 8,8 ± 0,3 | 9,2 ± 0,3 | 0,4011 |
| β-sejt funkció 1. fázis | 782,1 ± 66,0 | 1013,85 ± 66,1 | 0,0209 |
| β-sejt funkció 2. fázis | 239,0 ± 19,0 | 253,7 ± 19,0 | 0,5894 |
| Adiponektin pg/ml | 13,5 ± 1,3 | 13,5 ± 1,3 | 0,9919 |
| Rezisztin ng/ml | 3,1 ± 0,3 | 2,8 ± 0,2 | 0,4147 |
| Leptin ng/ml | 20,2 ± 2,2 | 16,1 ± 2,1 | 0,18 |
| Ghrelin pg/ml | 163,2 ± 12,8 | 158,4 ± 12,8 | 0,7942 |
| BDNF ng/ml | 141,7 ± 26,7 | 148,1 ± 26,6 | 0,8175 |
Az étkezés gyakoriságának nem volt szignifikáns hatása a HOMA-IR-re, ISI-re vagy MCR-re (1. táblázat). Az OGIS-értékek azonban szignifikánsan alacsonyabbak voltak az alanyokban, amikor 1 étkezés/nap, 3 étkezés/nap értékkel szemben (1. táblázat). Ezen túlmenően, amikor 1 étkezés/nap alkalmával a β-sejtfunkció 1. fázisának értékei szignifikánsan alacsonyabbak voltak, mint a 3 étkezés/nap értékek (1. táblázat). A diéta nem befolyásolta szignifikánsan a β-sejt funkció 2. fázisának értékeit.
Annak érdekében, hogy tovább tisztázzuk az étkezés gyakoriságának a kalória-korlátozás nélküli hatásait az energia-anyagcserére, több adipokin éhomi szintjét mértük, amelyekről ismert, hogy fontos szerepet játszanak az energiaegyensúly szabályozásában. Az éhomi plazma ghrelin-koncentráció hasonló volt az alanyokban, ha 1 étkezés/nap vagy 3 étkezés/nap volt (1. táblázat). Az OGTT során az étrendnek nem volt szignifikáns hatása a plazma ghrelin-koncentrációra, bár a szintek általában alacsonyabbak voltak az alanyokban, amikor 1 étkezés/nap adagot kaptak a glükóz bevétele után 40 és 100 perc között (3. ábra). Az étrendnek nem volt szignifikáns hatása a glükagon, a leptin, az adiponektin, a rezisztin és a BDNF reggeli plazmakoncentrációjára (1. táblázat).
A plazma ghrelin koncentrációja az orális glükóz tolerancia tesztek során minden vizsgálati időszakban. Az adatokat úgy mutatjuk be, hogy a legkisebb négyzetek átlagai ± SEM, n = 15 (10 nő, 5 férfi), egy ismételt ANOVA-mérés alapján. Az orális glükóztolerancia teszt során az 1 étkezés/nap (●) és a 3 étkezés/nap (○) között nem volt szignifikáns kezelési hatás a plazma ghrelin-koncentrációra.
4. Megbeszélés
A reggeli glükóztolerancia romlásának oka nem egyértelmű az 1 étkezést naponta fogyasztó alanyokban a 3 étkezés/nap étkezéshez képest. Beszámoltak arról, hogy az éhomi inzulin, leptin és glükagon koncentrációja emelkedett a csökkent glükóztolerancia esetén [36, 37]. Azonban a diéta nem gyakorolt jelentős hatást az utóbbi hormonok koncentrációjára ebben a vizsgálatban. Hasonlóképpen, az étkezési gyakoriságnak nem volt szignifikáns hatása a ghrelin, az adiponektin, az rezisztin vagy a BDNF plazmaszintjére. Így, bár az éhomi inzulin és az adipokin szintje nem különbözött a két étrendcsoport között, az inzulinérzékenység nyilvánvalóan csökkent az alanyokban, amikor 1 ételt/nap fogyasztottak. Valójában az OGIS és az 1. fázisú β-sejt funkció értékei szignifikánsan alacsonyabbak voltak az alanyokban, amikor 1 étkezést fogyasztottak naponta, összehasonlítva az alapértékkel, a napi 3 étkezéssel és a diétán kívüli értékekkel. Ez utóbbi eredmények az inzulinérzékenység és a hasnyálmirigy β-sejtes inzulinválaszainak relatív károsodására utalnak az alanyokban 1 étkezés/nap adagban, 3 étkezés/nap arányban.
Az OGTT-ket reggel hajtották végre. Ezért amikor az 1 étkezés/nap diéta alatt az alanyok sokkal nagyobb mennyiségű ételt fogyasztottak az OGTT közelében, mint a 3 étkezés/nap dózisban, ez befolyásolhatta a reggeli inzulinérzékenységet. Sőt, a glükóz tolerancia cirkadián változásait úgy dokumentálták, hogy a tolerancia a legjobb reggel [38]. Ha nem szokták meg a reggeli étkezést, majd reggeli OGTT-nek vetik alá, az 1 étkezés/nap étkezési alanyok gyengébb glükóz toleranciát mutathatnak, mint a reggeli étkezéshez alkalmazkodók. A nyugatiasodott társadalom jelenlegi étkezési módja, hogy este a legnagyobb ételt fogyasztja, rosszul alkalmazkodó életmódnak tűnik.
Köszönetnyilvánítás
Ezt a kutatást az Országos Öregedési Intézet intramurális kutatási programja támogatta. Köszönjük K. Spears technikai segítségét.
Lábjegyzetek
Kiadói nyilatkozat: Ez egy szerkesztetlen kézirat PDF-fájlja, amelyet kiadásra elfogadtak. Ügyfeleink számára nyújtott szolgáltatásként a kéziratnak ezt a korai változatát biztosítjuk. A kézirat átmásolásán, szedésén és a kapott bizonyíték felülvizsgálatán átesik, mielőtt a végső hivatkozható formában közzétennék. Felhívjuk figyelmét, hogy a gyártási folyamat során olyan hibákat fedezhetnek fel, amelyek befolyásolhatják a tartalmat, és a naplóra vonatkozó minden jogi felelősségvállalás vonatkozik.
- Azt; Bizonyítottan étkezési idõink hatással vannak a Web24 Hírek súlygyarapodására
- Mesomorph étkezési terv egészséges táplálkozás SF kapu
- Hogyan befolyásolja a kávé a fogyást, a kávé egészséges fitnesz turmixgép
- Joy Bauer; s 7 napos étkezési terv egy egészséges hétre
- Fogyjon le ezzel az egészséges étkezési tervvel a női fitnesz edzőtől