Patkány krónikus vesebetegsége
Gregory F. Grauer, DVM, MS, diplomata ACVIM (kisállati belgyógyászat)
Kansas Állami Egyetem
A krónikus vesebetegség (CKD) az összes macskának körülbelül 1–3% -át érinti. 1 Ez a macskák elhullásának fontos oka hónapok vagy évek alatt alakul ki. Az ezzel járó nephron károsodás progresszív és irreverzibilis, annak ellenére, hogy néhány CKD-s macskának hónapokon át évekig stabil a szérum kreatinin-koncentrációja.
A korai CKD diagnózisa, amelyet megfelelő kezelés követ, javíthatja a túlélést. Ott
szilárd bizonyíték arra, hogy az étrendi kezelések és egyre több bizonyíték arra, hogy az antiproteinurikus kezelések lassíthatják a CKD progresszióját.
PROFIL
A macska CKD előfordulása az életkor előrehaladtával növekszik; a 15 évnél idősebb macskák 30-50% -ának van CKD-je. A CKD 2–4 gyakorisága a hím és nőstény macskákban hasonló, de a hím macskákat gyakran fiatalabb korban diagnosztizálják, mint a nőstény macskákat. 5 Bizonyos fajták felülreprezentáltnak tűnnek, köztük a Maine Coon, az abesszin, a sziámi, a burmai és az orosz kék. 4
ETIOLÓGIA
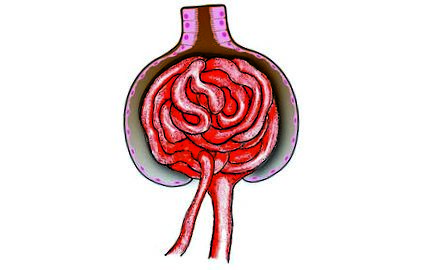
A macska CKD okát általában nehéz meghatározni. A nephron vaszkuláris és tubuláris komponenseinek kölcsönös függősége miatt az irreverzibilis glomeruláris vagy tubuláris károsodás végpontja megegyezik: a nephronok rostos hegszövetének pótlása (1.ábra).
1. ÁBRA CKD-s macska vese szövettani képe. Vegye figyelembe a rostos hegszövet pótlását (nyilak); és mononukleáris sejtek beszivárognak.
A nefronok közötti morfológiai heterogenitás a krónikusan beteg vesében létezik, a változások a súlyos atrófiától a kifejezett hipertrófiáig terjednek. A szövettani változások nem folyamatspecifikusak, ezért etiológiai diagnózist gyakran nem állapítanak meg. A leggyakoribb szövettani diagnózis a krónikus tubulointerstitialis nephritis. 6.
PATHOPHIOLÓGIA
A CKD kórélettana mind szervi, mind szisztémás szinten megfontolható.
Csökkent glomeruláris szűrés
A vese szintjén az alapvető rendellenesség a nephronok elvesztése és a csökkent glomeruláris szűrés. A csökkent glomeruláris szűrés megnöveli azoknak az anyagoknak a plazmakoncentrációját, amelyek normálisan vesekiválasztással ürülnek ki a szervezetből.
Hormonális zavarok
Az anyagcsere-hulladékok kiválasztásán és a folyadék- és elektrolit-egyensúly fenntartásán túl a vesék endokrin szervként működnek, és számos peptidhormont katabolizálnak. Ezért a hormonális zavarok a CKD-vel összefüggő multisystem rendellenességek patogenezisének részét képezik. Például az eritropoietin csökkent termelése hozzájárul a CKD nonregeneratív vérszegénységéhez, a parathormon csökkent metabolizmusa és kiválasztódása pedig az osteodystrophiához.
Kompenzációs mechanizmusok
Végül a CKD patofiziológiájának egy részét kompenzációs mechanizmusok hozzák létre. Az intakt nephronok egyéni glomeruláris szűrési sebessége (GFR) növekszik a megfelelő vesefunkció fenntartása érdekében; a proteinuria és a glomerulosclerosis azonban ennek a hiperszűrésnek a következményei vagy „kompromisszumai” lehetnek (2. ábra). CKD-ben a renális véráramlás autoregulációja elvész, és az egyetlen nephron GFR az elveszített nephronok számával arányosan növekszik. Az így megnövekedett intraglomeruláris nyomás károsítja a glomeruláris kapilláris falat és növeli a plazmafehérje-szűrést, ami későbbi glomeruláris és tubulointerstitialis károsodásokhoz vezet.
2. ÁBRA A nephronok progresszív veszteségének lehetséges mechanizmusai CKD-ben. Mal Hoover Rooks, CMI, Kansas Állami Egyetem jóvoltából
A FELINE CKD ÁTALAKÍTÁSA
A vesebetegség és a csökkent vesefunkció leírására sokféle kifejezést használtak, és sajnos ezek a kifejezések zavaróak lehetnek a standard meghatározások és az alkalmazás hiánya miatt.
Vesebetegség vagy veseelégtelenség: melyik kifejezést kell használni?
A krónikus veseelégtelenség kifejezés előnyben részesíti a krónikus veseelégtelenséget, mivel a CKD veseelégtelenség nélkül is fennállhat, és az ügyfelek gyakran csüggedten érzik magukat, amikor a diagnózis magában foglalja a „meghibásodás” kifejezést. Veseelégtelenség - amelyet a tartós vese azotémia határoz meg, amely a vizelet koncentrálására való képtelenségre épül - akkor következik be, amikor mindkét vese nefronjainak legalább 75% -a nem működik.
Az IRIS-t (iris-kidney.com) azért hozták létre, hogy elősegítse a kisállatok vesebetegségének tudományos megértését, és különösen, hogy segítse a szakembereket a kutyák és macskák vesebetegségének jobb diagnosztizálásában, megértésében és kezelésében.
Az IRIS iránymutatásokat dolgozott ki (2. táblázat–4) - amelyet az amerikai és európai állatorvosi nephrológiai és urológiai társaságok fogadtak el - stabil macska CKD rendezésére annak érdekében, hogy:
- Javítani kell a kommunikációt a CKD-vel kapcsolatban
- Kapcsolja össze a megfelelő diagnosztikai és terápiás erőfeszítéseket a különböző mértékű CKD-vel rendelkező betegekkel.
| 3. TÁBLÁZAT. IRIS irányelvek: A macska CKD osztályozása a vizelet fehérje és a kreatinin arány szerint | |
| OSZTÁLYOZÁS | UPC RATIO |
| Nem fehérje | 0.4 |
| 4. TÁBLÁZAT. IRIS irányelvek: A macska CKD osztályozása szisztolés vérnyomás alapján | ||
| ARTERIÁLIS NYOMÁSKATEGÓRIA | SZISZTOLÉS VÉRNYOMÁS (Hgmm) | A CÉLSZERV SZÉRÜLÉSÉNEK KOCKÁZATA |
| AP0 | 180 | Magas |
Szérum kreatinin koncentráció
A vázlatos rendszert vázolta fel 2. táblázat addig nem alkalmazzák, amíg a CKD jelenlétét meg nem erősítik. Ez a rendszer, amely a vesebetegségeket a 4 szakasz egyikébe sorolja, a jól hidratált, stabil CKD-s macskák szérum kreatinin-koncentrációján alapul; a stabilitást 2 glomeruláris tartományú proteinuria javasolja, ami macskákban ritkán fordul elő kutyákkal összehasonlítva. Fontos felismerni, hogy ez az arány nem különbözteti meg a vese proteinuriáját az alsó húgyúti gyulladással járó proteinuria-tól; a klinikusnak meg kell különböztetnie a proteinuriát a vizelet üledékének felmérésével.
Szisztolés vérnyomás
A szisztolés vérnyomást tipikusan Doppler-módszerrel mérik macskáknál. Az IRIS vérnyomás alrendszere a célszerv károsodásának (szem, agy, szív és vese) kockázatán alapul. A legtöbb klinikus a szisztolés hipertóniát 160 Hgmm-nél nagyobb szisztolés vérnyomásnak tekinti, és ezen a ponton kezdik meg a kezelést.
KLINIKAI JELEK ÉS DIAGNÓZIS
Klinikai jelek
A CKD klinikai tünetei korai stádiumban nem jelentkezhetnek, és ha a későbbi szakaszokban jelentkeznek, általában nem specifikusak, például letargia, gyengeség, anorexia, hányás és dehidráció. Időnként urémiás lélegzet vagy szájüregi fekélyek figyelhetők meg. A CKD egyedi tünetei (szemben az akut vese sérüléssel) a fogyás és a polydipsia/polyuria régóta fennálló kórtörténete, a rossz testállapot, a kicsi és szabálytalan vesék, valamint a vese másodlagos hyperparathyreoidizmusa.
Diagnosztikai eredmények
A veseelégtelenség klasszikus diagnózisa, amely a vese azotémián alapul (a vizelet koncentrálására való képtelenségre ráhúzódó perzisztens azotemia) a CKD 2–4. Szakaszára vonatkozik. Néhány vese azotémiás macskában megmarad a hipersthenurikus vizelet előállításának képessége (USG> 1,035) esetekben a folyadékterápiára adott válasz segít a prerenalis versus vese azotemia diagnosztizálásában.
Az 1. stádiumú CKD az alábbiak alapján diagnosztizálható:
- Kóros vese tapintás vagy ultrahangos/radiológiai eredmények
- Tartós vese proteinuria
- A vesebetegség miatti vizeletkoncentrációs hiány
- A szérum kreatininszint növekedése az idő múlásával, még akkor is, ha az értékek a normális tartományban maradnak.
Például egy szérum kreatinin-koncentráció, amely 0,6-ról 1,2 mg/dl-re növekszik több év alatt, a GFR legalább 50% -os csökkenését jelezheti (a nephronok legalább 50% -os csökkenése, mert a fennmaradó nephronok kompenzációs hipertrófiája növeli funkcionális képességüket).
Szérum szimmetrikus dimetilarginin
A szérum szimmetrikus dimetilarginin (SDMA) egy új vesefunkciós marker, amely segíthet a macskák CKD korai diagnózisában. Egy nemrégiben végzett, CKD-t mutató macskákon végzett longitudinális vizsgálatban az SDMA-koncentráció a normál érték fölé nőtt körülbelül 17 hónappal azelőtt, hogy a szérum kreatinin-koncentrációja meghaladta a referencia-tartományt (> 2,1 mg/dL). 8 Megjegyzendő, hogy ha ebben a vizsgálatban a szérum kreatinin-koncentrációt ≥ 1,6 mg/dl rendellenesnek tekintették, akkor mind a szérum kreatinin, mind az SDMA közel azonos időben azonosította volna a vese azotémiáját.
A Feline CDK diagnosztikai megközelítése
Általánosságban elmondható, hogy a betegek diagnosztikai megközelítése a CKD azonosítása és stádiumba állítása után 3 területre összpontosít (5. táblázat):
1. Az elsődleges vesebetegség jellemzése és/vagy a betegség folyamatainak bonyolítása
2. A vesebetegség és a működés stabilitásának jellemzése
3. A csökkent vesefunkcióval járó betegproblémák értékelése
A vesebetegség további meghatározása (a teljes vérképen, a szérum biokémiai profilján és a teljes vizeletvizsgálaton túl) a következőket tartalmazza:
• A proteinuria mennyiségi meghatározása
• A vérnyomás mérése
• Vizeletkultúra
• Húgyúti képalkotás röntgenfelvételekkel és ultrahanggal
A vesefunkció stabilitása a vesebetegség kezdeti jellemzése során azonosított rendellenességek soros monitorozásával értékelik. Ennek az ellenőrzésnek mindig tartalmaznia kell:
• Szérum biokémiai profil
• vizeletvizsgálat
• A proteinuria mennyiségi meghatározása
• A vérnyomás mérése
A monitorozás vizeletkultúrák és ultrahangvizsgálatokat is tartalmazhat.
A vesebetegség további meghatározása A legfontosabb a CKD korábbi szakaszaiban, amikor az alapbetegség vagy a betegség szövődményének korrekciója képes a legnagyobb mértékben javítani vagy stabilizálni a vesefunkciót.
A betegség stabilitásának jellemzése A legfontosabb a CKD korábbi szakaszaiban, amikor a megfelelő kezelés a legnagyobb mértékben képes a veseműködés stabilizálására.
A beteg problémáinak jellemzése a CKD későbbi szakaszaiban válik fontosabbá, amikor a klinikai tünetek általában súlyosabbak. Ebben az esetben a diagnosztikai (és az azt követő terápiás) erőfeszítéseket a beteg problémáira kell irányítani, beleértve az étvágytalanságot, hányást, dehidrációt, acidózist, káliumhiányt és vérszegénységet.
Terápiás megközelítés
Hasonló a CKD diagnosztikai megközelítéséhez (lásd A macskák CKD diagnosztikai megközelítése), a terápiás megközelítést a beteg betegség stádiumához kell igazítani (5. táblázat).
Például a CKD korábbi szakaszaiban a nephrolithok és a bakteriális pyelonephritis betegségspecifikus kezelése, valamint a vesebetegség progressziójának lassítására tervezett kezelések (renoprotektív kezelések) nyújtják a legnagyobb értéket. A renoprotektív kezelések közé tartozik az étrend megváltoztatása, amely csökkenti a szérum foszforkoncentrációját 9 és csökkenti a lágyrész mineralizációját3. ábra).
A proteinuria fontos kockázati tényező az azotemia kialakulásában és progressziójában, valamint a macskák túlélésének csökkenésében. 10-13 Angiotenzin-konvertáló enzim inhibitorokat és kalciumcsatorna blokkolókat használnak a proteinuria csökkentésére, valamint a szisztémás és intraglomeruláris vérnyomás normalizálására. 14-16
A CKD későbbi szakaszaiban a kezelés általában a csökkent vesefunkcióval járó klinikai tünetek korlátozására összpontosít.
Figyelje meg a túlélés fokozatos csökkenését a CKD stádium növekedésével: 1151 nap a 2.b stádiumú macskáknál (ami magasabb lenne, ha az összes 2. stádiumú macskát beleszámítanák), szemben a 679 nappal a 3. stádiumú macskáknál és 35 nappal a 4. stádiumú macskáknál. Ez a tendencia nem meglepő, de a tényleges számok megkönnyítik a jobb prognosztikát és hangsúlyozzák a korai diagnózist.
CKD = krónikus vesebetegség; GFR = glomeruláris szűrési sebesség; IRIS = Nemzetközi Renal Interest Society; SDMA = szérum szimmetrikus dimetilarginin; USG = vizelet fajsúly
Hivatkozások
1. Brown SA. A kezelés összekapcsolása a krónikus vesebetegség stádiumával. Augusztusban JR (szerk.): Konzultációk a macska belgyógyászatában. St. Louis: Elsevier Saunders, 2010, 475-482.
2. Polzin DJ, Osborne CA, Adams LG, Lulich JP. A macska krónikus veseelégtelenségének orvosi kezelése. In Kirk RW, Bonagura JD (szerk.): Kirk jelenlegi állatorvosi terápiája XI. Philadelphia: Saunders, 1992, 848-853.
3. Ross SJ, Polzin DJ, Osborne CA. A korai krónikus veseelégtelenség klinikai progressziója és következményei a kezelésre. Augusztusban JR (szerk.): Konzultációk a macska belgyógyászatában. St Louis: Elsevier Saunders, 2005, 389–398.
4. Lulich JP, Osborne CA, O’Brien TD és mtsai. Macskaveseelégtelenség: Kérdések, válaszok, kérdések. Compend Cont Educ Pract Vet 1992; 14, 127-153.
5. White JD, Norris JM, Baral RM és mtsai. Természetesen előforduló krónikus vesebetegség ausztrál macskáknál: 184 eset prospektív vizsgálata. Aust Vet J 2006; 84, 188-194.
6. DiBartola SP, Rutgers HC, Zack PM, Tarr MJ. Krónikus vesebetegséggel járó klinikopatológiai leletek macskáknál: 74 eset (1973-1984). JAVMA 1987; 190, 1196-1202.
7. Lees GE, Brown SA, Elliott J és mtsai. A proteinuria értékelése és kezelése kutyákban és macskákban; 2004 ACVIM fórum konszenzusos nyilatkozata (kis állat). J Vet Intern Med 2005; 19: 377-385.
8. Hall JE, Yerramilli M, Obare E és mtsai. A szimmetrikus dimetilarginin és kreatinin szérumkoncentrációinak összehasonlítása vesefunkció biomarkerként krónikus vesebetegségben szenvedő macskáknál. J Vet Intern Med 2014; 28: 1676-1683.
9. Polzin DJ, Osborne CA, Ross S és mtsai. A macska krónikus veseelégtelenségének diétás kezelése. Hol tartunk most? Milyen irányba tartunk? J Feline Med Surg 2000; 2: 75-82.
10. Chakrabarti S, Syme HM, Elliott J. Az azotemia progresszióját előrejelző klinikopatológiai változók krónikus vesebetegségben szenvedő macskákban. J Vet Intern Med 2012; 26: 275-281.
11. Jepson R, Brodbelt D, Vallance C és mtsai. Az azotemia kialakulásának előrejelzőinek értékelése macskáknál. J Vet Intern Med 2009; 23: 806-813.
12. Syme HM, Markwell PJ, Pfeiffer D és mtsai. A természetben előforduló krónikus veseelégtelenségben szenvedő macskák túlélése a proteinuria súlyosságával függ össze. J Vet Intern Med 2006; 20: 528-535.
13. King JN, Tasker S, Gunn-Moore DA, Strehlau G. Prognosztikai tényezők krónikus vesebetegségben szenvedő macskákban. J Vet Intern Med 2007; 21: 906-916.
14. King JN, Gunn-Moore DA, Tasker S és mtsai. A benazepril tolerálhatósága és hatékonysága krónikus vesebetegségben szenvedő macskáknál. J Vet Intern Med 2006; 20: 1054-1064.
15. Mizutani H, Koyama H, Watanabe T és mtsai. A benazepril klinikai hatékonyságának értékelése macskák krónikus veseelégtelenségének kezelésében. J Vet Intern Med 2006; 20: 1074-1079.
16. Jepson RE, Elliott J, Brodbelt D, Syme HM. A szisztolés vérnyomás szabályozásának hatása a szisztémás magas vérnyomásban szenvedő macskák túlélésére. J Vet Intern Med 2007; 21, 402-409.
17. Boyd LM, Langston C, Thompson K és mtsai. Túlélés természetesen előforduló krónikus vesebetegségben szenvedő macskáknál (2000-2002). 2008; 22: 1111-1117.
Gregory F. Grauer, DVM, MS, Diplomate ACVIM (kisállati belgyógyászat), a Kansas Állami Egyetem Állatorvostudományi Főiskolájának Klinikai Tudományok Tanszékének professzora és Jarvis orvostan elnöke. Dr. Grauer klinikai és kutatási érdekeltségei a kisállatok vizeletürítési rendszerét érintik, az IRIS és az American Veterinary Nephrology and Urology Society igazgatótanácsában van. Dr. Grauer a Colorado Állami Egyetemen szerzett belgyógyászati posztgraduális képzést. A Wisconsini Egyetem Állatorvostudományi Karának és a Colorado Állami Állatorvosi Főiskola oktatója volt.
- Macskák allergiás bőrbetegségének kezelése Állatorvosi gyakorlat
- Macskás vesebetegség - Metropolitan Veterinary Associates
- Étrendi nátrium krónikus vesebetegségben Átfogó megközelítés
- Krónikus vesebetegségi étrend-terv Harbour Light Hospice
- Krónikus vesebetegség (CKD) szakaszában tünetek; Kezelés