A magas sótartalom a magas zsírtartalmú étrend mellett fokozhatja az egerek oxidatív stresszének és diszlipidémiájának indukálta máj steatosis gyulladását és fibrózisát
Absztrakt
Háttér
Széles körben ismert, hogy a só gyorsítja a metabolikus szindróma előrehaladását, és szív- és érrendszeri betegségeket okoz, valószínűleg prooxidáns tulajdonságainak köszönhetően. Feltételeztük, hogy a túlzott sóbevitel megkönnyíti az alkoholmentes steatohepatitis (NASH) kialakulását is, amely gyakran társul metabolikus szindrómához.
Mód
Megvizsgáltuk a magas sótartalmú étrend fokozott hatását a magas zsírtartalmú étrend okozta májkárosodásra, az oxidatív stresszre, az apoE kiütésre és a lektinszerű oxidált kis sűrűségű lipoprotein receptor-1 (LOX-1) transzgénikus egerekre fogékony modellben.
Eredmények
A magas sótartalmú étrend NASH-hoz vezetett a magas zsírtartalmú étrenddel táplált LOX-1 transzgénikus/apoE knockout egerekben anélkül, hogy befolyásolta volna a magas zsírtartalmú étrend okozta diszlipidémiát vagy a máj triglicerid felhalmozódását. Ezenkívül a magas sótartalmú és magas zsírtartalmú étrend nagyobb mértékben stimulálta az oxidatív stressz kialakulását és a gyulladásos reakciókat, mint a magas zsírtartalmú étrend a LOX-1 transzgénikus/apoE knockout egerek májában.
Következtetések
Kimutattuk, hogy a magas sótartalmú étrend súlyosbította a NASH-t a magas zsírtartalmú, táplálékkal táplált LOX-1 transzgénikus/apoE knockout egerekben, és hogy ez a hatás összefüggésbe hozható az oxidatív és gyulladásos folyamatok stimulálásával; ez az első tanulmány, amely a túlzott sóbevitel fontos szerepét sugallja a NASH kialakulásában.
Háttér
A nem alkoholos steatohepatitis (NASH) a közelmúltban vonzza magára a figyelmet növekvő prevalenciája és szoros összefüggései miatt krónikus betegségekkel, például cukorbetegséggel, diszlipidémiával és elhízással, amelyek a metabolikus szindróma (MetS) fő alkotóelemei [1] - [6], számos újabb tanulmány arról számolt be, hogy szoros összefüggés van a NASH és a magas vérnyomás között is [7] - [9]. Ezért a NASH-t a MetS máj manifesztációjának tekintették. Fontos, hogy a túlélési arány csökkent a NASH-betegeknél, akik a szív- és érrendszeri események mellett gyakran májval kapcsolatos okok miatt haltak meg [10]. Mivel a NASH nem jóindulatú betegség, a MetS fontos egészséget veszélyeztető elemének tekintik [11], [12].
A NASH kialakulásában és progressziójában a koleszterin fontos szerepet játszik a máj szövetében oxidatív stresszt okozó NASH kialakulásában [13]. A magas zsírtartalmú étrend (HFD) növeli a szabad zsírsavakat, amelyek a mitokondriális β oxidációját és a szabad gyökök túltermelését indukálják [13], amelyek mindkettő fontos szerepet játszik a NASH progressziójában. Általában a NASH-ban szenvedő betegek hajlamosak a túlzott telített zsírsavval és koleszterinnel dúsított ételeket fogyasztani anélkül, hogy antioxidáns tápanyagokat, például E- és C-vitaminokat adnának; Az oxidatív stressz iránti fogékonyság és a túlzott lipidbevitel a NASH-betegek jellemzői lehetnek [8]. Tekintettel arra a kísérleti tényre, hogy az E- és C-vitamin javította a májkárosodást a NASH-ban [14], [15], a környezeti és belső reaktív oxigénfajta (ROS) -növelő ingerek felgyorsítják a NASH megjelenését és progresszióját.
Nemrégiben számos tanulmány azt sugallta, hogy a túlzott sóbevitel serkenti a ROS-termelést számos szervben, beleértve az ereket [16], a veséket [17], a szívet [18] és az agyat [19], egy Dahl-sóra érzékeny patkányokat alkalmazó modellben. Ezenkívül a magas sótartalmú étrend (HSD) normális patkányok esetében is növeli az oxidatív stresszt a vesékben [20], valamint az arterioláris és venularis falakat a vázizomzatban [21]. Ezért feltételeztük, hogy a túlzott sóbevitel, egy oxidatív stresszinduktor, a HFD által kiváltott NASH megjelenésének és progressziójának gyorsítója a ROS túltermelés miatt.
Hipotézisünk tisztázásához HFD-vel táplált lektinszerű oxidált kis sűrűségű lipoprotein receptor-1 (LOX-1) transzgén (Tg) és apoE knockout (KO) (TgKO) egereket használtunk a MetS modelljeként [22], amelyek krónikus lefolyást követ. Mivel a LOX-1, az oxidált, kis sűrűségű lipoprotein (ox-LDL) receptora, amely felhalmozódik az érelmeszesedésben, azt javasolják, hogy oksidatív stresszel kapcsolatos sejtkárosodást okozzon [23], [24], várható, hogy a LOX- Az 1 túlexpresszió tovább fokozhatja a szervkárosodást a só által kiváltott ROS túltermeléssel, és a NASH progresszióját okozhatja. Ebben a tanulmányban megvizsgáltuk a magas sótartalmú és zsírtartalmú étrend (HS/HFD) és a HFD hatását a TgKO egerek májkárosodására. Ezenkívül megvizsgáltuk, hogy az antioxidáns 4-hidroxi-2,2,6,6-tetrametil-piperidin-N-az oxil (tempol) enyhítheti a májkárosodást a TgKO egerekben.
Anyagok és metódusok
LOX-1 Tg/apoE KO (TgKO) egerek generálása
A célzott LOX-1 génexpressziót az endoteliális sejtekben a korábban leírtak szerint állítottuk elő [25]. A transzgén 24 példányát hordozó heterozigóta LOX-1 Tg egérvonalakat kereszteztük homozigóta C57BL/6-mal: a TgKO előállításához az apoE KO egereket a korábban leírtak szerint fejlesztettük [26], és a genetikai háttér helyettesítésére nyolcszor kereszteztük a C57BL/6 törzzsel. . Az apoE gén homozigóta mutációját Southern blot analízissel igazoltuk, a korábban leírtak szerint [27].
Állatok és protokollok
A jelen vizsgálatot 8 hetes hím TgKO egereken végezték. Véletlenszerűen csoportokba sorolták őket normál étrenddel (ND) (0,5 tömeg% só és 13 tömeg% zsír kalóriában), HFD (38 tömeg% zsír) vagy HS/HFD (7,9% sótartalmú HFD) táplálékkal 8 héten keresztül. Néhány HS/HFD-vel táplált TgKO egeret antioxidáns tempollal (Sigma-Aldrich, Mo) kezeltünk (7 mmol/l ivóvízben 8 hétig).
Valamennyi állat humánus gondozásban részesült, összhangban a Nemzeti Kutatási Tanács kritériumaival, amelyeket az Egyesült Államok Nemzeti Tudományos Akadémia készített és a Nemzeti Egészségügyi Intézet által kiadott „Útmutató a laboratóriumi állatok gondozásához és felhasználásához” vázoltak fel. A protokollt a Tokiói Egyetem állat-kutatási etikai bizottsága hagyta jóvá (engedélyszám: P08-051). Az összes műtétet nátrium-pentobarbitális altatásban végezték, és minden erőfeszítést megtettek a szenvedés minimalizálása érdekében.
Májszövettan
A szövettan számára a májszövet 5 μm vastag paraffin metszeteit készítettük az egyes májlebenyek közepéből. A metszeteket ezután hematoxilinnal és eozinnal, Masson-féle trichrommal vagy 4-hidroxinonenal (4HNE) és F4/80, TNF-a, szuperoxid-dismutáz-1 (SOD-1), kataláz, glutation ellen ellenanyagokkal festették. A NASH betegség súlyosságát Brunt és munkatársai osztályozási/stádiumrendszere alapján értékeltük. [28] és az alkoholmentes zsírmájbetegség (NAFLD) aktivitási pontszáma Kleiner és mtsai. [29].
A ROS termelésének vizsgálata, a 4HNE (anti-4HNE antitest; JaICA, Shizuoka, Japán) és a SOD-1 (anti-SOD-1; sc-11407, Santa Cruz, CA), kataláz (anti-kataláz; sc-50508) immunhisztokémiája., Santa Cruz, Kalifornia), glutationt (anti-glutation; AB-T01, Advanced Targeting Systems, CA) végeztünk. A gyulladás kimutatásához a máj metszeteket F4/80 (anti-F4/80; sc-59171, Santa Cruz, CA) és TNF-a (anti-TNF-a; ab-34674, Abcam, Cambridge, Egyesült Királyság).
A máj szövettani jellemzőit két olyan kutató értékelte, akik nem tudtak a tárgylemezek eredetéről. A NAFLD aktivitási pontszámot állatonként 5 kettős-vak, véletlenszerű képen értékeltük (n = 6–23) a máj különböző lebenyeiből.
A biokémiai index mérése
A szérum teljes koleszterinszintjét 8 hetes diéta után mértük ELISA készletekkel (T-Cho H, Wako, Osaka, Japán). A szérum alanin-transzamináz (ALT) aktivitásokat spektrofotometriásan mértük egy kereskedelemben kapható tesztkészlet (ALT reagensek, Alfresa, Osaka, Japán) alkalmazásával. Az összes máj trigliceridet fagyasztva szárított mintákból kloroform: metanol (2: 1) eleggyel extraháltuk. A májszövet-kivonatban lévő triglicerideket ezután enzimatikusan meghatároztuk egy auto-analizátorban egy kereskedelmi készlet segítségével (L típusú Wako trigliceridek H, Wako, Osaka, Japán). A májfibrózis vérmarkerként a szérum hyaluronsavat (HA) szintén megvizsgálták egy kereskedelmi készlet segítségével (Lpia ace HA, IATRON, Tokió, Japán).
Western blot elemzés
Western-blotot a korábban leírtak szerint hajtottunk végre [30]. A 4HNE-t, a fibronektint és a béta-aktint ugyanarra a membránra blotoltuk megfelelő monoklonális antitesttel. Elsődleges antitestek a 4HNE (JaICA, Shizuoka, Japán), a fibronektin (sc-71113, Santa Cruz, Kalifornia) és a β-aktin (A-5316, Sigma-Aldrich, St. Louis, MO). A blotokat Scion képanalízissel számszerűsítettük.
Az endogén és transzgén LOX-1 mRNS-szintjének elemzése
A teljes szöveti RNS-t kivontuk a májszövetekből. A reverz transzkripciós polimeráz láncreakció (RT-PCR) elemzéséhez a cDNS terméket szintetizáltuk és PCR-rel amplifikáltuk kereskedelmi készlet (Thermoscript RT-PCR készlet, Invitrogen, CA) felhasználásával. A termikus ciklusos körülmények 35 ciklus: 94 ° C 40 másodpercig, 60 ° C 1 percig és 72 ° C 1 percig LOX-1-hez.
A nikotinamid-adenin-dinukleotid-foszfát (NADPH) által kiváltott szuperoxid termelés mérése a májban
A májban a szuperoxid-anionok termelését lucigenin kemilumineszcencia alkalmazásával mértük mikrotányér-luminométerben (LB 9507, Berthold Technologies, Németország), az előzőekben leírtak szerint [18].
Máj perfúziós kísérletek
Az egereket pentobarbitállal (50 mg/kg) altattuk, és a katétert a portális vénába juttattuk. A májat 95% O2 és 5% CO2 tartalommal telített Krebs-Henseleit-hidrogén-karbonát pufferral 5 ml/perc sebességgel 5 percig 37 ° C-on perfundáltuk. Ezt követően a májat 10 percig 1 mM H2O2-t tartalmazó Krebs-Henseleit-hidrogén-karbonát-pufferrel és 5 percig 0,05% nitrokék-tetrazóliumot (NBT, Sigma-Aldrich, Mo) tartalmazó Krebs-Henseleit-hidrogén-karbonát-pufferrel perfundáltuk. Ezután a májat 10% -os formalinnal rögzítettük, paraffinba ágyazottuk, metszettük és nukleáris gyorsan vörös színnel festettük. A formazan lerakódások mértékét fénymikroszkóppal értékeltük [31].
Statisztikai analízis
Az összes értéket átlag ± SEM-ben fejezzük ki. A csoportok közötti összehasonlításokat ANOVA-val számítottuk, majd Dunnett-módszerrel, és a valószínűségi értékekkel P
Eredmények
A máj LOX-1 expressziójának RT-PCR elemzése
Csak a LOX-1 transzgének májban való expresszióját igazoltuk RT-PCR analízissel. Transzgénikus szarvasmarha LOX-1 és endogén egér LOX-1 mRNS-t detektáltunk a májban (1. kiegészítő fájl: S1 ábra). Az endogén egér LOX-1 és a transzgénikus szarvasmarha-LOX-1 azonos intenzitású LOX-1 jel intenzitással rendelkezett, amint arról korábban beszámoltunk [24].
Szisztolés vérnyomás
A szisztolés vérnyomás a HFD és a HS/HFD csoportokban egyaránt megemelkedett (114,2 ± 0,3 Hgmm és 118,4 ± 3,3 Hgmm; P 1. ábra
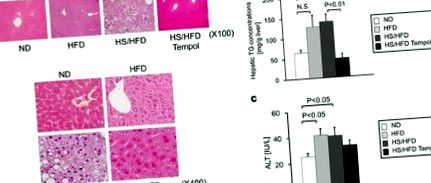
A zsír felhalmozódása a májban és a máj működése különböző diétás kezelésekkel rendelkező egerekben. a, Reprezentatív májszövettani leletek (HE festés: eredeti nagyítás, X100, X400). b, A normál étrend (ND), a magas sótartalmú és magas zsírtartalmú étrend (HS/HFD), a magas zsírtartalmú étrend (HFD) és a HS/HFD táplálás, valamint a 4-hidroxi-2,2,6,6-tetrametil- piperidin-N-oxil (tempol) kezelés (HS/HFD Tempol) a máj triglicerid koncentrációin (n = 4-14/csoport). c, Szérum alanin-transzamináz (ALT) aktivitások (n = 5-11/csoport). Az értékek átlag ± SEM.
A NASH értékelése a NAFLD aktivitási pontszám alapján. a, steatosis fokozatú. b, - a májsejtek léggömbölés fokozata, és c, gyulladásos fokozat. d, fibrózis stádium. e, NAFLD aktivitási pontszám. A NASLD diagnózisához a NAFLD aktivitási pontszámának legalább öt pontját értékelték. A folytonos vonalak öt pont határát jelzik. n = 6-23/csoport. Lásd a rövidítéseket az 1. ábra jelmagyarázatában.
A szérum HA és a fibronektin expressziója a májban
A fibrózis progressziójának vizsgálatához steatohepatitisben értékeltük a szérum HA értékeket (2a. Ábra). A sótöltés növelte a HA-t. Hasonlóan a HA-hoz, a sótöltet is megnövelte a fibronektin expressziót a HS/HFD csoport májában (2,6-szoros) az ND csoporthoz képest (P 4. ábra
Ezután az oxidatív stressz felhalmozódásának igazolására a 4HNE-addukált fehérje immunfestését végeztük a májszakaszokban. A lipidperoxidáció szignifikánsan megemelkedett a HS/HFD csoportban az ND vagy HFD csoportokhoz képest (4b. Ábra). A lipid peroxidáció mennyiségét a máj 4HNE Western blot analízisével számszerűsítettük. A 4HNE körülbelül 2,0-szeresére nőtt a HS/HFD-ben (P
Vita
Ez a tanulmány először megerősíti, hogy a HFD sóterhelése felgyorsíthatja a NASH indukcióját. A HS/HFD jelentős zsíros degenerációt váltott ki a máj központi vénái körül, ami fibrotikus változásokkal társult. A HS/HFD-vel táplált egerekben megfigyelt zsíranyagcsere, gyulladás és pericelluláris fiborosis romlása megfelelt a NASH kritériumainak humán [28], [29], és a Kleiner-pontszám szignifikánsan magasabb volt a HS/HFD-vel táplált egerekben (3. ábra ) [29]. Ezek a fibrotikus változások összehasonlíthatók voltak a máj szérum HA-szintjével és a fibronektin-expresszióval, mindkettő szignifikánsan megemelkedett a HS/HFD-vel táplált egerekben.
A jelenlegi modellben a sótöltés rövid idő alatt (8 hét alatt) 23 egérből 8-ban (35%) felgyorsította a NASH megjelenését és progresszióját (3e. Ábra). A humán NASH kóros kritériumaiban a zsíros degeneráció és a fibrózis mellett a pericelluláris hepatocita ballonozást kritikus patológiás eredménynek tekintik az NASH diagnózisában emberben. Érdekes, hogy a jelenlegi vizsgálat megerősítette, hogy a hepatocita ballonosodás korábban, mint a zsíros degeneráció, több mintában történt, amikor sóterhelést adtak a HFD-vel táplált egerekhez. Ebben a sótúlterheléssel rendelkező csoportban a hisztopatológiai gyulladásos és fibrotikus változások figyelemre méltóbbak voltak, és a szérum HA és fibronektin szintje szignifikánsan magasabb volt (2a. És b. Ábra) a sótúlterhelés nélküli HFD-vel táplált egerekhez képest.
Egy másik figyelemre méltó eredmény az volt, hogy a tempol, egy SOD utánzó, csökkentheti a máj NASH-szerű hisztopatológiai változásait a HS/HFD-vel táplált egerekben. A Tempol eltávolítja a ROS-t a NADPH oxidáz segítségével. Beszámoltak róla, hogy maga a ROS képes aktiválni a NADPH-oxidázt valószínűleg az érrendszerben az előre-visszahordó hurokban [34] - [36], és az ROS redukciója egy radikális megkötővel, a tempol-mal megszakíthatja a NADPH-oxidáz aktivitást. Jelen tanulmányban a tempol visszaállíthatja mind a NADPH oxidáz aktivitást (4a. Ábra), mind az ROS-t, amint azt a 4HNE expressziója (4b és c ábra) mutatja a májban és az oxigéngyök képződése a Kupffer-sejtekben H2O2 előkezelés után (4d. Ábra). Mivel a tempol csak az ROS-t szedi és nem befolyásolná közvetlenül a NADPH-oxidáz aktivitását, a NADPH és az ROS közötti előremenő aktivációs mechanizmus a májban is jelen lehet [18].
A vizsgálat korlátai közé tartozik, hogy az ebben a vizsgálatban alkalmazott modell nagyon érzékeny volt a zsír túlterhelésére, és a sótöltés viszonylag erős volt. Így továbbra is nehéz meghatározni, hogy a sótöltés mekkora mértékben növeli a NASH kockázatát. Ezenkívül a ROS-termelés részletes mechanizmusa a sóterhelésben még mindig nem világos, és további vizsgálatokra van szükség. A jelenlegi eredmények azonban egyértelműen jelezték annak lehetőségét, hogy a sótúlterhelés felgyorsíthatja a NASH indukcióját a HFD-re fogékony egerekben. Ezenkívül modellünk jobb modellt tud nyújtani a NASH-tól, összehasonlítva a hagyományos állatmodellekkel, amelyek hosszabb távú étrendi módosításokat vagy több géntechnikát igényelnek. Ezt a modellt az étrend okozta oxidatív stressz és a MetS genetikai hátterének túltermelése jellemzi. Ezért fel lehet használni a NASH környezeti és genetikai hajlamának hatásainak értékelésére.
Összefoglalva, a sótúlterhelés felgyorsíthatja az oxidatív stressz felhalmozódását HFD-fogyasztás mellett, és diszlipidémiás modellben, LOX-1 Tg és apoE KO egerekben indukálhatja a NASH-t a májban. Bár további vizsgálatokra van szükség annak tisztázására, hogy a sóbevitel mennyire befolyásolja a krónikus májkárosodás ROS termelését és előrehaladását, ez a tanulmány kiváltaná a kísérleti érdeklődést, hogy a sóbevitel fontos-e a májbetegség előrehaladásában vagy sem.
- A magas zsírtartalmú étrend által kiváltott zsírbetegség, zsírgyulladás, máj steatosis és hiperinsulinémia
- A magas zsírtartalmú étrend hajlandóvá teszi az egereket a máj károsodására - ScienceDaily
- Májbetegség - ájurvédikus étrend, életmód,; Gyógynövényes gyógymódok - mindAyurveda
- Májfunkció és vegetáriánus étrend egészségesen
- A magas zsírtartalmú étrend-fogyasztás különböző módon befolyásolja a zsírszövet gyulladását és a zsírsejtek méretét