Topiramát által kiváltott perifériás neuropathia: Esettanulmány és irodalom áttekintése
Sherifa Ahmed Hamed
Neurológiai és Pszichiátriai Osztály, Assiut Egyetemi Kórház, Assiut 71516, Egyiptom. [email protected]
Levelezés: Dr. Sherifa Ahmed Hamed, egyetemi tanár, neurológus tanácsadó, Assiuti Egyetemi Kórház Neurológiai és Pszichiátriai Osztálya, 7. emelet, 4. szoba, Assiut 71516, Egyiptom. [email protected]
Telefon: + 20-88-2371820 Fax: + 20-88-2333327
Absztrakt
Alap tipp: A perifériás neuropathia az epilepszia elleni gyógyszerek (fenitoin, fenobarbitál, karbamazepin, valproát, gabapentin, levetiracetám és lakozamid) rövid vagy hosszú távú alkalmazásának ritka káros hatása. Ez a topiramát által kiváltott perifériás neuropathia (TIPN) első esete. A TIPN megnyilvánulásai distalis paresztézia, areflexia, érzékszervi hiányok, valamint az alsó végtagok motoros és szenzoros perifériás idegeinek csökkent amplitúdói és idegvezetési sebességei, amelyek demielinizáló és axonális neuropátiákra utalnak. A kockázat hosszabb a hosszú távú terápia esetén. A TIPN mechanizmusai magukban foglalhatják az idegműködés károsodását a nátrium feszültségcsatornáinak blokkolásával, a gamma-amino-vajsav gátló neurotranszmisszió fokozásával vagy másokkal.
BEVEZETÉS
A topiramát (TPM) egy széles spektrumú epilepszia elleni gyógyszer (AED) a rohamok fajtáinak kezelésére felnőtteknél és gyermekeknél. A TPM kiegészítő vagy monoterápiaként ajánlott két vagy több éves, generalizált tonikus klónikus epilepsziában vagy fokális epilepsziában szenvedő, másodlagos generalizációval vagy anélkül szenvedő betegek kezelésére, amelyek refrakterek a többi AED-kezelésre; valamint Lennox-Gastaut-szindróma (LGS) esetén [1]. A TPM-et az Egyesült Államok Élelmiszer- és Gyógyszerügyi Hivatala (FDA) fenterminnel kombinálva hagyta jóvá a fogyás [2] és a migrén megelőzése érdekében [3]. A TPM nem engedélyezett felhasználásokkal is rendelkezik, vagyis nem szerepel a betegtájékoztatóban és/vagy az előírásokról szóló tájékoztatóban], amelyek magukban foglalják a bipoláris rendellenesség kezelését [4]; határos személyiségzavar [5]; alkoholizmus [6]; és antipszichotikumok által kiváltott súlygyarapodás [7]; és hangulatstabilizátorként [8].
A TPM-nek számos káros mellékhatása van. Néhány nagyon gyakori (> 10% -os előfordulási gyakoriság), beleértve a szédülést, a fogyást, az arc, a száj és a végtagok paresztéziáját (tűk és tűk, amelyek a betegek 12% -14% -ánál fordulnak elő), aluszékonyságot, émelygést, hasmenést és fáradtságot. Mások gyakoriak (1% -10% előfordulása), ideértve a figyelem zavart, memóriahiányt, amnéziát, kognitív rendellenességeket, pszichomotoros lassulást, rendellenes koordinációt, remegést, szedációt, hányást, vertigo, fülzúgást, szájszárazságot, ízérzékenységet és hasi kellemetlenségeket. Ezen mellékhatások többsége azonban enyhe/mérsékelt, átmeneti és összefügg a magasabb dózisokkal és/vagy a dózis gyors titrálásával. Így ezek a mellékhatások csökkenthetők vagy megelőzhetők a TPM alacsony dózisban történő indításával és az adag fokozatos növelésével [9]. Emellett a TPM-nek vannak olyan ritka és súlyos mellékhatásai, amelyek szükségessé teszik a gyógyszer megvonását és helyettesítését, ezek közé tartozik az akut szögletes glaukóma, az akut myopia, az izzadás csökkenése és a testhőmérséklet emelkedése, zavartság, beszédleállás [10], nyilvánvaló metabolikus acidózis [11]. és klinikai jelentőségű urolithiasis [12]. Ezen mellékhatások többsége a TPM karboanhidráz enzim gátló tulajdonságaihoz kapcsolódik.
Az irodalom áttekintése azt mutatja, hogy az AED-terápia ritkán társul perifériás neuropathiával. A perifériás neuropathia a fenitoin (PHT) ritka káros hatása, klinikai és kísérleti vizsgálatok bizonyítékaként [13,14]. Rövid távú (óráktól-hetekig) PHT-kezeléssel toxikus [15-18] vagy nem toxikus dózisokban [19-21] és hosszú távú (≥ 5 éves) PHT-terápiával [22-25] számoltak be . Perifériás neuropathiáról más AED-kkel, például karbamazepinnel (CBZ) [26-28], fenobarbitállal (PB) [27], nátrium-valproáttal (VPA) [26,27,29,30], gabapentinnel (GPN) [ 31], levetiracetám (LEV) [32] és lakozamid (LCM) [33]. A TPM által kiváltott perifériás neuropathiáról nincs korábbi jelentés.
ESETLEÍRÁS
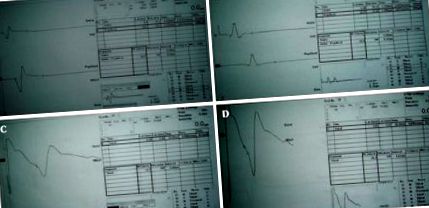
A jobb (A) és a bal tibialis (B) idegek, valamint a jobb (C) és a bal sural (D) idegek vezetési sebességének vizsgálata nyúlt hosszan tartó disztális látenciát, csökkent motoros és érzékszervi vezetési sebességet, valamint csökkent motoros és szenzoros cselekvési potenciált (amplitúdó) ).
Ezt a vizsgálatot a Helsinkiben megállapított és az Assiuti Egyetemi Kórház etikai bizottságának jóváhagyása alapján végezték el. Tájékozott írásos beleegyezést kapott a pácienstől klinikai előzményeinek, laboratóriumi és neurofiziológiai adatainak közzétételéhez.
VITA
A PHT által kiváltott perifériás neuropathia mechanizmusa (patogenezise) nem ismert. Kísérleti vizsgálatok kimutatták, hogy a PHT depressziós hatást fejt ki a perifériás idegekre [13], ami a gyógyszer perifériás idegekre gyakorolt közvetlen toxikus hatásának és/vagy a nátriumcsatornák elzáródásának tudható be, amely a fő görcsoldó hatásmechanizmusa. Korey [43] kimutatta a PHT gátló hatását a tintahal óriás axonján, amelyet az alacsony kalcium- és magnéziumszint hiperexcelhetővé tett. Eisen és munkatársai [22] primer axonális zsugorodásról és másodlagos demyelinizációról számoltak be PHT-vel. Long és munkatársai [44] és Hansen és mtsai [45] kimutatták, hogy a PHT által kiváltott perifériás neuropathia a megaloblasztos vérszegénységgel összefüggésben állt összefüggésben a szubnormális szérum foláttal. Javasoljuk, hogy a TPM által kiváltott perifériás neuropathia összefüggésben lehet antikonvulzív hatásmechanizmusával, amely multifaktoriális és magában foglalja a feszültségfüggő nátriumcsatornák blokkolását (hasonlóan a PHT-hez); a nagyfeszültség által aktivált kalciumcsatornák gátlása; a GABAerg transzmisszió erősítése a GABA-A receptorokon keresztül; az izgató útvonalak gátlása a-amino-3-hidroxi-5-metil-4-izoxazol-propionsav (AMPA) AMPA/kainát receptor helyeken kifejtett hatás révén és a karboanhidráz izoenzimek gátlása [1].
Perifériás neuropathiában szenvedő betegről számolunk be a TPM krónikus terápiás dózisa után. Ez a káros hatás azonban enyhe, statikus volt, és a beteg tolerálta, és nem tűnt el B-vitamin-kiegészítőkkel. Szükség van kísérleti és klinikai vizsgálatokra is a TPM perifériás idegekre gyakorolt hatásának és a TPM által kiváltott perifériás neuropathia mechanizmusának (mechanizmusainak) azonosítására.
HOZZÁSZÓLÁSOK
Az eset jellemzői
Egy 37 éves nő másodlagos generalizációval jelentkező frontális lebeny epilepsziában szenvedett, amely mono- vagy kombinált terápiában nem volt kezelhető a különböző epilepsziaellenes gyógyszerekkel szemben. A topiramát (TPM) monoterápia jelentősen kontrollálta a beteg rohamait. Két éves TPM-terápia után a beteg paresztéziát váltott ki, csökkentette az Achilles-ín reflexeit, csökkentette a hipesztéziát és késleltette a disztális látenciákat, csökkentette a hátsó tibialis és surális idegek vezetési sebességét és cselekvési potenciáljának amplitúdóját.
- A nagyon megnagyobbodott méh (3030 g) teljes laparoszkópos méheltávolítása esettanulmány és a
- Az agomelatin és a melatonin hatása az alvással kapcsolatos étkezésre esettanulmány Journal of Medical
- A gyógygomba Agaricus blazei Murrill Irodalmi és gyógyszer-toxikológiai áttekintése
- Mi akadályoz a fogyásban Sámángyógyító eset jelentés
- Tula Ergonomic Baby Review BabyGearLab