A TRPV1 megvédi a vese ischaemia-reperfúziós károsodást étrend okozta elhízott egereknél azáltal, hogy fokozza a CGRP felszabadulást és növeli a vese véráramlását.
Absztrakt
Háttér
Az elhízás a végstádiumú vesebetegségek egyik fő kockázati tényezője. A tranziens receptor potenciális vanilloid 1 knockout (TRPV1 -/-) egerek felhasználásával teszteltük azt a hipotézist, miszerint a TRPV1 véd az elhízás által kiváltott vese ischaemia-reperfúziós (I/R) sérüléssel szemben.
Mód
A TRPV1 -/- és a vad típusú (WT) egereket 22-23 héten át etettük chow- vagy Western-étrenddel (WD). Ezt követően az egereket vese I/R sérülésnek vetették alá, és mértük a vesekérgi véráramlást (CBF) és a medulláris véráramlást (MBF).
Eredmények
A nyugati étrend mind a TRPV1 -/-, mind a WT egerekben jelentősen megnövelte a testsúlyt és az éhomi vércukorszintet. A WD által kiváltott glükóz tolerancia romlás a TRPV1 -/- egerekben súlyosbodott a WT egerekhez képest. A WD bevitele meghosszabbította a kéreg és a medulla csúcsos reperfúziójának eléréséhez szükséges időt (mindkettő P -/- egerek (mind P -/- egerek és a WD gyengítette a CGRP felszabadulást a WT egerekben. Ezenkívül a CGRP receptorok blokádja károsította a vese regionális véráramlását és a vesefunkciót a vese I/R sérült WT egerekben.
Következtetés
Ezek az eredmények azt mutatják, hogy a TRPV1 védő szerepet játszik a vese I/R sérülés WD által kiváltott exacerbációjában, valószínűleg a CGRP felszabadulás fokozásával és a vese véráramlásának fokozásával.
Bevezetés
Az elhízás a cukorbetegség és a magas vérnyomás egyik fő kockázati tényezője (Hall, 2003; Steinberger & Daniels, 2003), amelyek együttesen a végstádiumú vesebetegségek 70% -át teszik ki (Collins et al., 2005; Griffin, Kramer & Bidani, 2008). Az ischaemia-reperfúziós (I/R) sérülés az akut vesekárosodás (AKI) gyakori oka számos klinikai környezetben (Lameire, Van Biesen és Vanholder, 2006). Az AKI a kórházi betegek kb. 7% -ában fordul elő (Nash, Hafeez & Hou, 2002), és a kritikus betegek 40–60% -os teljes halálozásával jár (Uchino et al., 2005). A nyugati étrend (WD) bevitele elhízáshoz vezet, súlyosbítja a krónikus gyulladást és fokozza az akut vese ischaemiás károsodást (Kelly, Burford & Dominguez, 2009).
Az átmeneti receptor potenciál vanilloid 1 (TRPV1) egy ligandumkapu, nem szelektív ioncsatorna, amelyet többféle ingerrel lehet aktiválni, beleértve a káros hőt, az alacsony pH-értéket és a kémiai irritáló anyagokat, például a kapszaicint (Caterina et al., 2000; Julius & Basbaum, 2001). A TRPV1 elsősorban nem myelinizált C-rostokban és vékonyan myelinizált Aδ-afferens idegrostokban fejeződik ki, amelyek beidegzik a belső szerveket, beleértve a vesét is (Caterina et al., 2000; Julius & Basbaum, 2001). A TRPV1-aktiváció neuropeptidek, köztük a kalcitonin-génnel rokon peptid (CGRP) és a P-anyag felszabadulását okozza erős értágító hatásokkal (Wang, 2005), valamint natriuretikus és diuretikus hatásokkal (Arendshorst, Cook & Mills, 1976; Shekhar et al., 1991 ). A vesét a CGRP-pozitív érzékszervi idegek sűrű hálója innerválja (Chai et al., 1998). Sok más értágítóval ellentétben a CGRP növeli a vese véráramlását és a glomeruláris szűrést (Shekhar et al., 1991). A TRPV1 hiány fokozott I/R sérülést eredményez (Huang et al., 2009), ami arra utal, hogy a TRPV1 fontos szerepet játszik a vesekárosodásban (Levite et al., 1998, Okajima & Harada, 2006).
Az átmeneti receptor potenciális 1. vanilloid szorosan kapcsolódik az elhízáshoz és kölcsönhatásba lép azzal (Gram, Holst & Szallasi, 2017). Az elhízás rontja az érzéki idegek által közvetített értágulatokat (Davidson et al., 2010, Haddock & Hill, 2011). Baskaran és mtsai. (2017) arról számolt be, hogy az étrend okozta elhízás elnyomta a TRPV1 expresszióját a zsírszövetben. Ezen kívül Kentish és mtsai. (2015) kimutatta, hogy a ganglionos TRPV1 inaktiválódott elhízott egerekben, amelyet magas zsírtartalmú étrend váltott ki. Sőt, a TRPV1 hiány súlyosbítja az étrend okozta elhízást és inzulinrezisztenciát (Lee és mtsai, 2015). Így a WD bevitele károsíthatja a TRPV1 expresszióját vagy működését, ami súlyosabb vese I/R sérüléshez vezethet, és a TRPV1 hiány súlyosbíthatja a vese I/R sérülést. Ebben a tanulmányban azt a hipotézist teszteltük, hogy a WD bevitel által kiváltott elhízás súlyosbítja a vese I/R gyógyulását, és hogy a TRPV1 abláció fokozza a vese perfúziójának károsodását, majd rontja a vesefunkció helyreállítását.
Anyagok és metódusok
Etetési tanulmányok és gyógyszerek
A hím TRPV1 gén knockout (TRPV1 -/-) B6.129S4-TRPV1 tm1Jul törzset és a vad típusú (WT) C57BL/6J törzset (Jackson Laboratory, Bar Harbor, Maine) használtuk. A testtömeget 3 és 23 hetes kor között figyeltük, miközben mindkét egértörzs szabadon hozzáférhetett a chow-étrendhez (con; 8664; Harlan Teklad, Madison, WI, USA) vagy (WD; 42% kcal zsírból; 88,137, Harlan Teklad ) és csapvíz a kísérletek során. Az egereket normál világos/sötét ciklusban tartottuk. A táplálékfelvételt és a testsúlyt hetente egyszer mérték. Az összes kísérleti eljárást a Michigani Állami Egyetem Intézményi Állattenyésztési és Felhasználási Bizottsága hagyta jóvá (08/14-141-00).
Intraperitoneális glükóz tolerancia teszt
A kísérleti egereket 15 órán át éheztettük (tápláléktól megfosztva, de vizet adva), majd intraperitoneális injekcióval glükózt (két g/testtömeg-kg) adtak be tudatos egereknek. A glükóz beadását követően a farok vénájának véréből mintát vettünk a glükóz meghatározásához Accu-Chek glükózmérővel (Roche Diagnostics, Mannheim, Németország) 0, 30, 60 és 120 perccel. A görbe alatti területeket (AUC) a glükóz toleranciához a trapéz szabály szerint számítottuk ki a glükóz mérésekből 0, 30, 60 és 120 percnél. A glükóz toleranciát AUC-ként határozták meg vs. a trapéz szabállyal számított időgörbe.
Western blot elemzés
A fehérjéket a vese szövetéből kivontuk proteázinhibitorokat tartalmazó lízispufferrel (Sigma, St. Louis, MA, USA). Az összes fehérjét 10% -os nátrium-dodecil-szulfát-poliakrilamid gélen szétválasztottuk, és polivinilidén-difluorid membránra vittük át. A membránokat 1 órán át szobahőmérsékleten blokkoltuk 5% zsírmentes tejmosó oldatban (50 mM Tris-HCl, 100 mM NaCl, 0,1% Tween 20, pH 7,5). Ezután a membránokat nyúl anti-TRPV1 poliklonális IgG-vel (1: 1000, ab6166; Abcam, Cambridge, MA, USA) és nyúlellenes IgG-HRP-vel (1: 5000, Santa Cruz Biotechnology, Dallas, TX, USA) inkubáltuk. A membránokat egy továbbfejlesztett kemilumineszcencia detektáló rendszerrel (ECL; Amersham Biosciences, Piscataway, NJ, USA) tettük láthatóvá és filmeknek tettük ki (Hyperfilm-ECL; Amersham Pharmacia Biotech, Little Chalfont, Egyesült Királyság). A sűrűségeket a J 1.46 kép (NIH) alkalmazásával határoztuk meg, és normalizáltuk az egyes üregekbe töltött glicerinaldehid-3-foszfát-dehidrogenáz teljes mennyiségére.
A vizelet 8-izoprostán elemzése
A 23 hetes diétás kezelés végén az egereket 24 órás vizeletgyűjtés céljából egér metabolikus ketrecekbe helyeztük. A vizelet 8-izoprostán szintjét kit segítségével határoztuk meg (Cayman Chemical, Ann Arbor, MI, USA).
Vese ischaemia-reperfúziós modell
A vizelet laktát-dehidrogenázának mérése
Reperfúzió után a vizeletet a húgyhólyagba helyezett katéteren keresztül gyűjtötték, és a mintákat az elemzésig -80 ° C-on tartották. A laktát-dehidrogenázt (LDH) LDH Activity Assay Kit (Biovision, San Francisco, CA, USA) segítségével mértük.
A vesefunkció értékelése
A vesefunkciót a plazma kreatinin és a karbamid koncentrációjának mérésével értékeltük. A plazmamintákat összegyűjtöttük és standard assay készletek felhasználásával megmértük (Biovízió).
A CGRP mérése
A plazmát összegyűjtöttük, majd a CGRP-t megtisztítottuk és patkány CGRP radioimmunassay kit alkalmazásával elemeztük. A vizsgálatot a szállító ajánlása szerint hajtottuk végre (Peninsula Laboratories Inc., Belmont, Kalifornia, USA).
Statisztikai analízis
Valamennyi értéket átlag ± SEM-ben fejezzük ki. A csoportok közötti különbségeket egyirányú varianciaanalízissel hajtottuk végre, amelyet Tukey-Kramer többszörös összehasonlító teszt követett. Két csoport közötti különbségeket a t-tesztek. Az eredményeket statisztikailag szignifikánsnak tekintették a P
Eredmények
A TRPV1 kiiktatása súlyosbította a WD által kiváltott glükóz-intoleranciát és az oxidatív stresszt
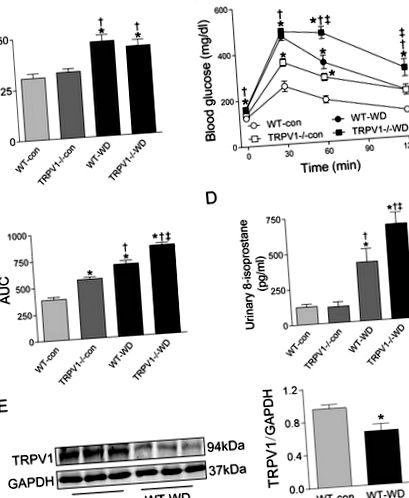
23. héten a WD bevitel növelte a testsúlyt mind a WT, mind a TRPV1 -/- egerekben, összehasonlítva a chow étrend csoportokkal (mindkettő P -/- egerekkel chow vagy WD tápláltak (1A. Ábra). Hasonlóképpen, az éhomi plazma glükózszintje szignifikánsan magasabb volt a WD csoportokban mindkét törzsben (P -/- egerek (1B. Ábra). Ezzel szemben a WD által kiváltott glükóz tolerancia károsodást súlyosbította a TRPV1 -/- egerek a WT egerekhez képest (P -/- egerek a WT egerekhez képest (P
1. ábra: Testtömeg, glükóz tolerancia, oxidatív stressz és TRPV1 expresszió.
A TRPV1 kiiktatása súlyosbította a vesék véráramának helyreállításának WD által kiváltott károsodását
I/R után a chow-étrenden lévő TRPV1 -/- egereknél jelentősen csökkent a CBF és az MBF helyreállítási aránya, és megnőtt a reperfúzió csúcsáig eltelt ideje a chow-étrenden lévő WT egerekhez képest, ami arra utal, hogy a TRPV1 abláció rontja a vese I/R gyógyulását (2. ábra ). Ahogy az várható volt, a WD bevitele csökkentette a CBF és az MBF helyreállítási arányát, és megnövelte a reperfúzió csúcsáig eltelt idejét a vese I/R sérülés után mindkét törzsben, nagyobb mértékű csökkenés mellett a TRPV1 -/- egereknél a reperfúzió csúcsáig tartó idő további növekedése (2. ábra).
2. ábra: A vese véráramlásának helyreállítási aránya és a reperfúzió csúcsáig eltelt idő.
A TRPV1 kiiktatása súlyosbította a WD által kiváltott veseműködési rendellenességeket
A vese I/R sérülésnek kitett egerekben a WD bevitele mindkét törzsben növelte az LDH aktivitást, a plazma kreatinint és a vér karbamid-nitrogént (BUN) P -/- egerek a WT egerekhez képest (mind P
3. ábra: Vesekárosodás és működés.
A CGRP hozzájárul a vese I/R helyreállításához
A plazma CGRP-szinteknek nincs szignifikáns különbség a WT és a TRPV1 -/- egerek között sem chow, sem WD diétával. A renalis I/R fokozta a CGRP felszabadulást a WT egerekben, de a TRPV1 -/- egerekben nem. Ezenkívül a WD gyengítette az I/R indukálta CGRP felszabadulást WT egerekben (4A. Ábra). A csecsemőtáplálást végző WT egerekben a CGRP8–37 a CBF és az MBF helyreállítási arányának jelentős csökkenéséhez és a reperfúzió csúcsáig eltelt idő figyelemre méltó növekedéséhez vezetett. Ezenkívül a CGRP8–37 kezelés megnövelte a vizelet LDH, BUN és plazma kreatininszintjét a WT egerekben (4B – 4F. Ábra).
4. ábra: A CGRP 8–37 hatása a vese véráramlására és működésére.
Vita
Jelen tanulmányban azt tapasztaltuk, hogy a WD bevitele glükóz intoleranciát, oxidatív stresszt és a vesék véráramlásának és vesefunkciójának károsodott helyrehozását okozta I/R sérülés után, amit súlyosbítottak a TRPV1 -/- egerekben a WT egerekhez képest. A renalis I/R fokozta a CGRP felszabadulást a WT egerekben, amelyet a WD bevitele tompított. A CGRP receptorok blokádja károsította a vese regionális véráramlását és a vesefunkciót az I/R után a WT egerekben. Ezzel szemben a CGRP felszabadulása nem változott a TRPV1 -/- egerekben vese I/R sérülés után.
Az átmeneti receptor-potenciál vanilloid 1 fontos szerepet játszik az étrend okozta elhízásban és a glükóz intoleranciában (Lee és mtsai, 2015). Megállapítottuk, hogy a TRPV1 -/- egerek glükóz intoleranciában szenvedtek még a kontroll étrendben is, míg a vizelet 8-izoprostánja normális volt a WT egerekhez képest. Korábbi tanulmányok kimutatták, hogy a TRPV1 aktiváció indukálhatja az inzulin szekrécióját (Mori et al., 2018). Ezért a TRPV1 hiány okozta glükóz intolerancia valószínűleg az inzulin szekréciójának károsodása, nem pedig az oxidatív stressz miatt következik be. Ez is oka lehet annak, hogy az étrend okozta glükóz intolerancia súlyosbodott a TRPV1 -/- egerekben.
A vese véráramlásának általános csökkenése hozzájárul a glomeruláris szűrési sebesség (GFR) csökkenéséhez az iszkémiás AKI-ban (Alejandro et al., 1995). Korábbi vizsgálataink azt mutatták, hogy a TRPV1 aktiválása megnövelte a GFR és a vesekiválasztási funkciót (Li & Wang, 2008), ami arra utal, hogy a TRPV1 abláció tovább csökkentheti a GFR és a vesék kiválasztási funkcióját I/R alatt. Más tanulmányok azt mutatták, hogy a TRPV1 aktiváció fokozta az endothelium-függő vaszkuláris relaxációt (Yang et al., 2010) és a WD bevitel károsította az endotheliális funkciókat (Vogel, Corretti & Plotnick, 1997), ami arra utal, hogy a TRPV1 abláció csökkentheti a vese véráramlásának helyreállítását a vese I/R közvetlenül károsítja az endothelium-függő relaxációt.
Az ischaemia-reperfúzió növelheti az endogén TRPV1 agonistákat, például a 20-HETE analógokat, amelyekről kimutatták, hogy dózisfüggő módon növelik a vese véráramlását (Oyekan, 2005). Továbbá a 20-HETE analógoknak protektív hatása van a kísérleti vese I/R-ben (Regner et al., 2009). A TRPV1 abláció vagy a WD bevitele csökkentheti az endogén TRPV1 agonisták jótékony hatásait az I/R során, ami csökkent vesefolyáshoz és veseműködési zavarhoz vezet.
Következtetés
Összefoglalva, ezek az eredmények azt sugallják, hogy a TRPV1 protektív szerepet játszhat a vese I/R sérülésében az elhízásban, esetleg a vese véráramlásának fokozásával a fokozott CGRP felszabadulás révén.
- A genetikailag elhízott (obob) egerek étkezési mintája - ScienceDirect
- A görögdinnye-kiegészítők elhízott egerek számára hasznosak
- A görögdinnye-kiegészítők egészségügyi előnyökkel járnak az elhízott egerek számára - ScienceDaily
- A rapamicin heti adagolása javítja a túlzott zsírtartalmú elhízott hím egerek túlélését és biomarkereit
- Az étrend okozta elhízás és glükóz intolerancia kialakulása C57Bl6 egerekben zsírtartalmú étrenden