Az alkoholos zsírmáj molekuláris mechanizmusa
Karuna Rasineni
1 Belgyógyászati Klinika, Nebraskai Egyetem Orvosi Központ, Omaha, NE, USA
3 Biokémiai és Molekuláris Biológiai Tanszék, The Liver Study Unit, VA Nebraska-Western Iowa Health Care System, Omaha, NE, USA
Carol A. Casey
1 Belgyógyászati Klinika, Nebraskai Egyetem Orvosi Központ, Omaha, NE, USA
2 Biokémiai és Molekuláris Biológiai Tanszék, University of Nebraska Medical Center, Omaha, NE, USA
3 Biokémiai és Molekuláris Biológiai Tanszék, The Liver Study Unit, VA Nebraska-Western Iowa Health Care System, Omaha, NE, USA
Absztrakt
Bevezetés
Az alkoholfogyasztás és az alkohol okozta májbetegség (ALD) mind az Egyesült Államokban, mind világszerte jelentős közegészségügyi problémát jelent. Az ALD valószínűleg a súlyos alkoholfogyasztással élők fő halálozási oka, és a globális halálozás körülbelül 3,8% -áért felelős [1]. Az alkoholos májbetegség (ALD) korai megnyilvánulása a zsírmáj (máj steatosis) jelenléte, amely folyamatos sértés esetén alkoholos májbetegséggé (ALD) válhat.
Az alkohol okozta zsírsavszintézis általános mechanizmusa
Frissített mechanizmusok az etanol által kiváltott máj steatosisban
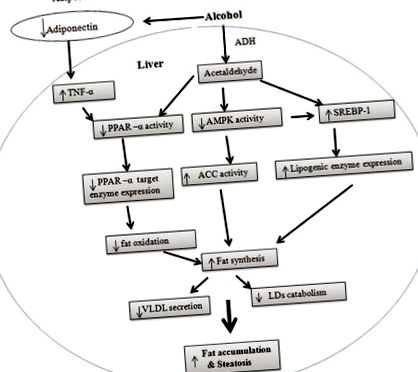
A máj teljes zsírmennyisége a zsírsavszintézistől és annak oxidációjától függ. Amint az 1. ábrán látható, az alkoholos zsírmáj patogenezise a megnövekedett glicerin-lipid szintézis és a mitokondriumok csökkent zsírsav-oxidációjának kombinációján alapul. A szintézis és az oxidáció mellett a zsírsavexport folyamatok is befolyásolják a zsírszintet.
Az alkoholos zsírmáj mögött álló potenciális mechanizmusok. A májban a szterin szabályozó elemeket megkötő fehérje 1 felelős a zsírsavszintézisért és a peroxiszóma proliferátor által aktivált receptor-α, az AMP-függő protein-kináz (AMPK) és az adiponektin felelős a zsírsav-oxidációért. Az etanol befolyásolhatja a PPAR-α, SREBP-1 és AMPK aktivitását közvetlenül, vagy az adiponektin és a tumor nekrózis faktor-α révén. Ezek a hatások aktiválják a lipogén útvonalakat és gátolják a zsírsavak oxidációját. A zsírsavszintézis és az oxidáció mellett az etanol megváltoztatja a lipidcseppek (LD, a TG tárolási formája) metabolizmusát a májsejtekben és a nagyon alacsony sűrűségű lipoproteinek májból történő kiválasztását. Mindezek a változások hozzájárulnak az alkohol okozta zsírmájhoz
Gyorsított szintézis
A zsírsavszintézisben részt vevő enzimeket főleg az 1-es szterin szabályozó elemet kötő fehérje (SREBP-1) szabályozza. [19] A szterol szabályozó elemeket megkötő fehérjék (SREBP) egy transzkripciós faktor család, amely szabályozza a májban és más szövetekben a koleszterin, zsírsavak és trigliceridek szintéziséért felelős enzimeket. Az SREBP-ket prekurzorokként szintetizálják (
125 kDa) kötődik az endoplazmatikus retikulumhoz és a mag burkolatához. Aktiválás után az SREBP-k érett fehérjeként felszabadulnak a membránból a sejtmagba (
68 kDa) szekvenciális kétlépéses hasítási eljárással. [20] Kimutatták, hogy az etanol expozíció jelentősen növeli az SREBP által szabályozott transzkripciót az érett SREBP-1 fehérje megemelkedett szintje révén. Így az etanol növeli a zsírsavszintézist az SREBP-1 révén. Az etanol SREBP-1-re gyakorolt hatása látszólag acetaldehiddé történő metabolizmusa révén közvetített. A publikált munka eredményei azt sugallják, hogy az acetaldehid növelheti az érett SREBP-1 fehérje szintézisét, ami fokozza a máj lipogenezisét és zsírmáj kialakulásához vezet [1. ábra]. [21]
Zavart zsírsav oxidáció
A zsírsavak oxidációja 3 szubcelluláris organellumban fordul elő, a β-oxidáció a mitokondriumokra és a peroxiszómákra korlátozódik, és a citokróm P450 4A (CYP4A) katalizált ω-oxidáció az endoplazmatikus retikulumban fordul elő. Ennek a 3 zsírsav-oxidációs rendszernek néhány kulcsfontosságú enzimét a májban peroxiszóma-proliferátor-aktivált alfa-receptor (PPAR-α), adiponektin és adenozin-monofoszfát-aktivált protein-kináz (AMPK) szabályozza.
A béta-oxidáció a zsírsav-észterek fő lebontási útja az emberekben, és ezt a karnitin-palmitoil-transzferáz-1 (CPT-1), a karnitin koncentrációja és a malonil-CoA szabályozza, amely gátolja a CPT-1-et. [22] A zsírsavbioszintézis etanollal történő egyidejű felfelé történő szabályozásával a zsírsavszintézis közbenső termékeinek, például a malonil-CoA intracelluláris felhalmozódása negatívan befolyásolhatja a zsírsavak mitokondriumba történő transzportját és oxidációját a CPT-1 gátlásával. A zsírsavak, a zsírsav-acil-CoA-k és a szerkezetileg különböző szintetikus vegyületek, amelyek peroxiszóma-proliferátorként ismertek, aktiválhatják a PPAR-α-t, és így szabályozhatják a máj CPT-1 szintjét. [22]
PPAR-α máj steatosisban
A peroxiszóma proliferátor által aktivált alfa-receptor (PPAR-α) a nukleáris hormon receptor szuper családjának tagja, és a májban lipid-érzékelőként működik. A PPAR-α felismeri a zsírsavak beáramlását és reagál azokra azáltal, hogy stimulálja a szabad zsírsavak oxidációjában, transzportjában és exportjában részt vevő PPAR-α által szabályozott gének transzkripcióját. Ide tartoznak a membrántranszporterek, például a CPT-1, az apolipoprotein gének, valamint a mitokondriális és peroxiszomális zsírsav β-oxidációs útvonalak számos alkotóeleme. AOX), 3-hidroxi-acil-CoA dehidrogenáz, multifunkcionális β-oxidációs fehérje (3-ketoacil-CoA tioláz), acil-CoA szintáz, malonil-Coa dekarboxiláz (MCD), CYP4A és CPT-1. Ezenkívül az MCD-t, amely a malonil-CoA szintjét szabályozza, pozitívan szabályozza a PPAR-α. [25]
Az alkohol alkoholos zsírmájban a PPAR-α-ra gyakorolt hatását tenyésztett hepatocitákban, valamint etanollal táplált rágcsálókban vizsgálták. Az alkohol kimutatta, hogy gátolja a PPAR-α aktivitást mind in vitro, mind in vivo körülmények között. [26,27] Az acetaldehid, az alkohol metabolitja, kulcsfontosságú tényező az alkohol PPAR-α-ra gyakorolt hatásában. Lehetséges, hogy az acetaldehid a fehérjék kovalens megkötésére való képessége miatt adduktokat képezhet a PPAR-a transzkripciós komplexszel, ezáltal megakadályozva a promóter elem (ek) megkötésének képességét. [28,29]
Adiponektin alkoholos májbetegségben
A PPAR-α mellett a máj lipidanyagcseréjét szorosan szabályozza az adiponektin és az adenozin-monofoszfát-aktivált protein-kináz (AMPK). Az adiponektin egy zsírszármazékból származó hormon, amely számos előnyös biológiai funkcióval rendelkezik. [30] Egyre több bizonyíték utal arra, hogy a zsírszövetben megváltozott adiponektin termelés és a máj adiponectin receptorainak (AdipoR) károsodott expressziója számos rágcsáló modellben összefüggésbe hozható az alkoholos máj steatosis kialakulásával. [31] Kimutatták, hogy az adiponektin hatását nagymértékben a zsírsav-oxidáció növekedése közvetíti, amely az AMPK és a PPAR-α útvonalak aktiválódásával és a TNF-α májtermelésének elnyomásával jár. [32,33] Köztudott, hogy az adiponektin és a TNF-a szabályozza a kölcsönös termelést és antagonizálja biológiai hatásukat a célszövetekre. Bár ismert, hogy a krónikus etanolfogyasztás megnövekedett keringési és helyi TNF-α koncentrációhoz vezet, [34,35] továbbra sem tisztázott, hogy az etanol adagolásából származó megnövekedett TNF-α adiponektin-redukciót eredményez-e, vagy az adiponectin termelésének etanollal történő elnyomása TNF-α indukció.
Az adenozin-monofoszfáttal aktivált protein-kináz szerepe
Az AMPK köztudottan kulcsfontosságú metabolikus „master kapcsolóként” működik, mivel számos szövetben, beleértve a májat is, foszforilezi a lipidanyagcserében részt vevő célenzimeket. Ezt az enzimet, egy heterotrimer fehérjét, maga az AMP, valamint a máj-kináz B-1 foszforilezése aktiválja. [36] Amikor az AMP aktiválja az AMPK-t, az lefelé szabályozza az energiaigénylő utakat, általában a lipid-, RNS- és fehérjeszintézist. Ezzel szemben az AMPK aktiválja az ATP-t generáló katabolikus utakat, például a zsírsav oxidációt, a TCA ciklust és a glikolízist. [37] Foszforilálja és gátolja a lipidanyagcserében részt vevő enzimeket, például a 3-hidroxi-3-metil-glutamát-CoA reduktázt és az acetil-CoA karboxilázt (ACC). [38] A lipidmetabolizáló enzimek aktivitásának közvetlen szabályozása mellett az AMPK modulálja az SREBP-1 aktivitását is, [39] amely fontos szerepet játszik a zsírsavszintézisben.
Az AMPK fehérje-foszfatáz 2A (PP2A) defoszforilezése okozza az AMPK inaktiválódását. Ezt a PP2A-t ceramiddal lehet aktiválni, amelyről ismert, hogy az etanol beadása után megnő. [40–42] Így az etanol növeli a ceramid szintjét, így növeli a PP2A aktivitást, ami viszont gátolja az AMPK aktivitást és növeli a zsírsav szintézist.
Hepatikus TG-k: Exportálás VLDL-be és tárolás LD-kben
A szabad zsírsavak fokozott szintézise az alkoholisták májában, valamint a máj csökkent képessége ezen vegyületek oxidálására a TG, a máj fő zsírraktározási formájának fokozott szintéziséhez vezethet. A TG-ként tárolt zsírsavakat ezután nagyon kis sűrűségű lipoproteinek (VLDL) részecskékbe importálják, amelyeket a szérumban exportálnak és szállítanak a perifériás szövetekbe. A VLDL-ben exportálható zsír mennyisége függ a fehérjekomponensek szintézisétől és a TG-k elérhetőségétől. A felesleges TG-ket lipidcseppekként (LD) tárolják a májban. [43]
Az etanol rontja a máj nagyon alacsony sűrűségű lipoproteinek szekrécióját
A lipidcseppek anyagcseréjének zavara
Következtetés
- A Sirt1 megcélzása magas zsírtartalmú étrend okozta alkoholmentes zsírmájbetegség patkánymodelljében
- Az étrend és az alkoholmentes zsírmájbetegség kapcsolata Felülvizsgálati cikk
- Az étrendi kalóriák, zsírok és vas korlátozása javítja az alkoholmentes zsírmáj betegségeket - PubMed
- Neurodegeneráció fiatalkori ibériai sertésekben étrend által kiváltott alkoholmentes zsírmájbetegségben
- Gyógynövények és aktív vegyületeik zsírmájbetegségek esetén