Biomarkerek a Helicobacter pylori fertőzésre és a gastroduodenalis betegségekre
Seiji Shiota
1 Környezeti és megelőző orvoslás tanszék, Oita Egyetem Orvostudományi Kar, Yufu City, Oita, Japán
Yoshio Yamaoka
1 Környezeti és megelőző orvoslás tanszék, Oita Egyetem Orvostudományi Kar, Yufu City, Oita, Japán
2 Orvostudományi Intézet - Gasztroenterológia, Baylor College of Medicine és Michael Eeast Debakey Veterans Affairs Medical Center, 2002 Holcombe Blvd, Houston, TX 77030, USA
Absztrakt
A Helicobacter pylori fertőzés a gyomorrák fő oka. Bár a H. pylori fertőzött alanyok azonosítása az első megközelítés a gyomorrák magas kockázatú populációjának meghatározásában, a H. pylori antitestek jelenléte nem elegendő a gyomorrák szűréséhez. A H. pylori fertőzött alanyok közül csak a fertőzöttek egy részénél alakul ki gyomorrák. A H. pylori fertőzés szerológiai markerei potenciális előrejelzőkként szolgálhatnak a gyomorrák kialakulásában. Beszámoltak arról, hogy a szérum vagy a vizelet H. pylori antitestjei, a citotoxinnal társított A gén A antitestek, a pepszinogén és a mikroRNS-ek összefüggenek a rákot megelőző elváltozásokkal vagy a gyomorrákkal. Ebben az áttekintésben összefoglaltuk az egyes stratégiák hasznosságait és korlátait.
A gyomorrák az ötödik leggyakoribb rák és a harmadik vezető oka a rákkal kapcsolatos halálozásnak a világon (ez elérhető a Nemzetközi Rákkutató Ügynökségnél is; GLOBOCAN2012 [1]). A Helicobacter pylori fertőzés a krónikus gyomorhurut, a peptikus fekélyek és a gyomorrák fő oka [2]. Noha a világ népességének körülbelül a fele fertőzött ezzel a baktériummal, a fertőzött személyek csak kisebb részénél alakul ki gyomorrák [3]. A H. pylori fertőzés változó eredményeinek egyik lehetséges oka a H. pylori törzsek virulenciájában mutatkozó különbségekhez kapcsolódik a gazda, a környezeti és az étrendi tényezők mellett. A személyre szabott megelőzés szempontjából nagyon kívánatos a kockázati markerek azonosítása a H. pylori-fertőzött betegek magas és alacsony kockázatú csoportokba sorolásához. Különösen a H. pylori fertőzés szerológiai markerei szolgálhatnak a gyomorrák kialakulásának potenciális előrejelzőjeként. Ebben az áttekintésben a H. pylori fertőzés szerológiai és vizeleti biomarkereire összpontosítottunk.
Anti-H. pylori antitest
Azokon a területeken, ahol a H. pylori fertőzés alacsony előfordulási gyakorisággal rendelkezik, a H. pylori fertőzött alanyok szűrése elegendő lehet a gyomorrák magas kockázatú populációjának szűkítésére. Azonban azokon a területeken, ahol a H. pylori fertőzés elterjedt, különösen a kelet-ázsiai országokban, a H. pylori fertőzöttek csak egy részénél alakul ki súlyos gasztroduodenális betegség, beleértve a gyomorrákot is; ezért a H. pylori antitestek jelenléte nem elegendő a gyomorrák magas kockázatú populációjának azonosításához. További szűrőeszközökre van szükség a gyomorrák magas kockázatú lakosságának azonosításához.
Nagyszabású kohorszos vizsgálatot végeztek a H. pylori antitest-titerek és a gyomorrák közötti összefüggés vizsgálatára Japánban, amelyben a gyomorrák előfordulása magas (29,9 eset/100 000 évente) [1,11]. Összesen 36 745 alany vett részt a Japán Egészségügyi Központ alapú prospektív tanulmányból, és 15 évig követték nyomon. A nyálkahártya atrófiája nélküli H. pylori szeropozitív alanyok közül a magas H. pylori antitest-titerrel rendelkező alanyok voltak a legnagyobb a gyomorrák kockázatának. Azonban a pepszinogén (PG) szintje alapján meghatározott nyálkahártya atrófiában szenvedő szeropozitív alanyok közül az alacsony H. pylori antitest titerűeknél volt a legnagyobb a gyomorrák kockázata. Ezért a nyálkahártya atrófiája mellett alacsony H. pylori antitest titerű betegeket a gyomorrák rendkívül magas kockázatú populációjának tekintették.
Citotoxin-asszociált gén A antitestek
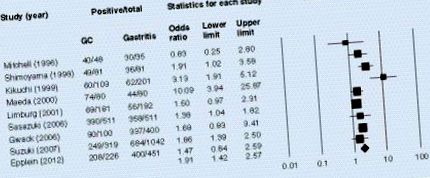
A legjobban tanulmányozott H. pylori virulencia faktor a citotoxinnal társított gén A (CagA) fehérje [19]. Számos jelentés jelezte, hogy a CagA-pozitív törzsek szignifikánsan összefüggenek a súlyos klinikai kimenetelekkel, különösen a nyugati országokban [20–23]. Huang és mtsai. metaanalízis elvégzésével vizsgálta a CagA szeropozitivitás és a gyomorrák közötti összefüggést [24]. Megállapították, hogy a szérum CagA antitestek szignifikánsan társultak a gyomorrákhoz, amikor nyugati és ázsiai országokból származó tanulmányokat is bevontak. Kelet-ázsiai országokban szinte az összes H. pylori törzs rendelkezik cagA-val és CagA fehérjét termel; ezért nehéz bemutatni a CagA jelentőségét a gyomorrákban. Például korábbi jelentésünkből kiderült, hogy a japán törzsek 96,3% -a volt cagA-pozitív a klinikai eredményektől függetlenül [25]. Hasonló eredményeket találtak Japán [26–28] és más kelet-ázsiai országok [29,30] különböző régióiban. A CagA-pozitív H. pylori fertőzöttek azonban még mindig kelet-ázsiai országokban sem mindig termelnek szérum CagA antitesteket. Korábbi tanulmányunk azt mutatta, hogy a japán alanyok 75,0% -ánál találtak szérum CagA antitesteket [31]. Ez arra utal, hogy a szérum CagA antitestek a cagA jelenléte helyett megfelelő biomarkert jelenthetnek.
A szérum citotoxin-asszociált gén A antitestek jelenléte szignifikánsan társult a gyomorrákkal egy véletlen hatású modellben egy metaanalízis során.
Korábbi vizsgálatunkban megvizsgáltuk a szérum CagA antitesttiterek és a szövettani pontszámok kapcsolatát Japánban [31]. Érdekes módon a szérum CagA antitest titer szignifikánsan korrelált a gyomor nyálkahártya gyulladásával a korpuszban. Ez arra utal, hogy mind az antitestek, mind az antitest-titerek biomarkerek a nagy kockázatú populáció körülhatárolásához. Eközben Suzuki és mtsai. a gyomorrák kockázatát vizsgálta a japán CagA antitest-titerek szerint [36]. Ezek között 299 noncardia gyomorrákban szenvedő beteg és 1048 egyeztetett kontroll szerepelt. A H. pylori-szeropozitív alanyok közül az alacsony CagA antitest-titerrel rendelkezőknél nagyobb volt a jövőbeli noncardia gyomorrák kockázata, mint a szérum CagA negatív vagy magas CagA antitest titerűeknél. Ezek az adatok azt sugallják, hogy a szeropozitivitás mellett figyelmet kell fordítani az antitest-titerre.
Nemrégiben Pan és mtsai. megvizsgálta a CagA, VacA, GroEL, az ureáz A alegység (UreA), a γ-glutamil-transzpeptidáz (gGT) és a HcpC szeropozitivitása és a gyomor elváltozások kialakulása közötti összefüggést az utánkövetési periódus alatt olyan betegeknél, akiknél a alapvonal [47]. Az antitestek jelenlétét minden specifikus antigén esetében a recomLine H. pylori tesztrendszer alkalmazásával vizsgáltuk, amely egy vonali immunvizsgálat. A CagA, VacA, GroEL, UreA, HcpC és gGT szeropéldányai 83,9, 38,9, 66,1, 17,8, 59,7 és 43,3% voltak. A CagA elleni szeropozitivitás független prediktor volt a fejlett gyomorelváltozásokra. Ezenkívül azt tapasztalták, hogy a CagA és a GroEL szeropozitivitása független előrejelzője volt a gyomorelváltozások progressziójának egy utólagos vizsgálatban. Ezek az eredmények hasznosak lehetnek a H. pylori-fertőzött populáció gyomorrák magas és alacsony kockázatú populációiba történő rétegzéséhez.
PG & ABC osztályozás
A gyomorrák kockázatát a H. pylori fertőzés jelenléte és a gyomornyálkahártya atrófia állapota alapján osztályozhatjuk [50]. Különösen a H. pylori szerológia, a PG I szintek és a PG I/II arány kombinációja használható a gyomorrák szűrésére, amelyet Japánban ABC módszerként neveznek [12,51]. Az ABC módszerben az alanyokat a H. pylori fertőzés és a PG jelenléte alapján négy csoportba sorolhatjuk: A csoport (H. pylori negatív és PG negatív), B csoport (H. pylori pozitív és PG negatív) ), C csoport (H. pylori pozitív és PG pozitív) és D csoport (H. pylori negatív és PG pozitív) [12]. A gyomorrák kialakulásának általában a D csoportot tekintik a legmagasabb kockázati csoportnak, ezt követi a C, B és A csoport [12].
Korábban megvizsgáltuk az ABC besorolás állapotát Bhutánban, ahol a gyomorrák előfordulása magas [52]. A B csoportban (53,8%) és a C csoportban (17,3%) a betegek aránya magasabb volt a bhutánoknál, mint Japánban, ahol az értékek 16,3, illetve 9,3% voltak [12]. Még a fiatalabb alanyokban is a C csoportba tartozó alanyok aránya megközelítőleg 20% volt Bhutánban, ami magasabb volt, mint Japánban (≤5%) [53]. Ez arra utal, hogy a súlyos gyomor atrófia magas előfordulása Bhutánban hozzájárulhatott a gyomorrák magas előfordulásához Bhutánban.
Yanaoka és mtsai. PG-t használva megvizsgálta a H. pylori felszámolási terápia megelőző hatását a gyomorrák kialakulására longitudinális kohortos vizsgálatban [54]. Összesen 473 H. pylori irtott és 3656 tartós fertőzésben szenvedő személyt követtek nyomon körülbelül 10 éven keresztül. Az alanyokat három csoportra osztottuk a krónikus atrófiás gastritis jelenléte alapján, PG alapján. Az enyhe krónikus atrófiás gyomorhurutban szenvedő PG-negatív csoportban a gyomorrák előfordulása szignifikánsan alacsonyabb volt a H. pylori felszámolt csoportban, mint a nem radikált csoportban. Éppen ellenkezőleg, a gyomorrák előfordulási gyakoriságában nem találtunk különbséget a PG-pozitív csoportban a H. pylori felszámolt és nem permetezett alanyok között. Ez arra utal, hogy a H. pylori felszámolási terápia csökkentheti a gyomorrák előfordulását súlyos krónikus atrófiás gyomorhurut nélküli személyeknél. Ez a megállapítás azt is alátámasztja, hogy a PG elérhető lehet a gyomorrák kialakulásának nagy kockázatú alanyok azonosítására.
A PG-k legjobb határértéke azonban a beteg hátterétől függően változhat [55]. Valójában az indiai alanyok alacsonyabb PG-szintet mutattak, mint a kínai és a malajziai populációk, még a szex és a H. pylori fertőzés arányának kiigazítása után is [56]. Ezért a szérum PG-szint nem használható gyomorrák szűrésére az indiai populációban [57]. A PG I és a PG II szintjét más tényezők is befolyásolhatják, például életkor, nem, testmagasság, testtömeg, testfelület, dohányzási és ivási szokások [48]. A kínai populációban az atrófiás gasztritisz kimutatására vonatkozó PG I és PG I/II arány határértékei 82,3 ng/ml, illetve 6,05 voltak. A PG-k megfelelő határértékeit minden populációban meg kell határozni [51,55].
A gyomorrákhoz kapcsolódó egyéb tényezők
A nem invazív biomarkereket a H. pylori felszámolási terápia után is alkalmazni kell. Shiotani és mtsai. a szérum miRNS szintjét olyan betegeknél vizsgálták, akiknek korai gyomorrákos megbetegedéseinek endoszkópos reszekciója nemrégiben fordult elő, és kontroll alanyokban (H. pylori-pozitív gyomorfekély vagy atrófiás gyomorhurut) a japán H. pylori felszámolási terápia előtt és után [62]. Megállapították, hogy a miR-106b és a let-7 szintje szignifikánsan magasabb volt a gyomorrákos betegeknél, mint a kontroll alanyokban, függetlenül a kórtörténetétől. Ezzel szemben a miR-21 szint magasabb volt a gyomorrákos betegeknél, mint a kontroll alanyoknál, csak az eradikációs terápia után. Ezek az eredmények arra utalnak, hogy a miRNS szintje megváltozhat a H. pylori felszámolási terápia után. Ezenkívül szem előtt kell tartanunk azt a lehetőséget, hogy a gyomorrák nagy kockázatának kitett személyek kimutatására a legalkalmasabb biomarkerek a populációtól függően eltérőek lehetnek.
A glycomics a gyomorrák érzékeny diagnosztikai eszközét is jelentheti. Ozcan és mtsai. a natív glükánokat vizsgálták SM-ben a mexikói gyomorrákban és nonatrophiás gastritisben szenvedő betegek szérumában [63]. Ennek eredményeként 19 glikán társult gyomorrákkal. Különösen három csoport szintje volt, ideértve a magas mannóz típusú glikánokat, az 1 komplex típusú antennával rendelkező glikánokat és a bigalaktozilezett kétévenkénti glikánokat gyomorrákos betegeknél alacsonyabb, mint a nonatrophiás gyomorhurutban szenvedőknél, míg a nongalaktozilezett kétéves glikánok gyomorrákban szenvedő betegeknél. Ezek a glikánok alkalmasak lehetnek a gyomorrák korai stádiumában történő kimutatására.
H. pylori fertőzéssel összefüggő egyetlen nukleotid polimorfizmusok
Magas expozíciós arány mellett is a populáció körülbelül 5–10% -a soha nem fertőzött H. pylori-val. Érdekes módon a H. pylori szerológiai státuszával összefüggő genetikai lókuszok azonosítását egy németországi genom-szintű asszociációs vizsgálatban végezték [64]. Két független népességalapú kohorszból összesen 10 938 alany került be. A szeropozitív arány 56,3% volt. A 4p14-es Toll-szerű receptor (TLR) lókusz és az 1q23.3-on az Fcγ-receptor 2a-lokuszt kódoló FCGR2A a H. pylori szeropozitivitással társult. Valójában a magas fekális H. pylori antigén titer magas TLR1 expressziós szinttel társult, ami arra utal, hogy a TLR1 okozati összefüggésben lehet H. pylori érzékenységgel. Ezek a megállapítások hozzájárulhatnak a H. pylori fertőzés magas kockázatú populációinak szűréséhez.
Hogyan lehet azonosítani a gyomorrák magas kockázatú populációját?
Következtetés
A Helicobacter pylori fertőzés a gyomorrák fő kockázati tényezője. Ezért fontos a H. pylori-pozitív alanyokat szűrési stratégiaként azonosítani. A H. pylori-fertőzöttek körében azonban csak a fertőzöttek egy részénél alakul ki gyomorrák. A szérum H. pylori antitest és a PG szint kombinációja hasznos lehet a H. pylori fertőzött alanyok gyomorrák magas kockázatú populációjának kimutatására. Ezenkívül a H. pylori fehérje elleni egyéb antitestek hasznosabbak lehetnek a magas kockázatú populáció körülhatárolásában. A legújabb vizsgálatok jelentős különbségeket tártak fel a miRNS-ek szérum/plazma szintjében a gyomorrákos betegek és a kontroll alanyok között. E tesztek előnyeit és hátrányait az 1. táblázatban foglaltuk össze. További prospektív kohorsz vizsgálatok szükségesek e tesztek fontosságának tisztázásához. Nem szabad megfeledkeznünk arról, hogy a nem invazív biomarkerek a célpopulációktól és a tesztkészletektől függően változhatnak. Ezenkívül a biomarkerekkel kapcsolatos pozitív eredményeket tartalmazó tanulmányok könnyen közzétehetők a negatív eredményekkel összehasonlítva, különösen a retrospektív vizsgálatok (publikációs torzítás) [67]. A szabványosított protokollok javíthatják a vizsgálatok megbízhatóságát.
Asztal 1
Biomarkerek a Helicobacter pylori fertőzésre és a gastroduodenalis betegségekre.
| Szérum Helicobacter pylori antitest | Könnyen használható epidemiológiai kutatásokhoz |
A jövő perspektívája
Jóllehet a H. pylori felszámolási terápia csökkentheti a gyomorrák előfordulását, nem tudja teljesen megakadályozni a gyomorrák kialakulását, különösen a rákot megelőző elváltozásokban szenvedő betegeknél. Alapvetően minden H. pylori-fertőzött alanynak nagy a kockázata a gyomorrák kialakulásának. Valójában a japán egészségbiztosítási rendszer 2013-ban jóváhagyta a H. pylori felszámolási terápiát minden H. pylori-val összefüggő krónikus gyomorhurutban szenvedő alany számára. Ezért fontos meghatározni a H. pylori felszámolási terápia után a betegek magas kockázatú populációját. A noninvazív tesztek sok populáció számára alkalmazhatók nagyobb kényelmük és egyszerű használatuk miatt. A tesztkészlet optimális határértékét minden egyes populációban és országban külön kell meghatározni. Ezenkívül a helyi H. pylori törzsek használata javíthatja a helyi specifikus tesztkészletek pontosságát. A legújabb tanulmányok azt illusztrálták, hogy számos miRNS lehet a gyomorrák biomarkere. Meg kell azonban fontolni a zavaró hatások vagy interakciók lehetőségét a független kockázati tényezők tisztázása érdekében. Ezenkívül prospektív vizsgálatokra van szükség a miRNS-ek jelentőségének tisztázásához a korai gyomorrák kimutatásában.
Vezetői összefoglaló
Szérum Helicobacter pylori antitest
A Helicobacter pylori antitestek prevalenciája szignifikánsan magasabb volt gyomorrákos betegeknél, mint kontroll alanyoknál.
Alacsony H. pylori antitest-titerrel és nyálkahártya-atrófiával rendelkező betegek a gyomorrák rendkívül magas kockázatú populációját képezték.
Fontos, hogy a H. pylori antitest titerek nagymértékben változtak az alkalmazott tesztkészlettől függően. Ezért előnyösebb egy helyi ELISA kit kifejlesztése helyi H. pylori törzsek felhasználásával.
Húgyúti H. pylori antitest
A H. pylori fertőzés kimutatására két vizeletvizsgálatot, enzim immunoassay és immunokromatográfiás módszert alkalmaztak.
A vizeletvizsgálati készletek pontossága a betegcsoporttól és országtól függően is változhat. Ezért jobb, ha tesztkészleteket fejlesztünk ki úgy, hogy helyi törzseket használunk antigénforrásként a legjobb vizsgálati teljesítmény elérése érdekében.
CagA antitest
A cagA-pozitív H. pylori fertőzöttek még mindig kelet-ázsiai országokban sem mindig termelnek szérum CagA antitesteket.
A CagA szeropozitivitás jelentősen társult a gyomorrákkal, még kelet-ázsiai országokban is, egy metaanalízis során.
A szérum CagA antitest titerek az alkalmazott ELISA kit szerint eltérhetnek.
PG & ABC osztályozás
A szérum PG-t a gyomor nyálkahártya-státuszának jelzőjeként azonosították, beleértve az atrófiát és a gyulladást.
A H. pylori szerológia, valamint a szérum PG I szintjének és a PG I/II arányának mérése kombinációja alkalmazható a gyomorrák szűrésére.
Egyéb biomarkerek
A szérum/plazma miRNS-ek vagy glikánok új noninvazív biomarkerként szolgálhatnak a gyomorrák kimutatására H. pylori fertőzött alanyokban.
Köszönetnyilvánítás
Ez a jelentés azon munkán alapul, amelyet részben az NIH (DK62813; Y Yamaoka), a Japán Oktatási, Kulturális, Sport-, Tudományos és Technológiai Minisztérium (MEXT) tudományos kutatási támogatásai támogattak (22390085, 22659087, 24406015 és 24659200; Y Yamaoka; 23790798; S Shiota), Stratégiai Fiatal Kutató Tengerentúli Látogatási Program az agyi keringés felgyorsítására Japánban a Tudománytámogató Társaság számára (JSPS), a japán tudomány és a technológia előmozdításának stratégiai alapjai és Technológiai Ügynökség (JST).
Lábjegyzetek
Pénzügyi és versengő érdekek nyilvánosságra hozatala
A szerzőknek nincs más releváns kapcsolata vagy pénzügyi közreműködése olyan szervezetekkel vagy szervezetekkel, amelyek pénzügyi érdekeltséggel rendelkeznek vagy pénzügyi konfliktusban vannak a kéziratban tárgyalt témával vagy anyagokkal, a közzétetteken kívül.
A kézirat elkészítéséhez nem használtak írásbeli segítséget.
Hivatkozások
A különös figyelmet érdemlő dolgozatokat a következők kiemelték: • érdeklődésre számot tartó;
- Bakteriális vaginosis mint vegyes fertőzés - polimikrobiális betegségek - NCBI könyvespolc
- Amebiasis (Entamoeba histolytica Infection) meghatározása, tünetei, kezelése
- A sinus fertőzés nyomorának száműzése Andrew Weil, M
- 4 éves krónikus gyomorhurut - Segítség keresése - Helicobacter fórumok
- Vérszegénység hemotróp mikoplazma fertőzésben szenvedő macskáknál 23 eset retrospektív értékelése (1996–2005)