Superior vena cava szindróma, amelyet Hodgkin-limfóma okoz egy serdülő lányban
Imran Rizvi
1 Általános Orvostani Osztály, J N Orvosi Főiskola, Aligarh, UP, India
Samsuz Zaman
2 Pathology Department, J N Medical College, Aligarh Muslim University, Aligarh, UP, India
Noorin Zaidi
2 Pathology Department, J N Medical College, Aligarh Muslim University, Aligarh, UP, India
Syed Mohammad Kamil Ashraf
1 Általános Orvostani Osztály, J N Orvosi Főiskola, Aligarh, UP, India
Arun Kumar
1 Általános Orvostani Osztály, J N Orvosi Főiskola, Aligarh, UP, India
Ankush Gupta
3 Általános Orvostani Osztály, Katonai Kórház, Jodhpur, Jodhpur, India
Mehtab Ahmad
4 Radiodiagnosis Department, J N Medical College, Aligarh Muslim University, Aligarh, UP, India
Absztrakt
Egy 14 éves női beteg légszomj, felsőtest duzzanata és diszfágia panaszaival jelentkezett előttünk, a felső testen kiemelkedő vénák voltak láthatóak. A mellkas CT-vizsgálata nagy mediastinalis tömeget eredményezett, amely összenyomta a környező struktúrákat. A hisztopatológia és az immunhisztokémia megerősítette, hogy ez Hodgkin-limfóma. A beteg kemoterápiát (doxorubicint, bleomicint, vinblasztint és dakarabazint) és helyi sugárterápiát kapott. Jelenleg jól teljesít.
Háttér
A felső vena cava szindróma (SVCS) a felső mediastinum domináns fő érösszenyomódására utal. Amikor az érösszenyomás társul a légcső tömörítéséhez, akkor ezt „felsőbb mediastinalis szindrómának” (SMS) nevezik. 1 A gyakorlatban az SVCS-t és az SMS-t gyakran szinonimán használják. Az SVCS gyermekeknél ritkán fordul elő, és rosszindulatú mediastinalis daganatokban szenvedő gyermekek 12% -ánál jelenik meg. 2 Bár a limfómák az SVCS gyakori okai, de szinte mindig az SVCS-t a nem Hodgkin-limfóma (NHL) okozza. A Hodgkin-lymphoma (HL) a mediastinalis lymphadenopathiával való közös megjelenése ellenére is ritkán okozza az SVCS-t. 3 Az alábbiakban bemutatott eset áttekinti az SVCS klinikai megjelenését, okait, diagnózisát és kezelését, különös tekintettel a HL-re.
Eset bemutatása
Vizsgálata során pulzusa 110/perc volt, a vérnyomás 110/70 Hgmm, a légzési sebesség 28/perc, a hőmérséklet 98,4 ° F volt. Általános vizsgálat során markáns arcödéma volt, a felső végtagok és a mellkas falán duzzanatot is észleltek. Nem volt sápadtság, cianózis, ütődés vagy icterus, az alsó végtagokon nem volt ödéma. Nyaki vénái kitágultak, a nyaki vénás nyomás (JVP) megemelkedett, de nem pulzáló, kiemelkedő vénák voltak a mellkas egész falán, és ezekben a vénákban felülről lefelé áramlott. A légzőrendszer vizsgálata során az infraclavicularis, suprascapularis és interscapularis területeken tompa volt a mellkas jobb oldala feletti ütés, az ezeken a területeken csökkent a vokális rezonancia és a vokális fremitus, valamint csökkent a légzési hangok intenzitása. A szegycsont felső része is tompa volt az ütőhangszereken. A légzőrendszer többi vizsgálata a normális határokon belül volt. A kardiovaszkuláris, a központi idegrendszeri és a hasi vizsgálatok szintén normálisak voltak. Jelentős lymphadenopathia nem volt jelen a nyak, hónalj vagy inguinalis régióban.
A felsőtest duzzanata, a nyak és a mellkas tágult vénái, dyspnoe és dysphagia klasszikus klinikai jellemzői alapján ideiglenesen diagnosztizálták az SVC/SMS-t, és tovább vizsgálták.
Vizsgálatok
Hemoglobinja 11 g/dl, a teljes leukocita szám 9800/mm 3, a differenciál leukocita szám neutrofilek 76% és a limfociták 24%. Egyéb biokémiai tesztek, például a máj- és vesefunkciós tesztek a normál határokon belül voltak.
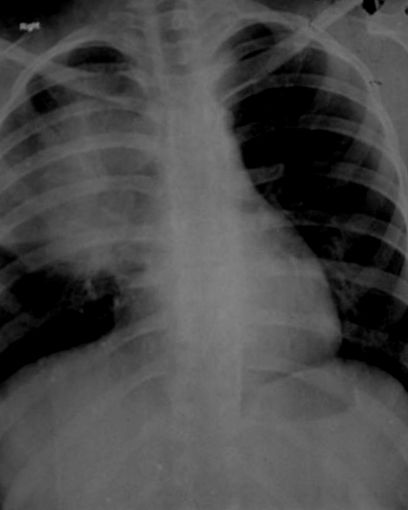
Röntgen mellkas hátsó elülső képe a jobb oldali paratrachealis csík széles, jól körülhatárolható lágyrész-sűrűségű elváltozással a jobb felső és középső tüdőzónában.
Postkontrasztos CT képek a bal brachiocephalicus véna és az aorta íve kereszteződésének szintjén, amely egy nagy, homogén módon fokozó tömeges elváltozást mutat az elülső mediastinumban, amely összenyomja és elmozdítja a szomszédos jobb tüdőt, valamint a brachiocephalicus vénák és a vena cava superior összenyomódása.
Reed – Sternberg sejtek bőséges citoplazmával és nagy kerek maggal, vastag membránnal és hatalmas, hiperkromatikus maggal. Gyakori limfociták és hisztiociták, amelyek a háttérsejt populációt tartalmazzák (H&E, 400x).
CD15 pozitivitást mutató immunhisztokémiai folt.
Kezelés
A hisztopatológiai jelentésre várva megkezdtük a kezelést a fej végének megemelkedése, injekciós furoszemid, injekciós dexametazon formájában. A beteg ésszerű tüneti enyhülést kapott ettől a kezeléstől csökkent ödéma és javuló légszomj formájában. A HL histopatológiai megerősítése után a beteget a legközelebbi onkológiai intézetbe irányították, ahol kemoterápiás kezelést kaptak, beleértve doxorubicint, bleomicint, vinblasztint és dacarabazint (ABVD), majd helyi sugárterápiát.
Eredmény és nyomon követés
A betegnek jelenleg jól megy, és rendszeres nyomon követés alatt áll.
Vita
Az SVC a jobb és a bal brachiocephalicus vénák egyesülésével jön létre, és a jobb pitvarba ürül, ez a fő vénás elvezetési rendszer a felső végtagokból, a fejből és a nyakból visszatérő vér számára. Mivel az SVC nem átdiszkálható térben (azaz a mediastinumban) fekszik, hajlamos a daganatok és a mediastinalis lymphadenopathia által történő kompresszióra. Az SVCS-esetek többségében rosszindulatú daganatok, például tüdőrák, limfóma és áttétes daganatok felelősek. A tüdőrák, különösen a kissejtes és a laphámsejt-szövettan, az SVCS rosszindulatú eredetének összes esetének 85% -át teszi ki. 3 Fiatal korban a malignus lymphoma az SVCS vezető oka. A HL gyakrabban veszi igénybe a mediastinumot, mint bármely más lymphoma, de ritkán okozza az SVCS-t. 3 Az SVCS egyéb okai közé tartozik a központi vénás hozzáférés miatti trombózis, pacemaker/defibrillátor vezetékek, aorta aneurysma, thyromegalia és a korábbi besugárzás vagy hisztoplazmózis következtében fellépő fibrosz mediastinitis. 3
Az SVCS-t a jelek és tünetek összegyűjtése jellemzi, beleértve a dyspnoét, az arc, a nyak, a felsőtest és a karok köhögését és duzzadását. Ritka esetekben a betegek rekedtségre, mellkasi fájdalomra, dysphagiára és haemoptysisre panaszkodhatnak. A fizikai tünetek közé tartozik a nyaki vagy mellkasi vénák kiemelkedése, az arc vagy a karok folyadékgyűjtése és a gyors légzés. Ritkán cyanosis, Horner-szindróma (miózis, ptosis és egyoldalú anhydrosis) és megbénult hangszalag is jelen lehet. 4 Betegünknél dyspnoe, az arc, a nyak, a felsőtest és a karok duzzanata, valamint a kiemelkedő nyaki és mellkasi vénák is jelentkeztek.
A tüneteket súlyosbítja fekvés vagy előrehajlás. Pemberton jele az arc rengetegének, a belégzési stridornak és a nem pulzáló JVP-emelkedésnek a kialakulása, amikor az SVCS-ben szenvedő beteg a karját a feje fölé emeli. A diszfágia, a rekedtség és a stridor nem az SVC kompressziójának köszönhető, de a jelenlét más mediastinalis struktúrák (nyelőcső, gégeidegek és a légcső) összenyomódását jelenti, ezen tünetek jelenléte rossz prognózissal korrelál.
A CT nagyon hasznos az SVCS-ben szenvedő betegek értékelésében, mivel pontosan lokalizálja az elváltozás helyét, és mediastinoscopy, bronchoscopy és perkután aspiráció segítségével irányíthatja a biopsziára tett kísérleteket. A mediastinum MRI-nek számos potenciális előnye van a CT-vel szemben, beleértve a kép több képsíkon történő képalkotásának és a véráramlás közvetlen megjelenítésének képességét, és az MRI nem igényel jódozott kontrasztanyagot sem. Az MRI hátrányai közé tartozik a megnövekedett szkennelési idő és költség. 5.
Kívánatos és a legtöbbször lehetséges, hogy a malignus betegség szövettani diagnózisát felállítsák a kezelés megkezdése előtt. A megalapozott szövetdiagnózis nélküli kezelést csak akkor szabad elkezdeni, ha a tünetek gyorsan progresszívek, vagy ha a szövetdiagnózis felállítására irányuló korábbi próbálkozások sikertelenek. 5 Az orvosnak szem előtt kell tartania, hogy a végső kezelési stratégia a diagnózistól függően változik, és a kezelés kezdeti modalitása nem veszélyeztetheti a végleges tervet. Például SVCS-ben szenvedő limfómás betegeknél a sürgősségi sugárkezelés veszélyeztetheti a tumor immunhisztokémiai markerekkel történő kategorizálásának képességét, és késleltetheti a szisztémás kemoterápia beadását. 5 A fenti kérdést szem előtt tartva, a terápia megkezdése előtt kértük a diagnózis kóros megerősítését.
Az SVCS-ben szenvedő betegek további hasznos vizsgálata a köpet citológiája, a tapintható supraclavicularis csomók biopsziája és a bronchoscopia.
Az olyan támogató intézkedések, mint a fej végének megemelkedése, az oxigén belélegzése és a vizelethajtók, bármilyen okból hasznosak lehetnek az SVCS-ben szenvedő betegeknél, a dexametazon tüneti enyhítést is nyújt az ödéma és a tumorterhelés csökkentésével az SVCS rosszindulatú okaiban. Akut thrombus jelenlétében thrombolysis javallt. A katéter által kiváltott SVCS kezelhető antikoagulánsok, trombolízis és endovaszkuláris kezelés segítségével. A rosszindulatú daganatos betegeknél, mint az SVC szindróma forrásától, a sugárzás és a kemoterápia enyhítheti a tüneteket. A műtét segíthet, ha az orvosi vagy az intervenciós kezelések sikertelenek. Betegünk reagált a fent említett támogató intézkedésekre is.
A HL a rosszindulatú daganatok egyik leggyakoribb formája fiatal felnőtteknél, akiknek átlagos életkora a diagnózis felállításakor 32 év. A HL két fő típusa a klasszikus HL és a limfocitákban domináns HL, a klasszikus HL további négy altípusra oszlik, mégpedig noduláris szklerózisra, vegyes cellularitásra, gazdag limfocitákban és kimerült limfocitákra. A klasszikus HL az összes HL 95% -át teszi ki.
Korábban legalább egy klasszikus R – S sejt jelenlétét elengedhetetlennek tartották a HL végleges diagnosztizálásához, de az R – S sejt morfológiai azonosítását már nem tartják szükségesnek, mert a kiegészítő immunhisztokémiai vizsgálatok jellegzetes fenotípust eredményezhetnek a végleges diagnózis alátámasztására. a HL. 14
A formalin fix-paraffinba ágyazott szakasz immunhisztokémia a leghasznosabb kiegészítő vizsgálat a HL diagnosztizálásához. Az R – S sejtek CD15 és CD30 pozitív eredményt, CD45/45RB negatív eredményt mutatnak. A törzsspecifikus markerek közül a CD20 a klasszikus HL esetek körülbelül 25% -ában festi az R – S sejtek egy részét. A CD3 tesztelésének eredményei szinte mindig negatívak az R – S sejtekben. Csak ezen öt marker (CD15, CD30, CD45/45RB, CD20, CD3) használatával oldható meg a klasszikus HL legtöbb esete (> 90%). A fő különbség a klasszikus és a limfocita domináns HL között az, hogy az R – S sejtek CD15 + és CD30 + a klasszikus HL-ben, és CD15−, CD30− és CD20 + a limfocitákban domináns HL-ben. Betegünk immunhisztokémiai festése CD 15 pozitivitást is kimutatott.
A legtöbb HL-ben szenvedő betegeknél tapintható nyirokcsomó van, amely nem gyengéd, a legtöbb betegben ezek a nyirokcsomók a nyakon, a supraclavicularis területen és a hónaljban vannak. 15 A betegek több mint felének mediastinalis adenopathiája lesz a diagnózis felállításakor, és ez néha a kezdeti megnyilvánulás. 15 Annak ellenére, hogy a HL-SVC szindrómában a mediastinalis érintettség gyakran előfordul, ritkán fordul elő. 3 A betegek egyharmada lázas, éjszakai izzadással és/vagy fogyással jár. 15 A klinikai stádium Ann Annor osztályozással történik. 16.
Számos komplex prognosztikai faktor sémát dolgoztak ki a korlátozott Hodgkin-limfóma kezelésére, amelyet csak sugárterápiával kezeltek. A masszív mediastinalis betegséget és az alkotmányos tüneteket következetesen azonosították a visszaesés független előrejelzőjeként, míg az idősebb életkor csak az alacsonyabb rendű túlélést jelezte előre. 17 18
Egy nemzetközi konzorcium összesítette a betegek adatait, és hét tényező alapján azonosított egy előrehaladott Hodgkin-limfóma prognosztikai pontszámát. férfi nem, legalább 45 éves életkor, IV. stádium, fehérvérsejtszám legalább 15 000/µl, limfocita szám kevesebb mint 600/µl vagy 19 Az I. és IIA stádiumú betegek gyógyulási aránya közel 90%. Még előrehaladott betegség esetén is (IVA és IVB stádium) 60–70% -os 5 éves betegségmentes túlélés érhető el. 9.
A lokalizált vagy jó prognózisú betegek rövid kemoterápiás kezelést kapnak, amelyet sugárterápia követ a csomópont érintettségének helyéig. A kiterjedt betegségben szenvedők vagy a „B” tünetekkel rendelkező betegek teljes kemoterápiás kezelést kapnak. A HL-ben alkalmazott legnépszerűbb kemoterápiás rendszer a doxorubicin, bleomycin, vinblastin és dacarabazine (ABVD), valamint a mechlorethamine, vinkristin, prokarbazin és prednizolon (MOPP). 15
- Emlékeztető a fontos klinikai leckére A hasfal fájdalma elhízott nőknél gyakran hiányzott és
- Superior Vena Cava-szindróma
- Emlékeztető a fontos klinikai leckére Súlyos étrenddel kapcsolatos vashiányos vérszegénység egy 17 hónaposnál
- Superior mesenterialis artéria szindróma egészséges aktív serdülő BMJ esetjelentésekben
- Superior mesentericus artériás szindróma egy 6 éves kislányban, akinek a lisztérzékenysége diagnosztizálható