Két kreatinin-alapú egyenlet összehasonlítása a vesefunkció csökkenésének előrejelzéséhez koreai populációban a nephropathiás 2-es típusú cukorbetegeknél
Eun Young Lee
1 Belgyógyászati Klinika, Yonsei Egyetem Orvostudományi Főiskola, 50 Yonsei-ro, Seodaemun-gu, Szöul 120-752, Koreai Köztársaság
Young-Mi Lee
2 Belgyógyászati Klinika, Dongtan Jeil Női Kórház, 42-1 Seokwoo-dong, Hwasung, Gyeonggi-do 445-170, Koreai Köztársaság
Kyu Hun Choi
3 Nefrológiai osztály, Belgyógyászati Klinika, Yonsei Egyetem Orvostudományi Főiskola, 50 Yonsei-ro, Seodaemun-gu, Szöul 120-752, Koreai Köztársaság
Hyun Chul Lee
4 Endokrinológiai és anyagcsere osztály, Belgyógyászati Klinika, Yonsei Egyetem Orvostudományi Főiskola, 50 Yonsei-ro, Seodaemun-gu, Szöul 120-752, Koreai Köztársaság
Byung-Wan Lee
4 Endokrinológiai és anyagcsere osztály, Belgyógyászati Klinika, Yonsei Egyetem Orvostudományi Főiskola, 50 Yonsei-ro, Seodaemun-gu, Szöul 120-752, Koreai Köztársaság
Beom Seok Kim
3 Nefrológiai osztály, Belgyógyászati Klinika, Yonsei Egyetem Orvostudományi Főiskola, 50 Yonsei-ro, Seodaemun-gu, Szöul 120-752, Koreai Köztársaság
Absztrakt
1. Bemutatkozás
A krónikus vesebetegségek (CKD) növekvő előfordulása világszerte nagyobb aggodalmat ébreszt [1]. Korábbi tanulmányok a CKD növekvő tendenciáját az általános népesség gyors öregedésének és a cukorbetegség járványának terjeszkedésének tulajdonítják [1–3]. 1991 és 2001 között a diabéteszes nephropathia előfordulása megduplázódott az újonnan diagnosztizált végstádiumú vesebetegségben (ESRD) szenvedő betegek körében [4]. A közelmúltban egy kiemelkedő keresztmetszeti vizsgálat, amelyből 33 208, 2-es típusú cukorbetegségben (T2D) szenvedő beteg vett részt 33 országból, feltárta, hogy a mikro- és makroalbuminuria általános prevalenciája kb. 39%, illetve 10% volt [5]. A helyzetet tovább súlyosbítja, hogy a cukorbetegség által okozott ESRD előfordulása a becslések szerint 2015-re 70% -ra nő [4]. A T2D jól ismert a szív- és érrendszeri betegségek (CVD) és az ESRD vezető okaként [6]. Az is jól megalapozott, hogy a CKD kimutatták, hogy szorosan összefügg a CVD-vel kapcsolatos kórházi kezelés és halálozás, valamint az ESRD fokozott kockázatával, még a kardiovaszkuláris kockázati tényezők kiigazítása után is [1, 7, 8]. Ezért a CKD-ben szenvedő betegek korai felismerése további klinikai következményekkel járhat, nem csupán az ESRD-re való közeledő progresszió észlelésén, különösen a T2D-ben szenvedő betegeknél [9, 10].
2. Anyagok és módszerek
2.1. Betegek és tanulmányterv
Ebben a retrospektív kohorsz vizsgálatban kivontunk egy adatot egy nephropathiás, 2-es típusú diabéteszes alanyok elektronikus orvosi nyilvántartásának (EMR) adatbázisából, akiknél két vagy több szérum kreatinin-mérést végeztek 2000 július és 2012 szeptembere között a koreai szöuli Severance Kórházban. A 2-es típusú cukorbetegségben szenvedő betegeket az EMR adatbázisban az ICD-10 kód keresésével azonosították. A diabéteszes nephropathiára utal, hogy legalább egy mérés során olyan diabéteszes betegeket vontunk be, akiknek 24 órás vizeletalbumin-kiválasztása ≥ 30 mg/nap volt. A kiindulási adatokat olyan adatokként határoztuk meg, amikor a 24 órás vizeletalbumin kiválasztási szint először túllépte a 30 mg/nap értéket. A betegeket kizárták, ha a kiinduláskor vesepótló kezelésen estek át, vagy ha 18 évnél fiatalabbak voltak. A kiindulási adatok kivonása után a betegeket retrospektíven követték két meghatározott végpont eléréséig: 2013 májusáig (idõpont) vagy a vesefunkció csökkenésének vagy halálesetéig (klinikai kimenetel végpontja). Azoknál az alanyoknál, akiket a nyomon követés miatt elvesztettek, az utolsó látogatásukig kapott adatokat is belefoglaltuk.
Az elsődleges eredményt a vesefunkció csökkenése alapján értékelték, és a kiindulási szérum kreatininszint megduplázódásaként határozták meg. A kiindulási szérum kreatininszint megkétszereződését a szérum kreatininszint kétszeres növekedéseként határozták meg legalább két egymást követő mérés során. Ezt a tanulmányt a Severance Kórház Intézményi Felülvizsgálati Testülete hagyta jóvá.
2.2. Klinikai és laboratóriumi mérések
A demográfiai és klinikai eredményeket retrospektíven vizsgálták az életkor, a nem, a cukorbetegség időtartama és a gyógyszerek tekintetében. A testtömeg-indexet (BMI, kg/m 2) a tömeg (kg) és a magasság (m) négyzetre osztásával számítottuk. A vizeletből származó albumin kiválasztási mennyiségeket egy automatikus analizátorral (Hitachi 7180 (Hitachi Instruments Service, Tokió, Japán)) mértük 24 órás vizeletmintában. A plazma glükózszintjét glükóz-oxidáz módszerrel határoztuk meg. A HbA1c-t nagy teljesítményű folyadékkromatográfiával mértük a Variant II Turbo Hemoglobin Tesztelő Rendszer (Bio-Rad Laboratories, Hercules, CA) alkalmazásával. A plazma teljes koleszterin, nagy sűrűségű lipoprotein (HDL) koleszterin, trigliceridek (TG) és kreatinin méréseket autoanalizátorral (Hitachi 7600: Hitachi Instruments Service, Tokió, Japán) végeztük. Az alacsony sűrűségű lipoprotein (LDL) koleszterint a Friedewald-képlet segítségével számítottuk ki.
2.3. A GFR becslése és a CKD osztályozása
A GFR becslését a négyváltozós MDRD vizsgálati egyenlet és a CKD-EPI egyenlet segítségével számoltuk ki [18, 19]:
A GFR megbecsülésére szolgáló CKD-EPI egyenletben k értéke 0,7 a nők esetében és 0,9 a férfiak esetében; α nőknél –0,329, férfiaknál –0,411; min a kreatinin/k vagy 1 minimális értékére vonatkozik; és a max a kreatinin/k vagy az 1. maximális értékét jelenti. Mindkét egyenlet esetében az eGFR-t ml/perc/1,73 m 2, súly kg-ban, a szérum kreatinin mg/dL-ben és az életkor években számoltuk. A CKD stádiumot öt alcsoportba soroltuk a CKD NKF-KDOQI kritériumai szerint: 1. stádium, eGFR ≥ 90 ml/perc/1,73 m 2; 2. stádium, eGFR 60–89 ml/perc/1,73 m 2; 3. szakasz, eGFR 30–59 ml/perc/1,73 m 2; 4. szakasz, eGFR 15–29 ml/perc/1,73 m 2; és 5. stádium, eGFR 2 vagy dialízis. A 3. stádiumú CKD-t további két alcsoportra osztottuk: a 3a. Szakasz, az eGFR 45–59 ml/perc/1,73 m 2, és a 3. b stádium, az eGFR 30–44 ml/perc/1,73 m 2 [12, 20].
2.4. Statisztikai analízis
Az adatokat átlagként ± szórásként adjuk meg. A CKD-t eGFR 2-ként határoztuk meg az eGFR-számítás mindkét egyenletéhez [12]. Az egyes egyenletek alapján számított eGFR és a klinikai eredmények kockázatának összefüggéseit Cox regressziós analízissel végeztük, miután korrigáltuk a lehetséges zavaró tényezőket, beleértve az életkort, a nemet, a cukorbetegség időtartamát és a HbA1c-t. Az összes statisztikai elemzést az SAS 9.2 verziójával (SAS Institute, Cary, NC, USA) és a P értékekkel végeztük el. Az átlagos életkor, a HbA1c és a cukorbetegség időtartama 61,9 ± 12,2 év, 8,2 ± 4,3% és 12,7 ± 8,9 év volt. A 24 órás átlagos vizeletalbumin kiválasztási mennyiség 1094,58 ± 1867,38 mg/nap volt, és a betegek 47,5% -a mutatott makroalbuminúriát. A 60 ml/perc/1,73 m 2 alatti eGFR-ként definiált CKD prevalenciája 54% (n = 382) volt az MDRD vizsgálati egyenletnél és 51,6% (n = 365) a CKD-PEI egyenletnél. Az orális antidiabetikus gyógyszereket és az inzulint az összes beteg 69,9% -ánál, illetve 26,0% -ánál alkalmazták. Ebben a vizsgálatban az alanyok 68,2% -a és 37,9% -a szedett gyógyszereket hipertónia és diszlipidémia ellen is,.
Asztal 1
A résztvevők demográfiai és kiindulási jellemzői (n = 707).
| Férfi nő | 416/291 |
| Életkor (év) | 61,9 ± 12,2 |
| A cukorbetegség időtartama (év) | 12,7 ± 8,9 |
| A nyomon követés időtartama (hónap) | 35,9 ± 49,6 |
| HbA1c (%) | 8,2 ± 4,3 |
| Cr (mg/dl) | 1,59 ± 1,24 |
| eGFR CKD-EPI (ml/perc/1,73 m 2) | 59,08 ± 30,27 |
| Szakaszok, n (%) | |
| 1. szakasz: ≥90 | 120 (17.0) |
| 2. szakasz: 60–89 | 222. (31.4.) |
| 3a szakasz: 45–59 | 102. (14.4.) |
| 3b. Szakasz: 30–44 | 113 (16.0) |
| 4. szakasz: 15–29 | 104. (14.7.) |
| 5. szakasz: 2) | 58,01 ± 31,77 |
| Szakaszok, n (%) | |
| 1. szakasz: ≥90 | 96 (13.6) |
| 2. szakasz: 60–89 | 229 (32,4) |
| 3a szakasz: 45–59 | 107. (15.1.) |
| 3b. Szakasz: 30–44 | 122. (17.3.) |
| 4. szakasz: 15–29 | 111. (15.7.) |
| 5. szakasz: 1. táblázat). Összehasonlítva az egyes egyenletek CKD stádiumát, az MDRD-vel becsült betegek 10,9% -át átsorolták a CKD-EPI egyenlet elfogadásával. A CKD stádium legtöbb átsorolását a 3a stádiumú betegeknél figyelték meg (eGFR MDRD 45–59 ml/perc/1,73 m 2) (1. ábra). Ezen betegek (n = 107) közül 15,9% -ot (n = 17) átsoroltak a CKD alacsonyabb stádiumába, és 0,9% -ot a CKD magasabb stádiumába. Az eGFR MDRD által a CKD 2. stádiumában szenvedő 229 beteg 13,5% -át (n = 31) lefelé csoportosította az 1. CKD stádiumba az eGFR CKD-EPI, csökkentve a 2. CKD stádium prevalenciáját 32,4% -ról 31,4% -ra. A CKD 3b. Stádiumú, 30–44 ml/perc/1,73 m 2 eGFR MDRD-s betegeknél az eGFR által a CKD 3a stádiumba történő felminősítés a CKD-EPI-vel 122 beteg 10,7% -ánál (n = 13) történt. Ezzel szemben az eGFR MDRD 1. CKD stádiumú 96 betegének 7,3% -át (n = 7) az eGFR CKD-EPI felfelé osztályozta a CKD 2. stádiumába. Összességében a CKD (60 ml/perc/1,73 m 2 alatti eGFR-ként definiált) prevalenciája 54% -ról 51,6% -ra csökkent a CKD-EPI egyenlet alkalmazásával. Ezenkívül a CKD-EPI egyenlet alkalmazásával a CKD korábbi stádiumába történő átminősítés valószínűleg fiatalabb személyeknél fordul elő (medián életkor, 55,5 vs. 64,2 év, P 2. ábra, a CKD stádiumának előrehaladása mindkét egyenlet esetében megnövekedett a szérum kreatininszint megduplázása szakaszfüggő módon. Cox regressziós analízisekben (2. táblázat) az egyes egyenletek szerint osztályozott CKD stádium a kiindulási szérum kreatininszint megduplázódásának fokozott kockázatával járt együtt. Összehasonlítva az összes CKD stádiumot az 1. stádiumú CKD-vel becsültük mindkét egyenlet alapján a szérum kreatininszint megkétszereződéséhez értékeltük a Cox arányos veszélyességi arányokat (HR), az MDRD vizsgálati egyenletnél a szérum kreatininszint megduplázódásának Cox arányos HR-je 1,54 volt (95% CI, 0,71–3,31; P = 0,27 ) a 2. szakaszban és 1,79 (95% CI, 0,79–4,07; P = 0,17) a 3a. szakaszban. Ezzel szemben a CKD-EPI egyenlet esetében a szérum kreatininszint megduplázódásának Cox-arányos HR-je 1,90 volt (95% CI, 0,97–3,73; P = 0,063) a szt ge 2 és 2,18 (95% CI, 1,04–4,55; P = 0,038) a 3a. A CKD (eGFR 2) előrehaladott stádiumában mindkét egyenlet szignifikáns HR-t mutatott a szérum kreatininszint megduplázódásához. Az 1. modellben az egyes egyenletek által becsült csökkent eGFR összefüggés az alapszint kreatininszint megkétszereződésének kockázatával statisztikailag szignifikáns maradt az életkor és nem szerinti kiigazítást követően. Ezenkívül a 2. modellben a cukorbetegség időtartamának, a 3. modellben a cukorbetegség és a HbA1c időtartamának igazítása, valamint a 4. modellben a magas vérnyomás kezelésére történő alkalmazkodás, mindkét Cox regressziós modellben az eGFR CKD-EPI nagyobb HR-t mutatott a szérum kreatininszint megduplázódásához, mint Az eGFR MDRD igen. |
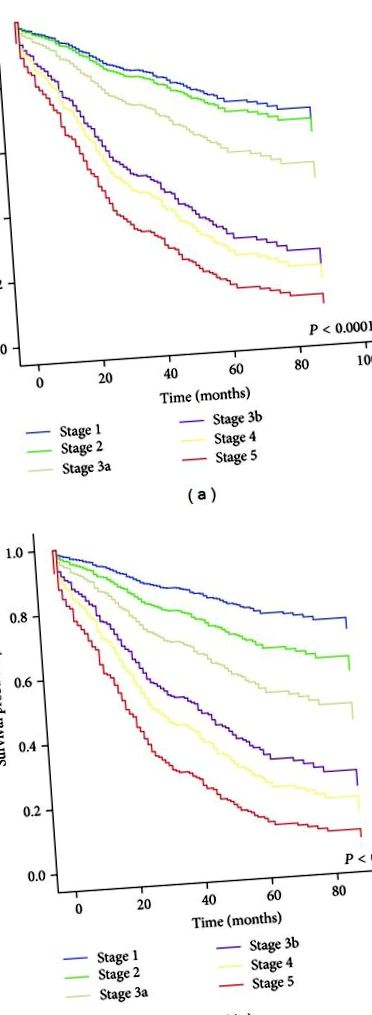
Cox-regressziós túlélési görbe a szérum kreatininszint megduplázásához a CKD stádium szerint minden eGFR egyenlet esetében: MDRD (a) és CKD-EPI (b). Az életkor és a nem igazodik.
2. táblázat
Nyers és kiigazított Cox-arányos kockázati arány a kiindulási szérum kreatininszint megduplázásához 707, 2-es típusú diabéteszes nephropathiás betegben, CKD-stádium szerint rétegezve az egyes egyenletek szerint.
| CKDMDRD | |
| Korrigált modell 1 | |
| 2. kiigazított modell | |
| Korrigált modell 3 | |
| Kiigazított modell 4 | 2) [23, 24]. Ezen kihívások miatt az MDRD vizsgálati egyenlet alkalmazása kevésbé hasznosnak tekinthető az 1. és 2. CKD stádiumú betegek osztályozásához, a hiperfiltráció igazolásához és a GFR változásainak nyomon követéséhez a magasabb tartományban [1]. Továbbá beszámoltak arról, hogy az MDRD tanulmányi egyenletével értékelt eGFR túl diagnosztizálta a CKD-t, különösen fiatalabb fehér nőknél [24, 25]. Egy nemrégiben készült, különböző populációkon alapuló metaanalízis feltárta, hogy a CKD-EPI egyenlet nemcsak a CKD osztályozását, hanem a mortalitás és az ESRD kockázatát is pontosan megjósolta, mint az MDRD vizsgálati egyenletét [26]. Ezek a kielégítetlen igények a CKD-EPI által javasolt új egyenlet megjelenését eredményezték. Egyre több bizonyíték bizonyította, hogy a CKD-EPI egyenlet pontosabb lehet, mint az MDRD tanulmányi egyenlet [18, 27–29]. Az eGFR klinikai következményeit azonban a CKD-EPI egyenlettel értékelve az MDRD vizsgálati egyenlettel összehasonlítva még nem ismerték jól a koreai 2-es típusú cukorbetegeknél. |
Vizsgálatunk retrospektív jellege mellett néhány fontos korlátozás is megfontolandó. Először nem értékeltük a két eGFR-egyenlet pontosságát a GFR becslésére nephropathiás 2-es típusú diabéteszes betegeknél a közvetlenül mért GFR-hez (pl. GFR mérés inulin vagy izotóp alkalmazásával) képest. Másodszor, bár a CKD-EPI egyenlet nagyobb klinikai következményekkel bír, mint az MDRD vizsgálati egyenlet a CKD korábbi stádiumában lévő betegeknél, mégis magában foglalja a szérum kreatinin eredendő korlátozását, amely függ az izomtömegtől, a generációtól és a tubuláris szekréciótól [11 ]. Harmadszor, az alanyokat viszonylag rövid ideig (medián, 2,4 év) követtük nyomon, és nem volt információnk a lehetséges zavaró tényezőkről (például a dohányzásról). Ezért néhány fontos klinikai eredményt, például az ESRD-t vagy a mortalitást nem sikerült megfelelően értékelni. Végül ez a tanulmány csak koreai T2D-ben szenvedő betegeket érintett, megakadályozva, hogy eredményeinket más etnikai populációkra általánosítsuk.
A T2D-ben szenvedő alanyok kezelését illetően figyelembe kell venni a hosszú távú orvosi szövődményeket, például a CVD-t és az ESRD-t, különösen azoknál a diabéteszes nephropathiában szenvedőknél, akik hajlamosabbak a vesefunkció romlására és nagyobb a társbetegségek, például a CVD és a halálozás. Ebben a tekintetben a veseelégtelenség lehetséges előrehaladásának pontos előrejelzése lehet az egyik legfontosabb klinikai végpont a cukorbetegek értékelésében, akik megmutatják a nem kívánt klinikai eredmények lehetőségét. Korábbi beszámolóinknak és eredményeinknek megfelelően a CKD-EPI egyenlet optimális egyenletnek tekinthető a normál vesefunkcióval rendelkező személyek vagy a CKD korábbi stádiumának értékelésében, amely a korai stádiumú diabéteszes nephropathiához hasonló klinikai szcenárió [18, 27–29]. Összességében megállapításunk, hogy korlátai vannak, számos klinikai vonzattal járhat, ami további vizsgálatot indokol.
5. Következtetések
Összegzésképpen azt javasoljuk, hogy a CKD-EPI egyenlet felülmúlja az MDRD vizsgálati egyenletet a vesefunkció csökkenésére hajlamos nephropathiás 2-es típusú cukorbetegek azonosításában. További vizsgálatokra van azonban szükség a CKD-EPI egyenlet pontosságának és pontosságának igazolásához az MDRD vizsgálati egyenlettel összehasonlítva a GFR becslésében sokszínűbb populációkban, például idős betegeknél, különböző etnikai csoportoknál és T2D-ben szenvedő betegeknél [18, 33].
Közzététel
A cikk tartalmáért és megírásáért egyedül a szerzők felelnek.
- A fogyókúra tápszerrel történő fogyásának hatása a veseműködésre elhízott, cukorbetegekben
- A testtípusú étrendek összehasonlítása
- A fajta és az étrend típusának hatása a tojások frissességére és minőségére A Mos összehasonlítása
- Különböző antropometriai indexek összehasonlítása a kínai gyermekek hasi elhízásának előrejelzésében a
- Széles körben alkalmazott JAX egerek összehasonlítása 2-es típusú cukorbetegség és elhízás esetén