Koncepcionális keretrendszer a precíziós táplálkozás tanulmányozásához és befektetéséhez
Absztrakt
A tápanyagoknak és az élelmiszerből származó bioaktív molekuláknak komplex anyagcsere útvonalakon kell haladniuk, és ezek az utak emberenként eltérőek. A metabolikus heterogenitást a genetikai variációk, az epigenetikai variációk, a mikrobiom összetételének és funkciójának különbségei, az életmódbeli különbségek és a környezeti expozíció változása okozza. Ez az áttekintés a metabolikus heterogenitás ezen forrásait tárgyalja, és bemutat néhány kutatási beruházást, amelyekre szükség lesz a precíziós táplálkozás alkalmazásának gyakorlati megvalósításához.
Bevezetés
Ennek a megértésnek a fejlesztése érdekében sürgősen szükség van olyan továbbfejlesztett módszerek kidolgozására, amelyekkel értékelhető számos ilyen tényező, amelyek hozzájárulnak a metabolikus heterogenitáshoz, jobb számítási és informatikai eszközökre, amelyek felhasználhatók az emberek metabolikus heterogenitásának forrásai közötti komplex kölcsönhatások modellezésére, és jobb eszközök a tudomány és a modellek tesztekké és beavatkozásokká történő átültetéséhez, amelyeket az egészségügyi szakemberek képesek megvalósítani. E precíziós táplálkozási célok megvalósításának képessége jelentős intellektust, pénzt és időt igényel (1. táblázat).
Asztal 1
A precíziós táplálás elősegítéséhez szükséges beruházások.
| Az étrend értékelése |
| 1. Jobb biomarkerek kifejlesztése az étrend bevitelének értékelésére 2. Jobb eszközök kifejlesztése az étrend bevitelének mérésére |
| Genetikai variáció |
| 1. A funkcionális genetikai variánsok nagyobb katalógusának kidolgozása 2. További vizsgálatok, amelyek genetikai, étrendbeviteli és egészségügyi eredményeket gyűjtenek 3. Metabolomikus és informatikus eszközök fejlesztése az emberek anyagcseréjét zavaró genetikai variánsok validálásához 4. Jobb informatikai megközelítések az adatok genetikai variánsok közötti integrálásához |
| Epigenetikus variáció |
| 1. Módszerek kidolgozása az emberekben nem könnyen hozzáférhető szövetek epigenetikai módosításainak értékelésére 2. Az emberi anyagcserét megváltoztató epigenetikus változásokhoz vezető kritikus események és időzítés jobb megértése. 3. A funkcionális epigenetikus változások nagyobb katalógusának kidolgozása (amelyek megváltoztatják az emberi anyagcserét) |
| Mikrobiom variáció |
| 1. Jobb módszerek kidolgozása a mikrobiota működésének azonosítására az emberi anyagcserére gyakorolt hatások szempontjából 2. Az étrend bevitelének jobb értékelésének bevonása a mikrobiota vizsgálatok tervezésébe 3. Az étrend és az expozíció mikrobiotapopulációkra és működésére gyakorolt hatásainak jobb megértése |
| Az expozíció változása |
| 1. Jobb módszerek kidolgozása az emberek expozíciójának (az emberek által kitett környezeti molekulák) azonosítására 2. Az expozóma funkcionális komponenseinek azonosítása (amelyek megváltoztatják az emberi anyagcserét) |
| Életmód variáció |
| 1. Jobb biomarkerek kidolgozása az életmód (különösen a fizikai aktivitás) értékelésére 2. Jobb eszközök fejlesztése az életmód (különösen a fizikai aktivitás) mérésére 3. A funkcionális életmód-változatok (különösen a fizikai aktivitás) nagyobb katalógusának kidolgozása az emberi anyagcserére gyakorolt hatások szempontjából. |
| Rendszerbiológia |
| 1. A metabolikus variáció összes fenti forrása közötti kölcsönhatások jobb megértésének fejlesztése 2. Jobb informatikai eszközök kidolgozása a fentiekből származó adatok integrálásához az emberi anyagcserét zavaró változatok szempontjából |
| Fordítás a gyakorlathoz |
| 1. Jobb képzési programok kidolgozása az egészségügyi szakemberek és a lakosság számára a precíziós táplálkozás terén 2. Precíziós táplálkozással irányított beavatkozások kidolgozása metabolikus zavarokkal küzdő emberek számára, amelyek egészségügyi problémákat okoznak. 3. Olyan informatika fejlesztése, amely felhasználhatja a fent meghatározott adatokat a megfelelő táplálkozási és étrendi beavatkozások azonosítására olyan metabolikus zavarokkal küzdő embereknél, akik egészségügyi problémákat okoznak |
A táplálkozással kapcsolatos anyagcsere-heterogenitás forrásai
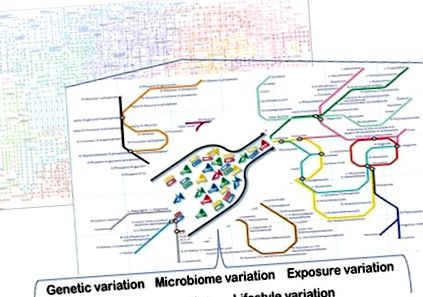
Számos olyan tényező létezik, amely hozzájárul az emberek metabolikus heterogenitásához. A genetikai variációk, az epigenetikai variációk, a mikrobiómákkal kapcsolatos változások, az életmódbeli változások (pl. Fizikai aktivitás, táplálkozási viselkedésbeli különbségek), valamint az ember környezetében jelenlévő kémiai és egyéb expozíciók variációi csak néhány ezek közül a tényezők közül (1. ábra). Ezen tényezők némelyike jobban megérthető, mint mások, és ez az áttekintés ezekre összpontosít.
A metabolikus heterogenitás forrásai. A Precision Nutrition az anyagcsere-változások mögöttes forrásainak megértésén alapul. Ide tartoznak az emberek közötti genetikai, epigenetikai, mikrobiológiai, életmódbeli és expozíciós különbségek. E változások némelyike az anyagcsere hatékonyságát (szűk keresztmetszeteit) idézi elő, amelyek káros diétájukkal járnak az étrendjük által megnehezített embereknél. Az alapul szolgáló komplex biológiai rendszerek számítógépes és matematikai modellezése, valamint ezeknek a modelleknek az alkalmazása az egyénre szabott beavatkozások alapján a precíziós táplálkozás gyakorlatának alapja.
A genetikai variáció, mint a táplálkozás szempontjából releváns anyagcsere-heterogenitás forrása
Az anyagcsere számos metabolikus út működését foglalja magában, ezeknek az útvonalaknak minden egyes lépését a gének által kódolt fehérjék közvetítik. A gének exonjain belüli kodonok határozzák meg a fehérjetermékek aminosav-szekvenciáját. Ezenkívül a promóter régiók genetikai kódja (általában ezekhez az exonokhoz közel) tartalmaz olyan válaszelem-szekvenciákat, amelyek képesek külső jelekhez kötődni, amelyek meghatározzák, hogy egy szabályozó erősítők, például hormonok, antioxidánsok, kalcium, fémek stb. (Resseguie és mtsai, 2011; Hou és mtsai, 2012). Végül a DNS egyes régiói nem a fehérjetermékeket kódolják, hanem a nem kódoló RNS-eket, amelyek szabályozzák, hogy a géneket átírják-e, vagy a keletkező mRNS-t fehérjévé alakítják-e át (Mirra et al., 2018).
Az embereknek milliónyi variációja van genetikai kódjuk „helyesírásában” (bármelyik embernek körülbelül 50 000 ilyen egyetlen nukleotid polimorfizmusa (SNP) van (Overbeek et al., 2005; Sabeti et al., 2007). Ezek a genetikai variációk öröklődnek az ősi ősöktől, és ezért örökségüktől függően különböznek az emberek között (Overbeek et al., 2005; Sabeti et al., 2007). Ezen SNP-k közül néhány olyan kodonhelyettesítést eredményez az anyagcsere kritikus génjeiben, amely megváltoztatja kifejezésüket, funkciójukat vagy Így az ember genetikai kódjának variációi befolyásolhatják a kritikus metabolikus enzim (vagy transzporter, vagy receptor) mennyiségének rendelkezésre állását (a fehérje szintézisének sebességének megváltoztatásával vagy aminosavmaradékok megváltoztatásával, amelyek befolyásolják a a fehérje élettartama) és/vagy a genetikai variációk megváltoztathatják a fehérje működését (olyan aminosavmaradékok megváltoztatásával, amelyek befolyásolják, hogy egy enzim hogyan kötődik a szubsztrátumához, vagy amelyek befolyásolják, hogy a fehérje hogyan katalizálja az adott szubsztanciát mérték). Az ilyen funkcionális SNP-k a metabolikus heterogenitás egyik forrását jelentik, és különbségeket okozhatnak az emberek között abban, hogyan reagálnak egy tápanyagra vagy bioaktív molekulára.
Mivel egy személy genetikai kódja az életciklus alatt viszonylag állandó marad, az ilyen génváltozat-alapú jóslatok ereje az, hogy az élet bármely szakában mérhetők, ellentétben a legtöbb más kockázati tényezővel. Kiváló molekuláris eszközök állnak rendelkezésre a génszekvencia és a genetikai polimorfizmusok értékelésére. Emiatt a nutrigenetika/nutrigenomika gyorsabban fejlődött a precíziós táplálkozáshoz való hozzájárulás terén. A genetikai variáció azonban csak egy hozzájárul a metabolikus heterogenitáshoz.
Epigenetikus különbségek, mint a metabolikus heterogenitás forrása
A genetikai kód önmagában nem elegendő a fenotípus megjóslásához. A test sejtjei nagyon különböző funkciókkal rendelkeznek a különböző szövetekben és szervekben, annak ellenére, hogy szinte azonos genetikai kódot tartalmaznak. Ezek a különbségek a genom epigenetikus szabályozásának tudhatók be (Ideraabdullah és Zeisel, 2018). Az epigenetikus szabályozás magában foglalja a kémiai jelek elhelyezését a DNS-en vagy a hisztonokon az íróként ismert enzimek által. Ezeket a jeleket az olvasónak nevezett specifikus szabályozó enzimeknek fel kell ismerniük, amelyek ezután elnyomják vagy aktiválják a génátírást vagy elnyomják az mRNS fehérjévé történő transzlációját, és végső soron e jelek hatásait radíroknak nevezett enzimeknek kell véget vetniük, amelyek eltávolítják az epigenetikus nyomokat. A mai napig kétféle epigenetikus jel létezik az emberekben: a DNS kovalens módosításai és a hiszton fehérjék kovalens módosításai.
A DNS-metiláció a legszélesebb körben vizsgált epigenetikai jel. A DNS metilezetté válik, ha metilcsoportot adnak a citozinhoz, így 5-metil-citozint (5mC) termelnek. Emberekben az 5mC elsősorban a palindróm CG dinukleotidoknál fordul elő (Szyf, 2005). Az 5mC jelenléte a lokuszban a gén repressziójával vagy az aktivációval jár együtt, a génen belüli helytől függően (Jones, 2012). Például, míg a promóter régiókban az 5mC gyakran társul a gén repressziójával, addig a géntestben lévő 5mC (intronok és exonok) gyakran génaktivációval társul (Ideraabdullah és Zeisel, 2018). Az 5mC gyakran nem kezdeményezi a gének elnémítását, inkább egy gén elnémított állapotának fenntartási mechanizmusaként működik (Jones, 2012). A DNS-metiláció metabolikus heterogenitást indukál, viszont az étrend és a metabolikus heterogenitás befolyásolja a DNS-metilációt (Jones, 2012). A DNS jelölésére használt metilcsoportok S-adenozil-metioninból származnak, amely étrendi metioninból, 5-metil-tetrahidrofolátból és betainból (kolinból) származik, és a DNS-metilezést közvetlenül az étrendi bevitel modulálja (Wolff és mtsai., 1998; Szyf, 2005; Dolinoy és mtsai, 2006; Waterland és mtsai, 2006, 2007; Mehedint és mtsai, 2010; Jones, 2012; Dominguez-Salas és mtsai, 2014; Ideraabdullah és Zeisel, 2018). A DNS-metiláció értékelésének módszereit nemrégiben felülvizsgálták (Shen és Waterland, 2007).
A DNS-szekvenciával ellentétben az epigenetikus jelek és a nem kódoló RNS-ek az élettartam alatt, különösen a korai élet során, megváltoztathatók, és ezek a változások közvetítik az anyagcsere újrarendezését, hogy igazodjanak a tápanyagok elérhetőségéhez és a környezethez (Ideraabdullah és Zeisel, 2018). Ezért fontos az adatgyűjtés időzítése. Ez bonyolultabb réteget ad hozzá, amellyel a precíziós táplálkozás tudományának finomításával kell foglalkozni. A tápanyagcserét nemcsak az epigenetikai különbségek módosítják, hanem ezeket a különbségeket az étrendi bevitel és a környezet is befolyásolja (Ideraabdullah és Zeisel, 2018).
A mikrobiom mint az anyagcsere-heterogenitás forrása
A gyomor-bél traktus a fő út, amelyen keresztül az emberek hozzáférnek a tápanyagokhoz; billió mikroba gyarmatosítja (Qin és mtsai., 2010). Ezek a mikrobák az idő múlásával fejlődve fejlődtek az emberi gyomor-bél traktusban, genomjaik tízszer nagyobbak, mint az emberi genom, és szinte bármilyen szubsztrátot képesek metabolizálni, ami eléjük kerül (Goodman és Gordon, 2010). Gyakran ezek a mikrobák hozzáférnek ezekhez a tápanyagokhoz, mielőtt azok hozzáférhetővé válnának a gyarmatosított emberek számára, és a mikrobák metabolizálják az ételeket, és olyan kis molekulákat állítanak elő, amelyeket az emberek abszorbeálnak (Manor et al., 2014; Hall és Versalovic, 2018). Ez módosíthatja, hogy az emberek mennyi energiát nyernek az ételektől (Scheithauer et al., 2016), ellátják az embereket nélkülözhetetlen vitaminokkal [például K-vitaminnal (Ramakrishna, 2013)], létrehozhatnak szabályozó molekulákat, például rövid láncú zsírsavakat (Ramakrishna, 2013), és módosítsa az egyéb nélkülözhetetlen tápanyagok elérhetőségét [például a kolin (Zeisel és Warrier, 2017)]. Az emberek nagymértékben különböznek a bennük lévő mikrobáktól (Eckburg et al., 2005), így a belünkben élő mikrobák fontos forrása az emberek közötti metabolikus heterogenitásnak.
- Mindent az élelmiszer-szín adalékanyagokról Precíziós táplálkozás
- Minden az endokrin rendellenességekről Precíziós táplálkozás
- Fekete bab recept; Táplálkozás Precíziós táplálkozás; s Élelmiszer-enciklopédia
- Butternut Squash recept; Táplálkozás Precíziós táplálkozás; s Élelmiszer-enciklopédia
- A helyreállítás fellendítése A leggyakoribb helyreállítási problémák megoldása Precíziós táplálkozás