Nem kontrollált, nyílt klinikai vizsgálat a diétás táplálék hatékonyságának értékelésére az atópiás kutyák viszketésén és dermatológiai pontozásán
Absztrakt
Háttér
A kutya atópiás dermatitis (AD) gyakori bőrbetegség. Ennek a vizsgálatnak az volt a célja, hogy értékelje a bőrgát működésének javítására és a gyulladás csökkentésére tervezett táplálékot a viszketés és a klinikai súlyosság csökkentése érdekében a kliens tulajdonában lévő atópiás kutyáknál. Az étel antioxidáns keveréket tartalmazott az oxidatív stressz csökkentésére, növényi polifenolokat a hízósejtek stabilizálására, és többszörösen telítetlen zsírsavakat a bőr egészségének javítására és a gyulladás csökkentésére.
Eredmények
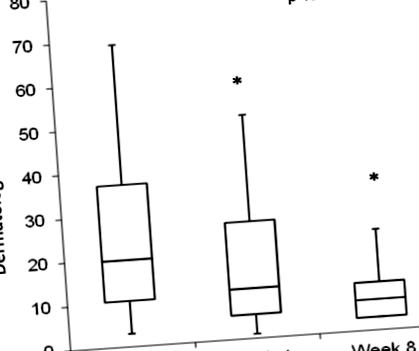
Tizenhét kutyát vontak be az elemzésbe. Kezdetben 48 felnőtt atópiás kutyát vontak be, és 8 héten keresztül kizárólag dermatológiai táplálékkal etették őket egy nem kontrollált, nyílt vizsgálatban. Harmincegy kutyát kizártak a következő okok miatt: orális és helyi gyógyszeres változtatások (n = 17), hiányzó adatok (n = 4), zsírsav-kiegészítés (n = 3), az élelmiszer megtagadása (n = 3), kiesett (n = 3), és a tulajdonos aggályai (n = 1). A 0 (normál) - 4 (súlyos) skála alkalmazásával az állatorvosok a 0., 4. és 8. héten értékelték az atópiás klinikai tünetek jelenlétét és súlyosságát. A háziállattartók 0 ( nincs jelen) - 10 (folyamatosan jelen van) a 0., 4. és 8. héten. A kiindulási kiindulási pontszámokkal (medián 19, 3–69 tartomány) összehasonlítva az összes állatorvos-pontszám szignifikánsan alacsonyabb volt a 4. héten (medián 11, 1– 15) és 8 (medián 7, 3–46 tartomány) (o
Háttér
Az atópiás dermatitis (AD) a kutyák gyakori betegsége, és viszketésként és gyulladásként definiálják az immunglobin E (IgE) termelés révén, amely túlnyomórészt a környezeti antigénekre irányul [1]. Noha az AD patogenezise nem teljesen ismert, a kutatók nemrégiben feltárták, hogy az AD magában foglalja a veleszületett immunrendszert és az epidermális gát változását [2]. Az AD hagyományos modelljei a genetikai változásokra összpontosítottak, amelyek kóros immunválaszokat eredményeztek a tipikusan ártalmatlan antigénekre. A közelmúltban új elméletek szerint az atópiás betegek kóros bőrgáttal rendelkeznek, amely lehetővé teszi az allergének és mikrobák behatolását az epidermiszbe és kölcsönhatásba lépést az immunsejtekkel. Ezek a modellek nem feltétlenül állnak ellentétben, és előfordulhat, hogy egy elsődleges epidermális hiba kombinálódik egy túlaktív immunválasszal [3].
A stratum corneum (SC) intracelluláris lipidlamellája fontos a normál bőrgátló funkció fenntartásához. Az AD-vel rendelkező kutyák nem sérülékeny bőre csökkentette ennek a lamelláris rétegnek a vastagságát és folytonosságát [13, 14]. Pontosabban, alacsonyabb ceramidszintet mutattak ki az AD kutyák SC-jében a normál kontrollokhoz képest [15, 16]. Úgy tűnik, hogy a PUFA-k orális kiegészítése enyhíti ezen strukturális változások legalább egy részét [14].
A polifenolok természetes vegyületek, amelyek elsősorban gyümölcsökben és zöldségekben találhatók, és tartalmaznak egy aromás gyűrűt, amelyhez több fenolcsoport kapcsolódik [17]. A polifenoloknak több osztálya van, beleértve a flavonoidokat, a stilbeneket, a fenolsavakat és a hidroxi-fahéjsav-lignánokat [18]. A polifenolok példái közé tartozik a resveratrol, a kvercetin, az epigallocatechin-gallát (ECGC) és a kurkumin [18]. A polifenolokat széles körben tanulmányozták daganatellenes és gyulladáscsökkentő tulajdonságaik miatt [19,20,21].
Bizonyítékok támasztják alá a polifenolok bizonyos osztályainak alkalmazását allergiás betegségek esetén is [17, 18]. Az allergiás immunválasznak két fő szakasza van, amelyről úgy gondolják, hogy a polifenolok befolyásolják: az allergén szenzibilizáció és az allergének újbóli expozíciója [18]. Bizonyos polifenolok oldhatatlan komplexek képződésével hipoallergénvé tehetik az antigén fehérjéket [22]. A polifenolok az antigént bemutató dendritikus sejteket is befolyásolhatják, befolyásolva azok működését és érését [23, 24]. Az allergén újbóli expozíciója során a B-sejtek antitesttermelését és a T-sejtek citokintermelését a polifenolok is csökkenthetik [18, 25,26,27,28,29]. Ezenkívül kimutatták, hogy a kvercetin gátolja a gyulladásos mediátorok felszabadulását a hízósejtekből [30,31,32]. A szájon át alkalmazott kvercetin és származékai (kaempferol, rutin) mérsékelt vagy súlyos AD-ben szenvedő betegek humán klinikai vizsgálatában csökkentették a klinikai tüneteket és gyulladásokat [33, 34]. Annak ellenére, hogy in vitro és in vivo bizonyíték van arra, hogy alátámasztja a polifenolok allergiás bőrbetegségben való alkalmazását, a kutya AD-re irányuló kutatások még mindig hiányoznak.
Az oxidatív stressz egyensúlyhiány a prooxidáns folyamatok és az antioxidáns védekezés között, és megzavarhatja a sejtek szignalizációját és az arachidonsav anyagcserét, szisztémás gyulladást eredményezve [35]. Az AD mind emberben, mind kutyában magasabb oxidatív stresszhez kapcsolódik [36, 37]. A C-vitamin egy antioxidáns, amely fontos a bőr egészségének megőrzéséhez, és az AD-ben szenvedő emberek intradermális koncentrációja lényegesen alacsonyabb [38]. Úgy tűnik, hogy a plazma C-vitamin-koncentrációja fordítottan korrelál az emberek klinikai AD-súlyosságával [39]. Az E-vitamin egy másik erős antioxidáns, amely különösen fontos a lipidperoxidáció megelőzésében. Egyes tanulmányok kimutatták, hogy az E-vitamin étrendi bevitele fordítottan összefügg az allergiás szenzibilizációval és a felnőtt emberek szérum IgE-koncentrációjával [40, 41]. Ezenkívül randomizált, placebo-kontrollos klinikai vizsgálatok kutyákon és embereken egyaránt megállapították az AD klinikai tüneteinek csökkenését E-vitamin-kiegészítéssel [42, 43].
Az AD kezelésének multimodálisnak kell lennie. Táplálkozási beavatkozás hozzáadása az általánosan alkalmazott terápiákhoz, például immunmodulációhoz, immunszuppresszióhoz és antimikrobiális/parazitaellenes gyógyszerekhez, tovább csökkentheti a viszketést és javíthatja a bőrgát funkcióit. A tanulmány célja annak meghatározása volt, hogy egy táplálkozásilag teljes és kiegyensúlyozott étrend, amely magas koncentrációban tartalmaz PUFA-kat, antioxidáns aktivitású vitaminokat és polifenolokat, például kvercetin, javítja-e az AD klinikai tüneteit és súlyosságát a kliens tulajdonában lévő kutyákban.
Mód
Az összes eljárást a Hill globális állatjóléti bizottsága hagyta jóvá, és az állattartók a részvétel előtt tájékozott beleegyezést adtak. Minden olyan fajtához tartozó kliens tulajdonú kutyákat (kísérleti egységeket), akiknek kórtörténetében környezeti allergia mutatkozott, viszketés, nyalás, karcolás, forró foltok kialakulása és/vagy atópiás miatti középfülgyulladás jelentkezett, 26 alapellátásból és 2 bőrgyógyászati állat-egészségügyi intézményből toboroztak. 11 európai országon belül. A diagnózis konzisztenciáját az atópiás dermatitis legalább 5 teljesített kritériumának jelenléte növelte.
A kutyák az atópiás dermatitis szokásos kezelésében részesülhetnek, beleértve az allergénelkerülést, az allergénspecifikus immunterápiát, a tüneti gyulladáscsökkentő terápiát (pl. Antihisztaminok, kortikoszteroidok, antidepresszánsok, ciklosporin, misoprostol, leukotrién inhibitorok, foszfodiészteráz inhibitorok) és antimikrobiális terápiát (pl. gombás szerek, antibiotikumok) mindaddig, amíg a gyógyszerek, az adagok és az adagolás gyakorisága az előző étkezés beadásától a vizsgálat befejezéséig állandó maradt. A tulajdonosoknak hajlandóknak kellett lenniük arra, hogy kizárólag a vizsgálat ideje alatt táplálják a dermatológiai étrendet. Az étrend tápanyag-összetétele és funkcionális összetevői az 1. és a 2. táblázatban találhatók
A kutyákat kizártuk, ha kezeletlen parazita vagy fertőző dermatitiszük volt, vagy egyidejű bőrbetegségeket diagnosztizáltak velük (pl. Bolhacsípés allergiás dermatitis, szarkoptikus rüh, Cheyletiella, Demodex canis, Trombicula autumnalis, Trichodectes canis és/vagy a bakteriális pyoderma vagy Malassezia). Ezenkívül a kutyáknak 1 évnél fiatalabbnak kellett lenniük, és nem voltak terhesek vagy szoptathatók. Kizárták azokat a kutyákat is, akiknek egyidejűleg súlyos szisztémás betegségei vannak, például diabetes mellitus, hypothyreosis, hyperadrenocorticismus és krónikus vesebetegség, valamint azokat a kutyákat, akiknél az etetési időszak alatt várható vagy tervezett műtétet végeztek. Bármely kutya, amely halolaj-kiegészítőket vagy olyan ételeket fogyaszt, amelyekről ismert, hogy magas EPA- és DHA-tartalmat (> 500 mg/1000 kcal EPA és DHA együttesen) tartalmaznak a vizsgálat megkezdése előtt 12 héten belül, nem kerültek beiratkozásra. A kutyatulajdonosok nem hajlandóak kizárólag 8 hétig táplálni a tesztet, abbahagyni a homeopátiás, táplálkozási, vitamin- vagy étrend-kiegészítőket (pl. E-vitamin, zsírsav-kiegészítők, glükózamin/kondroitin-szulfát, antioxidánsok), valamint az oclacitinib (Apoquel®) tervezett alkalmazását ) szintén kizárási kritériumként szolgált. 2. lábjegyzet
A normál valószínűségi görbék azt mutatták, hogy az állatorvos dermatológiai pontszámai (a teljes kutya és a kutya 12 régiója mindegyikének összesített pontszáma) és a testállapot pontszámok torzak voltak. A normál valószínűségi ábrák azt is megmutatták, hogy a testtömeg és az összes tulajdonos pontszám rendesen eloszlott. Ennek megfelelően az adatokat mediánként összegeztük, tartományban (állatorvos dermatológiai pontszámai és testállapot-mutatói) és legkevésbé négyzetes átlagértékeként standard hibával (testtömeg és a tulajdonos értékelési pontszámai).
A statisztikai szignifikanciát α = 0,05 értékre állítottuk be. Valamennyi elemzést a SAS 9.4 verziójával hajtottuk végre (Cary, NC, USA).
Eredmények
Tizenhét kutyát vontak be az elemzésbe. Kezdetben 48 felnőtt AD kutyát vontak be. Harmincegy kutyát kizártak a következő okok miatt: orális gyógyszeres változtatások (n = 14), helyi antimikrobiális sampon (n = 3), hiányzó adatok (n = 4), zsírsav-kiegészítés (n = 3), étel-elutasítás (n = 3), kiesett (n = 3) és a tulajdonos aggályai (n = 1). A 14 orális gyógyszermódosítással rendelkező kutya közül nyolc abbahagyta az antimikrobiális szerek (n = 4) és/vagy immunszuppresszív gyógyszerek (n = 5). A fennmaradó orális gyógyszermódosítással rendelkező kutyák olyan gyógyszereket kezdtek, mint például a ciklosporin (n = 2), prednizon (n = 1), oklacitinib (n = 3), dexametazon (n = 1) vagy immunterápia (n = 1). Az egyik kutya abbahagyta az oklacitinibet és elkezdte a dexametazont. Az elemzett kutyák csoportján belül hiányoztak az állattartó értékelési pontszámai, így az egyedi értékelések mintamérete 7 és 16 között mozgott. Az elemzett betegek demográfiai adatai a 3. táblázatban találhatók. A betegek 2 és 13 év közöttiek voltak, átlagosan 6,1 év volt, és 10 ivartalan nőstényt, 2 ép nőstényt, 2 ivartalanított hímet és 3 ép férfit tartalmazott. A végső elemzésbe bevont betegek kezdeti beiratkozási dátumai 2016. január 28. és 2016. június 24. között változtak.
Az állatorvosok (módosított CADESI) összesített dermatológiai pontszámának mediánja (az összes regionális helyszín együttvéve) szignifikánsan alacsonyabb volt a 4. héten (medián 11, 1–15 tartomány) és a 8. héten (medián 7, 3–46. Tartomány) az alapértékhez képest (medián 19, 3–69 tartomány) (o értékek 1. ábra
A módosított CADESI-pontszámok jelentős regionális javulást mutattak az idők során. Az arc körüli területek (a medián pontszám [tartomány] a kiinduláskor, 4 hét és 8 hét 3 [0–8], 1 [0–6], 0 [0–5] volt), hónalj (medián pontszám [tartomány] a kiinduláskor 4 hét és 8 hét 2 [0–10], 0 [0–6], 0 [0–4] és elülső mancs volt (a medián pontszám [tartomány] a kiinduláskor, 4 hét és 8 hét volt 3 [0–7], 1 [0–4], 1 [0–4] volt a legjelentősebb javulás (o értékek 2. ábra
A BCS mediánja a vizsgálat kezdetén 3,2 (3–4) volt az 5-ből, és nem változott szignifikánsan (o = 0,61). Az átlagos kezdeti testtömeg 17,3 kg (SE 3,18) volt, és a vizsgálat során nem változott szignifikánsan (o = 0,45).
Vita
Ebben a nyílt, ellenőrizetlen klinikai vizsgálatban az AD-vel rendelkező kutyák mind a kedvtelésből tartott állatok tulajdonosaitól, mind az állatorvosoktól jelentős javulást mutattak, amikor magas PUFA-tartalmú, antioxidáns és polifenol tartalmú étrendet fogyasztottak. Az EPA és a DHA koncentrációja a vizsgálati étrendben összehasonlítható volt a kutya bőrbetegségének egyéb klinikai kísérleteiben alkalmazott dózisokkal (1,35 g/1000 kcal), amikor a kutyák kielégítették az Országos Kutatási Tanács által becsült napi energiaigényt (95–180 × kg 0,75). ) [5, 6, 51]. Mivel a korábbi vizsgálatok kimutatták a javulást egyedül az omega 3 zsírsav-kiegészítéssel, nehéz meghatározni más hatóanyagok szerepét a próba-étrendben. Különösen a polifenolokat nem vizsgálták egyedileg a kutya atópiás tüneteinek enyhítésére.
A vizsgálati étrend általános elfogadottsága jó volt, a kutyák csaknem 90% -a kezdetben a teljes nyolc héten át fogyasztotta az étrendet, és az átlagos testállapot változatlan maradt. Az eredetileg a vizsgálatba bevont kutyák nagy részét el kellett távolítani az orális gyógyszerek megváltozása miatt. A gyógyszereket kezdő és abbahagyó kutyák száma szinte egyenletes volt, így megszűnt a szelekciós elfogultság a többé-kevésbé súlyos esetek felé.
A nyílt jelölés kontrollcsoport nélkül és a kis mintaméret a vizsgálat legfőbb korlátai. Lehet, hogy kedvtelésből tartott állatok tulajdonosai és állatorvosai kedvezőbben értékelték a kutyákat, tudván, hogy étrendet kaptak az AD javítására. Ezenkívül az AD-t a pollenek, a füvek és más környezeti allergének szezonális változásai befolyásolják. A legtöbb beteget kezdetben tél végén, a két hónapos vizsgálatba vonták be (n = 7) és tavasz (n = 8) amikor a szezonális allergia gyakran súlyosbodik. Ezért a szezonális allergia nagyobb valószínűséggel csökkenti az étrend előnyeit, mint fokozza azokat. Ugyanakkor kontroll étrendcsoport hozzáadására lenne szükség a szezonális hatások pontos meghatározásához. Ezenkívül a próbaidőszak egész évre történő kiterjesztése vagy a különböző évszakokban történő próbaidőszak hozzájárulhat a szezonális hatások elutasításához.
Míg ebben a vizsgálatban a dermatológiai értékeléshez használt skála a CADESI-03 skálán alapult, az eredetihez képest módosították. A módosítások célja a validált paraméterek (testhelytípusok) megőrzése, a protokoll egyszerűsítése, valamint az objektív, következetes, megfigyelőkön belüli és megfigyelők közötti megbízható adatok megszerzése volt. Bár ezt a skálát nem validálták, ugyanazokon az elveken alapult, mint a CADESI skála. Ezenkívül következetesen használták az összes beiratkozott betegnél, így lehetővé tette a kiindulási értéktől a 4. és a 8. hétig tartó különbségek objektív értékelését. A skálánk fő korlátja, hogy adataink nem hasonlíthatók össze fej-fej mellett más vizsgálatokkal.
Ez az ellenőrizetlen, nyílt klinikai vizsgálat azt mutatja, hogy mind a háziállattartók, mind az állatorvosok szerint jelentős klinikai javulás érhető el a bőrgát funkcióját támogató étrend táplálásával, miközben csökkenti a gyulladást és az oxidatív károsodásokat is. Az étrend felhasználása az AD kezelésére biztonságos és egyszerű terápiás stratégia az állattartók számára, amely kiegészítheti más kezeléseket. Míg a vizsgálati étrend önmagában nem eredményezte a klinikai tünetek teljes feloldódását, ez lehetővé teheti a klinikusok számára az adagok csökkentését vagy az AD-re felírt gyógyszerek számának csökkentését. Eredményeink azt sugallják, hogy az AD klinikai tüneteinek jelentős javulását kell észlelni a teszt étrend etetésétől számított 4 héten belül, a javulás pedig 8 héten keresztül folytatódik. Nem értékelték, hogy a kutyák tovább javulnak-e az elmúlt 8 hétben. Míg további kutatásokra van szükség a vizsgálat eredményeinek megerősítéséhez és annak meghatározásához, hogy mely étrendi vegyületek nyújtják a legkedvezőbb hatást, ennek a teszt étrendnek az összetevői és összetétele ígéretet tesz az AD kezelésére.
Következtetések
Nyílt, nem kontrollált klinikai vizsgálatban 17 atópiás dermatitiszben szenvedő kutya jelentős javulást mutatott mind az állattartók, mind az állatorvosok részéről dermatológiai diétával etetve.
- Nyílt klinikai vizsgálat a nifuroxazid és a probiotikumok összehasonlításában az akut hasmenés kezelésében
- Az ételallergia elsődleges megelőzése, a klinikai vizsgálatokból származó bizonyítékok átültetése a populációra
- Kutatási frissítések tesztelése élelmiszerallergiák ellen; Klinikai táplálkozási szolgáltatás a Cummings iskolában
- Purina Pro Plan állatorvosi diéták DM Dietetic Management macskatáp
- Bagoly étel; Vadászat - A bagoly oldalak