Táplálkozás és anyagcsere égési betegekben
Audra Clark
Texasi Egyetem délnyugati orvosi központja, 5323 Harry Hines Blvd., Dallas, TX 75390 USA
Jonathan Imran
Texasi Egyetem délnyugati orvosi központja, 5323 Harry Hines Blvd., Dallas, TX 75390 USA
Tarik Madni
Texasi Egyetem délnyugati orvosi központja, 5323 Harry Hines Blvd., Dallas, TX 75390 USA
Steven E. Wolf
Texasi Egyetem délnyugati orvosi központja, 5323 Harry Hines Blvd., Dallas, TX 75390 USA
Társított adatok
Absztrakt
A súlyos égés jelentős anyagcsere-zavarokat okoz, amelyek a táplálék-támogatást egyedülállóan fontossá és kihívássá teszik az égett betegek számára. Az égési sérülés tartós és hosszan tartó hipermetabolikus állapotot és fokozott katabolizmust okoz, ami fokozott izomvesztést és cachexiát eredményez. Az égési betegek anyagcseréje meghaladja a normális szint kétszeresét, és ezeknek az energiaigényeknek a teljesítése elmulasztja a sérült sebek gyengülését, a szervek működészavarát és a fertőzésekre való hajlamot. E betegek ellátásához elengedhetetlen a táplálkozási szükségletek megfelelő felmérése és kielégítése. Nincs egyetértés az égési betegek optimális időzítésével, útjával, mennyiségével és összetételével kapcsolatban, de a legtöbb orvos a korai enterális táplálkozást szorgalmazza magas szénhidráttartalmú tápszerekkel.
A táplálkozási támogatást egyénre kell szabni, figyelemmel kell kísérni és ki kell igazítani a gyógyulás során. További vizsgálatra van szükség az optimális táplálkozási támogatás, valamint a pontos táplálkozási végpontok és célok tekintetében.
Háttér
A táplálkozási támogatás kritikus szempont az égési betegek kezelésében. Ezeknek a betegeknek az anyagcseréje nagyobb lehet, mint a normálérték kétszerese, és ez a válasz a sérülés után több mint egy évig is tarthat [1, 2]. A hipermetabolikus állapotot súlyos katabolizmus kíséri, amely a sovány testtömeg óriási csökkenéséhez, valamint a gazda immunfunkciójának csökkenéséhez vezet [3]. A megnövekedett energiafogyasztáshoz szükséges jelentős táplálkozási támogatás létfontosságú az égett betegek túlélése szempontjából. Sajnos a táplálkozás bonyolult fiziológiájával kapcsolatos ismereteink hiányosak, és a táplálkozási rend az egyes központok között nagyban eltér. Sok kérdés merül fel még az étrend optimális útvonalával, mennyiségével és összetételével kapcsolatban az égési populációban. Ez a cikk áttekinti a táplálkozás jelenlegi állapotát égési sérülés után.
Felülvizsgálat
A hipermetabolikus állapot
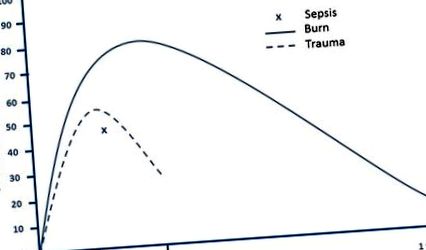
A súlyos égési sérülések mély patofiziológiai stresszreakciót és radikálisan megnövekedett anyagcserét okoznak, amely a sérülés után évekig fennmaradhat. A trauma és a szepszis szintén hipermetabolizmust eredményez, bár sokkal kisebb mértékben és lényegesen rövidebb ideig (1. ábra). Közvetlenül súlyos sérülés után a betegek csökkent anyagcserével és csökkent szöveti perfúzióval rendelkeznek, amelyet „apálynak” neveznek. Nem sokkal később belépnek a hipermetabolikus sebesség és a hiperdinamikus keringés fázisába, amelyet „áramlás” állapotnak neveznek [4]. Ez a hipermetabolikus állapot az egész test oxigénfogyasztásának növekedését tükrözi, és a beteget általában hipermetabolikusnak tekintik, ha a nyugalmi energia ráfordítás (REE) meghaladja a 10% -ot a normálistól [5]. Az akut, leégés utáni sérülési fázisban a teljes testfelület (TBSA) 40% -át meghaladó égési sérülés esetén a REE 40 és 100% között van a normálist meghaladó értéken [6, 7]. Fontos enyhíteni ezt a stresszreakciót és támogatni a páciens jelentősen megnövekedett anyagcsere-szükségleteit, mivel az ellenőrizetlen hipermetabolizmus a sovány izomtömeg óriási csökkenését, immunhiányt és késleltetett sebgyógyulást eredményez.
Hypermetabolikus válasz súlyos égés, trauma és szepszis után. Hivatkozások alapján adaptálva [5, 6, 123, 124]
Az égés utáni hipermetabolizmus nagyon bonyolult és még nem teljesen ismert. Ennek a hatalmas metabolikus, hormonális és gyulladásos diszregulációnak a mögöttes mechanizmusait még mindig aktívan vizsgálják. Sejt szinten az egész test megnövekedett oxigénfogyasztása támogatja az adenozin-trifoszfát (ATP) nagyobb forgalmát és termogenezisét. Az ATP-fogyasztó reakciók az égési sérülésekre adott hipermetabolikus válasz becsült 57% -át képviselik, ideértve a fehérjeszintézis ATP-forgalmát, a máj glükoneogenezisében az ATP-termelést, valamint a glükóz és zsírsavak körforgását [8]. Mivel az ATP-forgalom nem teljesen számol az égés okozta hipermetabolizmussal, ez azt jelenti, hogy a mitokondriális oxigénfogyasztás meghaladja az ATP-termelést súlyos égés után. Ez valószínűleg a mitokondriális légzés és az ADP-foszforiláció szétválasztásával történik, ami hőtermelést eredményez [5]. Ezt az elméletet támasztja alá az a közelmúltbeli megállapítás, miszerint az 1-es protein (UCP1), a mitokondriális transzmembrán fehérje és a termogenezis egyik fő közvetítője szétkapcsolása sokkal nagyobb az égési betegek zsírszövetében, mint egészséges egyénekben [9, 10].
Számos tanulmány szerint a katekolaminok a hipermetabolizmus elsődleges közvetítői [11, 12]. Az epinefrin, a kortizol és a glükagon katabolikus hormonszintjének emelkedése a fehérjeszintézis és a lipogenezis gátlásához vezet [13]. A fehérje lebontása szükséges és nagy energiaforrássá válik, és a vázizomzat cachexiája a fehérjeszintézis és a lebontás közötti tartós egyensúlyhiány következménye. A vázizom kinetikájának diszregulációja súlyos égés után egy évig vagy tovább tart, és a sérült testtömeg csökkenéséről számolhat be a betegek legfeljebb 3 évvel a sérülés után [14–16].
Sok más terápiát vizsgáltak az égés okozta hipermetabolizmus javítására. A környezeti menedzsment a betegek szobájának felmelegedésével és az okklúziós sebkötésekkel csillapítja a hipermetabolikus reakciót, mert az égési betegek elvesztették bőrgátját, ezért a hő semlegességének fenntartása érdekében több hőt kell termelniük. A korai sebkivágás és oltás javította a mortalitást, csökkentette az exudatív fehérje veszteséget, csökkentette az égési sebek fertőzésének kockázatát és csökkentette az izmok katabolizmusát [19, 23]. Ennek oka lehet a keringő gyulladásos citokinek, például az interleukin (IL) -6, IL-8, C3 komplement és a tumor nekrózis faktor (TNF) -α szintjének csökkenése [24].
Számos bevált farmakológiai módszer alkalmazható az égésre adott hipermetabolikus válasz csökkentésére. A béta-adrenerg receptor blokkolás, általában propranolollal együtt, súlyos égési sérülések esetén csökkenti a pulzusszámot és az anyagcserét [25–27]. A közelmúltban a propranolol-kezelés 1 éves postburn után javította a perifériás sovány testtömeg-felhalmozódást [28]. Kimutatták, hogy az oxandrolon, egy szintetikus androgén, tompítja a hipermetabolizmust, javítja a csont ásványianyag-tartalmát és sűrűségét, és növeli a sovány testtömeg növekedését súlyos égési sérülésekkel küzdő gyermekeknél [29–32]. A rekombináns humán növekedési hormonról (rHGH) kiderült, hogy csökkenti a hipermetabolizmust és javítja a sovány testtömeg-felhalmozódást az égés után, de két multicentrikus vizsgálat miatt korlátozottan alkalmazható, mivel a növekedési hormon terápia növelte a halálozást kritikus állapotú felnőtteknél [33–35]. További kutatásokra van szükség az rHGH égési betegekben történő alkalmazásának hatékonyságával és biztonságosságával kapcsolatban.
A táplálkozási támogatás időzítése
Kalóriaigény
Az égési betegek táplálkozási támogatásának elsődleges célja a hipermetabolikus állapot okozta megnövekedett kalóriaigény kielégítése, a túladagolás elkerülése mellett. Az évek során számos képletet fejlesztettek ki és használtak az égési sérülések kalóriaigényének becslésére [42]. Az egyik legkorábbi példa a Curreri-formula [43]. 1972-ben javasolták, és 9 beteg tanulmányozásával és hátrafelé történő kiszámításával hozták létre azoknak a kalóriáknak a közelítését, amelyekre a betegek fogyásának kompenzálására lett volna szükség. A Curreri-képlet és sok más régebbi formula túlbecsüli a jelenlegi anyagcsere-követelményeket, és kifinomultabb, különböző változókkal rendelkező képleteket javasoltak (1. táblázat) [44]. Az égési betegekben a kalóriaigény előrejelzésére szolgáló 46 különböző képlet egyik tanulmánya azt mutatta, hogy egyikük sem korrelált jól a 24 beteg mért energiafelhasználásával [1]. Az energiafogyasztás égés után ingadozik, és a rögzített képletek gyakran a legmagasabb energiafelhasználású időszakokban alultápláltsághoz és a kezelés végén késő takarmányhoz vezetnek.
Asztal 1
Az égési betegek kalóriaigényének kiszámításához használt általános képletek
| Felnőtt tápszerek | Kcal/nap | Hozzászólások |
| Harris Benedict | Férfiak: 66,5 + 13,8 (súly kg-ban) + 5 (magasság cm-ben) - 6,76 (életkor években) Nők: 655 + 9,6 (súly kg-ban) + 1,85 (magasság cm-ben) - 4,68 (életkor években) | Becsüli a bazális energiafelhasználást; az aktivitással és a stressztényezővel egyaránt beállítható, megszorozva 1,5-vel a gyakori égési stressz beállításához |
| Toronto Formula | −4343 + 10,5 (TBSA) + 0,23 (kalóriabevitel az elmúlt 24 órában) + 0,84 (Harris Benedict-becslés kiigazítás nélkül) + 114 (hőmérséklet) - 4,5 (a leégés utáni napok száma) | Hasznos az égési gondozás akut stádiumában; a monitorozási paraméterek változásával kell beállítani |
| Davies és Lilijedahl | 20 (súly kg-ban) + 70 (TBSA) | Túlértékeli a nagy sérülések kalóriaigényét |
| Ireton-Jones | Szellőztetett beteg: 1784 - 11 (életkor években) + 5 (súly kg-ban) + (244, ha férfi) + (239, ha trauma) + (804, ha ég) Nem szellőző beteg: 629 - 11 (életkor években) + 25 (súly kg-ban) - (609, ha elhízott) | Komplex képlet, amely integrálja a szellőzés és a sérülés állapotának változóit |
| Curreri | 16–59 éves kor: 25 (súly kg-ban) + 40 (TBSA) Életkor> 60: 20 (súly kg-ban) + 65 (TBSA) | Gyakran túlértékeli a kalóriaigényt |
| Gyermekgyógyászati tápszerek | ||
| Galveston | 0–1 év: 2100 (testfelület) + 1000 (testfelület × TBSA) 1–11 év: 1800 (testfelület) + 1300 (testfelület × TBSA) 12–18 év: 1500 (testfelület) + 1500 (testfelület × TBSA) | A testtömeg fenntartására összpontosít |
| Curreri junior | 1.0. Ez magyarázza az egyik félelmetes túladagolási szövődményt: nehéz leszoktatni a szellőztető támasztól [46]. Ennek az aggodalomnak az ellenére egy tanulmány megállapította, hogy a magas szénhidráttartalmú étrend gyermekek égési betegcsoportjában csökkent izomsorvadáshoz vezetett, és nem eredményezett 1,05-nél nagyobb RQ-értéket vagy légzési szövődményeket [47]. |
Aljzatok
Az anyagcsere folyamata a biológiai folyamatokhoz szükséges sok termék létrehozását és lebomlását foglalja magában. Három makrotápanyag - szénhidrátok, fehérjék és lipidek - metabolizmusa különböző utakon biztosítja az energiát (2. ábra).
- Onkológiai betegek ambuláns táplálkozási szolgáltatásai
- A táplálkozás a fej-, nyakrákos betegek ellátásának „nélkülözhetetlen” eleme
- Táplálkozás a csapatsportokban - FullText - Annals of Nutrition and Metabolism 2010, Vol
- Táplálkozás cisztás fibrózisban szenvedő betegeknél Európai Konszenzus - ScienceDirect
- Táplálkozás kezelése a macska onkológiai betegeknél - Ethos Veterinary Health