Túlzott táplálkozás és metabolikus kardiomiopátia
Chirag H. Mandavia
1 Missouri Egyetem Orvostudományi Kar, Belgyógyászati Klinika, Columbia, MO
3 Missouri Egyetem Orvostudományi Kar, Diabétesz és Kardiovaszkuláris Kutatóközpont, Columbia, MO
Lakshmi Pulakat
1 Missouri Egyetem Orvostudományi Kar, Belgyógyászati Klinika, Columbia, MO
3 Missouri Egyetem Orvostudományi Kar, Diabétesz és Kardiovaszkuláris Kutatóközpont, Columbia, MO
4 Harry S TrumanVeterans Affair Medical Center, Columbia, MO
Vincent DeMarco
1 Missouri Egyetem Orvostudományi Kar, Belgyógyászati Klinika, Columbia, MO
2 Missouri Egyetem Orvostudományi Kar, Orvosi Farmakológiai és Élettani Tanszék, Columbia, MO
3 Missouri Egyetem Orvostudományi Kar, Diabétesz és Kardiovaszkuláris Kutatóközpont, Columbia, MO
James R. Sowers
1 Missouri Egyetem Orvostudományi Kar, Belgyógyászati Klinika, Columbia, MO
2 Missouri Egyetem Orvostudományi Kar, Orvosi Farmakológiai és Élettani Tanszék, Columbia, MO
3 Missouri Egyetem Orvostudományi Kar, Diabétesz és Kardiovaszkuláris Kutatóközpont, Columbia, MO
4 Harry S TrumanVeterans Affair Medical Center, Columbia, MO
Absztrakt
A szív- és érrendszeri betegségeknek, amelyek az Egyesült Államokban a legmagasabb morbiditást és halálozást okozzák, számos fő kockázati tényező van, köztük az öregedés és a cukorbetegség. A túlsúly és az elhízás, különösen a hasi elhízás, egyre inkább önálló kockázati tényezőként szerepelnek a szív- és érrendszeri betegségek kialakulásában. A metabolikus és/vagy diabéteszes kardiomiopátia különösen a krónikus túlzott táplálkozás és a magas zsírtartalmú táplálkozás által okozott túlsúlyhoz kapcsolódik. A kezdeti szakaszban az elhízás ma már a szívzsírsav és a glükóz metabolizmusának jelentős diszregulációját okozza. Ezeket a rendellenességeket részben a megnövekedett oxidatív stressz okozza, ami viszont káros hatásokat okozhat a sejtek növekedését és proliferációját szabályozó intracelluláris jelátviteli utakon. Az oxidatív stressz ezen növekedése csökkent antioxidáns anyagokkal és a metabolikus jelátviteli utak szabályozatlanságával párosul. Az elhízásnál tapasztalt kardiomiopátia fokozott intersticiális fibrózissal és diasztolés diszfunkcióval jár. Idővel a fejlődő rendellenességek közé tartozik a hipertrófia és a szisztolés diszfunkció, ami végül szívelégtelenséghez vezet.
1. Bemutatkozás
2. A kardiorenalis metabolikus szindróma
3. A szív inzulin metabolikus jelátvitelének károsodása és a kapcsolódó szívműködési zavarok
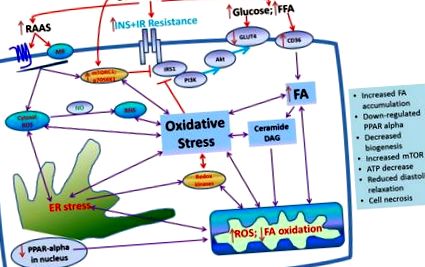
Az inzulinrezisztencia által közvetített túlzott táplálkozás hatása a celluláris oxidatív stressz és az azt követő metabolikus kardiomiopátia kialakulására a szívben.
Úgy gondolják, hogy az inzulin receptor szubsztrát (IRS-1) az inzulin szignál útvonal konvergencia pontja. A szerin foszforilezése több IRS-1 aminosavon csökkenti a tirozin foszforilációját és a downstream anyagcsere jelátvitelt. Bár az IRS-1 szerin-foszforilezéséhez több kináz is ismert, az mTOR/S6K1 útvonal különösen fontos a tápanyagok és a stressz által közvetített IRS-1 szerin-foszforilációban (11–13, 20). Az inzulin szívre gyakorolt jótékony hatásait az IRS-1/PI3K/Aktsignaling útvonal közvetíti, amely elősegíti a szívizom glükózfelvételét, az NO által közvetített véráramlást és a diasztolés relaxációt. Ennek eredményeként az anyagcsere és a hemodinamika közötti keresztbeszélés ennek eredményeként következik be az inzulin metabolikus szignalizációja a szívben (21–23). A túlzott táplálkozás és a túlzott RAAS-aktiváció egyre inkább felismerhető, hogy interaktív hatást gyakorolnak az mTOR/S6K1 jelátvitel stimulálására, ami viszont gyengíti az inzulinmetabolikus jelátvitelt a szív- és érrendszeri szövetekben (5, 11). Laboratóriumunk legújabb munkája azt jelzi, hogy az Ang II aktiválja az S6K1-t a szív és az érszövetben, és csökkent inzulin metabolikus jelátviteli és biológiai következményekhez vezet, például káros NO-mediált érrendszeri relaxációhoz, szívizom-glükóz-felhasználáshoz és diasztolés relaxációhoz (11).
Az S6K1 foszforilációját az mTOR által a szívben az rapTycinra érzékeny mTOR 1 komplex (mTORC1) közvetíti. Az mTOR szívtúlzott expressziója megvédi a bal kamrai (LV) nyomástúlterhelést követő szívműködési zavarokat. Továbbá a raptor, az állványfehérje, amely közvetíti az mTORC1 képződését és az mTOR szubsztrát aktiválódását, ablációja az adaptív hipertrófia károsodását eredményezi, és egerekben szívelégtelenséget okoz (2,11). Ezek a megfigyelések azt sugallják, hogy az mTORC1-aktiválás bizonyos körülmények között kardiovédő hatású lehet, és hangsúlyozzák az mTOR-közvetített jelátvitel jobb megértésének szükségességét a szív patológiájában. Kimutattuk, hogy a cardiacmTOR aktiválódik inzulinrezisztens Zucker elhízott patkányokban, de nem aktiválódik Zucker diabéteszes zsíros patkányok szívszöveteiben. Elképzelhető, hogy az mTOR aktivációjának hiánya a szívszövetben az elhízás okozta cukorbetegség körülményei között metabolikus váltás lehet inzulinhiány és előrehaladottabb diabéteszes kardiomiopátia (11). Csoportunk legújabb tanulmányai szintén megkezdték a keresztbeszélgetést a RAAS és az mTORC1 között, amelyet az angiotenzin-2-típusú receptor (AT2R) közvetített, és ezért lehetséges egy adaptív előnyös mTOR-AT2R jelző hurok megléte.
4. A szívzsírsav és a glükóz anyagcseréjének szabályozása
5. A metabolikus kardiomiopátia kialakulása
- Metabolikus olvadás (90 napos zsírvesztési kihívás)
- Metabolikus szindróma 6-11 éves gyermekek körében, Al Ain, Egyesült Arab Emírségek Az elhízás szerepe
- Metabolikus szindróma és jóindulatú prosztata hiperplázia Frissítés - ScienceDirect
- Metabolikus szindróma Hogyan segít az ideális fehérje az alakzat kialakulásában?
- Metabolikus szindróma gyermekeknél és serdülőknél