A GLP-1 hatása az étvágyra és a testsúlyra
Meera Shah
Endokrinológiai és Metabolizmus Osztály Mayo Clinic, 200 First ST SW, Rochester, MN 55905, USA
Adrian Vella
Endokrinológiai és Metabolizmus Osztály Mayo Clinic, 200 First ST SW, Rochester, MN 55905, USA
Absztrakt
A glükagonszerű peptid 1 (GLP-1) az előproglukagon gén hasítási terméke, amely a hasnyálmirigy α-sejtjeiben, a bél L-sejtjeiben, valamint a farok agytörzsében és a hipotalamuszban található neuronokban expresszálódik. A GLP-1 fontos az étvágy és a testsúly fenntartása szempontjából, mivel hatással van a gyomor-bél traktusra, valamint az étvágy közvetlen szabályozására. Késlelteti a gyomor kiürülését és a bélmozgást az embereknél. Ezenkívül a GLP-1 interventricularis injekciói gátolják a táplálékfelvételt, függetlenül az étel jelenlététől a gyomorban vagy a gyomor kiürülésében. A periférikusan beadott GLP-1 az etetés központi szabályozását is befolyásolja. Ezért a GLP-1 bélben és agyban kifejtett, mind a központi, mind a perifériás receptorokra ható szinergetikus hatásai látszólag felelősek a hormon jóllakottságra gyakorolt hatásáért.
1 A GLP-1 szintézise és szekréciója
A glükagonszerű peptid 1 (GLP-1) az előproglukagon gén [1] hasítási terméke, amely a hasnyálmirigy α-sejtjeiben, a bél l-sejtjeiben és a farok agytörzsében található neuronokban expresszálódik. és a hipotalamusz [2]. A GLP-1-et elsősorban a disztális vékonybél L-sejtjei szintetizálják és választják ki tápanyagterhelésre reagálva, bár nem tápanyagvezérelt szekrécióról is beszámoltak [3, 4]. A GLP-1-et a neuronok kis populációja szintetizálja a caudalis agytörzs magzati traktusának (NTS) magjában is, amelyek a hipotalamusz és a hátsó agy azon területeire vetülnek ki, amelyek expresszálják a GLP-1 receptorokat (GLP-1-R) [5 ]. A fő bioaktív fajok az emberekben a GLP-1 (7–36) amid és a GLP-1 (7–37).
2 A GLP-1 szerepe a jóllakottságban
A gyomor mechano-receptorainak aktiválásakor a gyomor kitágulása esetén a szatációs jeleket a vagális idegek közvetítik az agytörzs NTS-be. A táplálékfelvétel következtében fellépő gyomorfeszülés mértékét részben befolyásolja a gyomor kiürülésének sebessége, ami viszont befolyásolja az étkezés utáni glikémiás kirándulásokat. A GLP-1 késlelteti a gyomorürülést és a bélmozgást egészséges sovány és elhízott alanyokban, valamint 2-es típusú cukorbetegségben szenvedő betegeknél [15-17]. A GLP-1 szintén hozzájárul a gyomortérfogat változásához, amely az élelmiszer elfogyasztását megelőzően következik be. Ez a jelenség gyomor-befogadás néven ismert, és befolyásolhatja a gyomor duzzadásának észlelését étkezés után [18].
A vagus ideg szerepe a jóllakottság elősegítésében a GLP-1 beadásának útjától függ, amint azt egy vagotomizált patkányokon végzett kísérlet bizonyítja. Az intravénás és a GLP-1 intraperitoneális infúzióval szemben nincs szükség ép vagusra a tápanyagbevitel csillapításához [19].
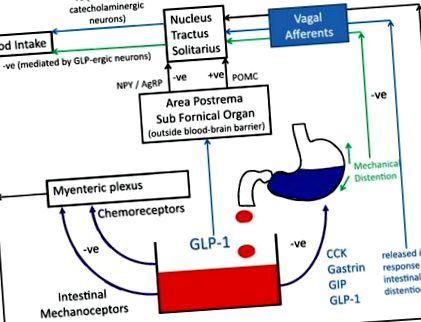
A GLP-1 központi (interventricularis) injekciói gátolják a táplálékfelvételt, függetlenül az étel jelenlététől a gyomorban vagy a gyomor kiürülésében [20]. Ugyancsak kimutatták, hogy a preproglucagon gén leütése az NTS-ben hyperphagia és súlygyarapodáshoz vezet [21]. Ezeket az eredményeket tükrözi neurovizáló vizsgálatok, amelyek azt mutatják, hogy a periférikusan beadott GLP-1 befolyásolja az agy aktivitását az etetés szabályozásában részt vevő területeken [22, 23]. Ezért a GLP-1 bélben és agyban kifejtett, mind a központi, mind a perifériás receptorokra ható szinergetikus hatásai látszólag felelősek a hormon jóllakottságra gyakorolt hatásáért (1. ábra).
A GLP-1 szerepe az étvágy modulálásában. A GLP-1 hatással van a központi és a perifériás receptorokra. A vagus relé információ afferens ágai a gyomor-bél traktus kemoreceptoraitól és mechanoreceptoraitól a nucleus tractus solitariusig (NTS). A keringő hormonok elméletileg közvetlenül stimulálhatják a vér-agy gáton kívül eső területeket, bár ennek az útnak a szerepe bizonytalan a normál fiziológiában (–ve gátló hatást, míg + ve megengedő/fokozó hatást jelent) [72,73,74]
Ezenkívül a GLP-1 intracerebroventrikuláris beadása feltételezett ízelhárítást indukálhat, valószínűleg a zsigeri érzés egyidejű hatása miatt [30].
Farmakológiai vizsgálatok állatokon kimutatták, hogy a táplálékfelvétel elnyomását a GLP-1 receptor agonisták, az exendin-4 és a liraglutid perifériás beadása után, a vagális afferenseken expresszált GLP-1R aktiválása, valamint a központi CNS GLP-1R közvetlen aktiválása közvetíti, kiemelve a a perifériás és a központi receptorok közötti kölcsönhatás fontossága [31].
3 A GLP-1 hozzájárulása a bariatrikus műtétekhez
Az étkezés utáni GLP-1 koncentrációja megnő a Roux-en-Y gyomor bypass után, amely megfigyelés felkeltette az érdeklődést a GLP-1 szerepének vizsgálata iránt a műtét utáni súlycsökkenés és az anyagcsere-zavarok remissziójának közvetítésében [32-34]
A bariatrikus műtétek minden formája kisebb-nagyobb mértékben fogyáshoz vezet. az RYGB fölénye az állítható gyomorszalaggal és esetleg a hüvelyes gasztrektómiával szemben kiemeli a tisztán korlátozó és a korlátozó/felszívódási zavarok közötti fontos különbséget. A pusztán korlátozó hüvelyes gasztrektómiához képest a 2-es típusú cukorbetegségben szenvedő betegeknél, akik RYGB-n estek át, nagyobb csontritkó-zsírvesztés és javult béta-sejtfunkció alakult ki a 24. hónapban annak ellenére, hogy a 12. hónapban hasonló cukorbetegség-remisszió történt [35]. Van néhány fontos figyelmeztetés ennek a tanulmánynak - ez a tanulmány kritizálható a kis (–er) számok áttekintése szempontjából, valamint az RYGB és SG csoportok közötti nemi különbségek (ezáltal a kezdeti testösszetétel szempontjából zavaró bevezetése) korlátozzák a test általánosíthatóságát. tanulmány [36].
Az állítható gyomorszalag (AGB) nem váltja ki a GLP-1 szekréciójának növekedését. Amikor azonban az AGB-n átesett patkányokat GLP-1 agonistával kezeltük, a testtömeg csökkent, miközben a sáv leeresztett és felfújt volt. Érdekes módon a sávinfláció kiváltotta az idegaktiválást az NTS azon területein, amelyekről ismert, hogy a GLP-1 receptor agonizmusa megcélozza őket, és potenciális mechanizmust kínál az interakcióra [37].
Mi és mások megvizsgáltuk az endogén GLP-1 szerepét a glükóz metabolizmusában az RYGB-t követően az Exendin 9,39 alkalmazásával, amely a GLP-1 kompetitív antagonistája rokon receptorán [38]. Nem diabéteszes alanyoknak, akik átlagosan 5 évvel voltak a RYGB után és állandó testsúlyúak, vegyes ételt adtak be; a glükóz fluxusokat 300 pmol/kg/perc sebességgel infundált Exendin 9,39 jelenlétében vagy távollétében vizsgálták. Az életkor és a testsúlynak megfelelő kontroll alanyokat hasonló kísérleti tervezéssel tanulmányozták. Az étkezés szilárd részének DTPA-jelölése lehetővé tette a gyomor ürítésének és az orocecalis tranzit mérését gamma kamerával. Megállapítottuk, hogy az Exe-9,39 felgyorsította a gyomor ürülését, ami arra utal, hogy az RYGB műtétet követően az endogén GLP-1 késlelteti a gyomor-béltranzitot. A gyomorürülés mérése szcintigráfiával az exendin 9,39 hatása alatt, egyébként egészséges emberekben sem hatást, sem gyorsított gyomorürítést nem mutattak ki [39, 40].
Bár fontos, a bariatrikus műtétek utáni súlycsökkenéshez és az anyagcsere-rendellenességek remissziójához való GLP-1 hozzájárulásának mértékét Wilson-Perez et al. aki a vertikális hüvelyes gasztrektómiát tanulmányozta GLP-1 receptor kiütéses egérmodellekben [41]. Ezek az egerek vad típusú társaikkal összehasonlítva hasonlóan reagáltak a testtömeg és a testzsír csökkenése, a glükóz homeosztázis javulása és az ételválasztás megváltozása szempontjából. Ezek az érdekes megállapítások mentesíthetik a GLP-1-et a vertikális hüvelyes gasztrektómia utáni jótékony eredmények nagy részének közvetítésétől, de nem feltétlenül vonatkoznak az RYGB-re, amely az anatómiát is újrakonfigurálja azáltal, hogy a disztális vékonybelet közelebb helyezi a gyomorból érkező tápanyagokhoz és megkerüli a proximális vékonybelet.
Azt, hogy a GLP-1 hozzájárul-e a bariatrikus műtét után észlelt súlycsökkenéshez, még meg kell határozni.
4 A GLP-1 szerepe a gyomor-bél traktusban
Úgy tűnik, hogy a GLP-1 mind a központi, mind a perifériás receptorokon kifejtett hatása révén befolyásolja a gyomor-bél motilitását. A vagus ideg fontos szerepet játszik ezeknek a hatásoknak a közvetítésében, amint azt mind az állati, mind az emberi modell megmutatta, talán a belek körizomára gyakorolt hatása révén [16, 42-44]. Egérmodellekben azt találták, hogy a GLP-1 gátolja a bél motilitását az enterális neuronokon a GLP-1R közvetlen kölcsönhatása és aktiválása révén [44]. Amikor a GLP-1-et közvetlenül beadták a patkányok intracerebroventrikuláris terébe, a gyomor kiürülését gátolták, ami kölcsönhatásra utalhat a perifériás és a központi GLP-1 receptorok között [45]. A felső emésztőrendszerrel ellentétben a vastagbélben a GLP-1 a vastagbél tranzitjának felgyorsítását szolgálja, amelyet valószínűleg a paraszimpatikus idegrendszer is közvetít [46, 47]. Ezenkívül a GLP-1 hozzájárul az ileális fékezéshez, amely egy gátló visszacsatolási hurok, amelynek célja a tápanyagok emésztésének és felszívódásának optimalizálása [48].
A vagális idegrendszer szerepét a GLP-1 gyomor elhelyezkedésére gyakorolt hatásainak közvetítésében ugyanaz a csoport tanulmányozta [50]. Két megfigyelés javasolta a vagus ideg fontos szerepét: 1. A gyomor tónusát vagális kolinerg bemenet tartja fenn. 2. Az étkezés utáni hasnyálmirigy-polipeptid felszabadulását (vagális kontroll alatt) tompítottuk GLP-1 jelenlétében.
A csoport a cukorbetegségben és a kardiovagális neuropátiában szenvedő betegeket vizsgálta ugyanazzal a kísérleti elrendezéssel, mint korábban. A GLP-1 nem befolyásolta a gyomor térfogatát ebben a csoportban, ami azt sugallta, hogy a vagálisan indukált mechanizmus fontos volt a GLP-1 gyomorban történő működéséhez. Azonban az étkezés gyomortérfogata ezekben a betegekben nem különbözött az egészséges önkéntesektől. Ez a megfigyelés azt szemlélteti, hogy a vagotomia utáni gyomor elhelyezkedése idővel helyreáll, amint azt állat- és emberkutatások is bizonyították.
5 Klinikai hatások a GLP-alapú terápia súlyára
Étkezésre adott válaszként a GLP-1 késlelteti a gyomor kiürülését és növeli a gyomor térfogatát. A GLP-1 fokozza az inzulin szekréciót és gátolja a glükagon felszabadulását glükózfüggő módon mind normális egyénekben, mind pedig 2-es típusú cukorbetegségben szenvedő betegeknél [51]. 2-es típusú cukorbetegségben szenvedő betegeknél a GLP-1 agonista infúzió farmakológiai dózisokban fokozta a jóllakottságot és elősegítette a fogyást [52]. Ennélfogva a GLP-1 terápia emberben csökkenti a táplálékfelvételt, az étvágyat és az éhséget, valamint elősegíti a teltséget és a jóllakottságot, a végeredmény pedig a fogyás elősegítése.
A GLP-1 agonista terápia (exenatid) randomizált, placebo-kontrollos vizsgálata elhízott serdülőknél mérsékelt súlycsökkenést eredményezett, amely hatás ugyanolyan vagy jobb volt, mint a hasonló időtartamú metformin vagy orlisztát kezelés ebben a betegcsoportban [63]. Az émelygés és hányás leggyakrabban jelentett mellékhatásai hasonlóak voltak a felnőttek szakirodalmában leírtakhoz, és nem eredményeztek lemorzsolódást a tanulmányból.
A GLP-1 agonista terápiával megfigyelt súlycsökkenés összefüggésbe hozható a teljes testzsír, különösen a visceralis és a truncalis zsírszint csökkenésével [64, 65].
Érdekes továbbá a GLP-1 agonisták sikeres alkalmazása a hipotalamusz elhízásának kezelésében, ami arra utal, hogy legalább ebben a kohorszban a GLP-1 analógok képesek súlycsökkenést kiváltani a hipotalamusz károsodása ellenére is [66].
A tiszta étrendtől eltérően a fogyás 3 évig tartható fenn GLP-1 agonista terápia jelenlétében [67, 68]. Ha azonban a terápiát abbahagyják, bizonyos mértékű visszanyerés tapasztalható [69]. Úgy tűnik, hogy a GLP-1 minimális hatással van az energiafogyasztásra önmagában, és így a GLP-1 terápia során tapasztalt negatív energiaegyensúly nagyrészt a csökkent energiafogyasztás eredménye [70].
6. Következtetés
A GLP-1 szerepét az étvágy és a súly modulációjában egy összetett agy-bél kapcsolat szervezi. A GLP-1-et elsősorban az enteroendokrin sejtek választják ki, de emellett a GLP-1 központi idegrendszeri forrása is van. A központi idegrendszerben és a bélben jelen lévő GLP-1 receptorok aktiválódását a vagus idegből származó kolinerg jelek tovább modulálják. Ezen és más, még mindig pontatlan mechanizmusok révén a GLP-1 mind fiziológiai, mind farmakológiai dózisokban elősegíti a jóllakottságot, befolyásolja a gyomor-bél traktus mechanisztikus tulajdonságait és negatív energiaegyensúlyt eredményez. Ezenkívül a fogyás előmozdításában elért sikere vonzó lehetőségsé teszi a GLP-1 agonista terápiát a 2-es típusú cukorbetegség kezelésében. Ezzel szemben egyensúlyba kell hozni a GLP-1 receptor agonista terápia és a hasnyálmirigy-gyulladás, a hasnyálmirigy-hiperplázia és a hasnyálmirigy-neoplazia közötti összefüggést [71]. Érdekesség, hogy egy új, transzgenikus egérmodellben végzett közelmúltban végzett munka megerősíti a GLP-1 receptorok jelenlétét az exokrin hasnyálmirigy érrendszerében, és csak a hasnyálmirigy-csatornákban azonosítható szórványos GLP-1 receptorok vannak [29]. Még mindig vita tárgyát képezi annak a következménye, hogy a GLP-1 agonista terápia közvetlenül kapcsolódik a megfigyelt káros eredményekhez.
7 Jövőbeli irányok
A GLP-1 felfedezése jelentős újításokat váltott ki a 2-es típusú cukorbetegség terápiájában, valamint a bél és a hasnyálmirigy közötti kölcsönhatás jobb megértését a glükóz homeosztázis, valamint az étvágy és a súly módosítása érdekében. Jelenleg a GLP-1 receptor agonizmusnak viszonylag kicsi, de jelentős hatása van a súlyra. Ennek okai még mindig bizonytalanok, és törekszenek a GLP-1 jelátvitelt csillapító endogén tényezők jobb megértésére. Sőt, azok a vegyületek, amelyek agonisták a GLP-1 és más, a súlyszabályozásban fontos receptorok számára, terápiás ígéreteket ígérhetnek.
Köszönetnyilvánítás
A szerzők elismerik a Mayo Klinika Általános Klinikai Kutatóközpont (DK TR000135) támogatását. Dr. Vellát a DK78646 és a DK82396 támogatja.
Dr. Vella kutatási támogatásokat kapott Mercktől és Daiichi-Sankyótól. A Novartis és a GI dinamikája által támogatott multicentrikus vizsgálatok nyomozója. Konzultált az XOMA, a Sanofi-Aventis, a Novartis és a Bristol-Myers Squibb munkatársaival.
Lábjegyzetek
Összeférhetetlenség Dr. Shah-nak nincs releváns közzététele.
Közreműködői információk
Meera Shah, Endokrinológiai és Metabolizmus osztály Mayo Klinika, 200 First ST SW, Rochester, MN 55905, USA.
Adrian Vella, Endokrinológiai és Metabolizmus osztály Mayo Klinika, 200 First ST SW, Rochester, MN 55905, USA.
- Teljes kiőrlésű gabonafélék fogyasztása a fogyás során az étrend minőségére, az élelmi rostokra gyakorolt hatása,
- Doc A gyógyszerek étvágytalansága fogyást okozhat
- Az epilepszia gyógyszer fogyáshoz vezet, mellékhatások Reuters
- Grigor Dimitrov súlycsökkenési mellékhatásokat tár fel egy hónapon belül a COVID-19 pozitív teszt, az Adria után
- A sótartalom füves ponty hatása a túlélésre, a fogyásra és az izomszövet víztartalmára