A szénhidrát-lipid anyagcserében részt vevő gének kifejeződése az izom- és zsírszövetekben a felnőttkori elhízás kezdeti szakaszában etetett és éheztetett egerekben
Fiziológiai genetika laboratóriuma, az Orosz Tudományos Akadémia szibériai részlege, a Szövetségi Kutatóközpont Citológiai és Genetikai Intézete, Novoszibirszk, Oroszország
Levelezés
Nadezhda M. Bazhan
Citológiai és Genetikai Intézet, Prospekt Lavrentyeva 10, Novoszibirszk, 630090, Oroszország.
Tel: +7 (383) 363-49-63
Fax: +7 (383) 333-12-12
Fiziológiai genetika laboratóriuma, az Orosz Tudományos Akadémia szibériai részlege, a Szövetségi Kutatóközpont Citológiai és Genetikai Intézete, Novoszibirszk, Oroszország
Fiziológiai Tanszék, Novoszibirszki Állami Egyetem, Novoszibirszk, Oroszország
Fiziológiai genetika laboratóriuma, az Orosz Tudományos Akadémia szibériai részlege, a Szövetségi Kutatóközpont Citológiai és Genetikai Intézete, Novoszibirszk, Oroszország
Fiziológiai genetika laboratóriuma, az Orosz Tudományos Akadémia szibériai részlege, a Szövetségi Kutatóközpont Citológiai és Genetikai Intézete, Novoszibirszk, Oroszország
Fiziológiai genetika laboratóriuma, az Orosz Tudományos Akadémia szibériai részlege, a Szövetségi Kutatóközpont Citológiai és Genetikai Intézete, Novoszibirszk, Oroszország
Levelezés
Nadezhda M. Bazhan
Citológiai és Genetikai Intézet, Prospekt Lavrentyeva 10, Novoszibirszk, 630090, Oroszország.
Tel: +7 (383) 363-49-63
Fax: +7 (383) 333-12-12
Fiziológiai genetika laboratóriuma, az Orosz Tudományos Akadémia szibériai részlege, a Szövetségi Kutatóközpont Citológiai és Genetikai Intézete, Novoszibirszk, Oroszország
Fiziológiai Tanszék, Novoszibirszki Állami Egyetem, Novoszibirszk, Oroszország
Fiziológiai genetika laboratóriuma, az Orosz Tudományos Akadémia szibériai részlege, a Szövetségi Kutatóközpont Citológiai és Genetikai Intézete, Novoszibirszk, Oroszország
Fiziológiai genetika laboratóriuma, az Orosz Tudományos Akadémia szibériai részlege, a Szövetségi Kutatóközpont Citológiai és Genetikai Intézete, Novoszibirszk, Oroszország
Finanszírozási információk:
Ezt a tanulmányt az Orosz Tudományos Alapítvány támogatta, 17-15.01036. Sz. Támogatás.
Absztrakt
Bevezetés
Embereknél és rágcsálóknál az elhízás előfordulása születéstől középkorig növekszik (Barzilai et al. 1998; Facchini et al. 2001; Mizuno et al. 2004). Laboratóriumi egerekben a középkorba beletartozik a 9 és 12 hónap közötti időszak (Flurkey és mtsai 2007; Jacobson 2002; Rusli és mtsai 2016). Az egerek azonban jóval a középkor előtt, a késői felnőtt korban (6 hónap) kimutatták a glükóz metabolizmusának károsodását, amelyben az inzulin és a vér glükóz koncentrációja nő (Stenbit et al. 1997) és az inzulin érzékenység csökken (Mizuno és mtsai 2004). A szénhidrát-anyagcsere szabályozatlanságát okozó élettani mechanizmusok a késői felnőtt korban a normális fejlődés során nem ismertek.
Ez a tanulmány azt mutatja, hogy a normál fejlődés során a C57Bl egerek megnövelték a WAT és BAT indexeket és csökkentek a glükóz toleranciát a késői felnőtt szakaszban. Eredményeink azt sugallják, hogy ezeket a változásokat az életkorral összefüggő enzimrendszeri aktivitás csökkenése okozhatja β- az FFA oxidációja az izmokban, a TG lipolízis a WAT-ban és a termogenezis a BAT-ban. Adataink új információkat nyújtanak az elhízás és a szénhidrát-lipid anyagcsere diszregulációjának hátterében álló mechanizmusokról a középkor előtt egerekben.
Mód
Etikai jóváhagyás
Valamennyi kísérletet a „Kísérleti és egyéb tudományos célokra használt gerinces állatok védelméről szóló európai egyezménynek” és a laboratóriumi állatok gondozására és felhasználására vonatkozó orosz nemzeti utasításoknak megfelelően hajtották végre. A jegyzőkönyveket az Orosz Tudományos Akadémia Szibériai Kirendeltsége, a Citológiai és Genetikai Intézet Független Etikai Bizottsága hagyta jóvá (35. jegyzőkönyv, 2016. október 26.). Minden erőfeszítést megtettek az állatok szenvedésének minimalizálása és a felhasznált állatok számának csökkentése érdekében.
Állatok és kísérleti protokoll
A C57Bl egereket a Citológiai és Genetikai Intézet viváriumában tenyésztették (Szibériai Kirendeltség, Orosz Tudományos Akadémia, Novoszibirszk). Az egereket 12: 12-órás világos-sötét rendben tartottuk 22 ° C környezeti hőmérsékleten. Az egereknek ad libitum hozzáférést biztosítottak a kereskedelmi egér-chow-hoz (Assortiment Agro, Moszkva régió, Turacovo, Oroszország) és a vízhez. A hím egereket elválasztották az anyáktól 28 napos korukban, és a kezelésig külön-külön tartották őket.
Az állatokat véletlenszerűen három korcsoportra osztottuk: 10 hét (fiatal egerek), 15 hét (korai felnőtt egerek) és 30 hét (késői felnőtt egerek) Flurkey és munkatársai osztályozási sémája szerint. (2007). Megfelelő korban az egereket 10: 00-kor lemértük, az ételt 18: 00-10: 00 között megfosztották, éjszakai böjt után ismét lemérték (a vízhez való hozzáférés ad libitum maradt), és OGTT-nek vetették alá (csoportonként 12–13 egér). Az OGTT elvégzéséhez a glükózt orálisan (2 mg/testtömeg-g) adtuk be 18: 00-10: 00 közötti éhomi éhgyomri után, majd a vérből mintát vettünk a farokvénából a glükóz beadása előtt, valamint 15, 30, 60 és 120 perccel a glükóz beadása után. . A vércukor-koncentrációt az alábbiakban leírtak szerint határoztuk meg.
Négy nappal az OGTT után az egyes korcsoportok egereit két alcsoportra osztották: kontroll és koplalás (6-7 egér alcsoportonként). Az éhomi csoportban az egereket 18:00 és 10:00 óra között megfosztották az élelemtől (a vízhez való hozzáférés ad libitum volt), és néhány másodpercen belül érzéstelenítés nélkül lefejezéssel leölték őket. A törzsvért műanyag csövekbe gyűjtötték EDTA-val és jégen hűtötték. A plazmát centrifugálással elválasztottuk, és a vizsgálatokig -20 ° C-on fagyasztottuk. A perigonadal WAT-t és az interscapularis BAT-ot azonnal boncoltuk, lemértük és folyékony nitrogénben gyorsan lefagyasztottuk a génexpresszió későbbi mérése céljából. A zsírszövetek tömegindexeit a zsírszövet és a testtömeg (BW) arányaként számítottuk ki. A combizom mintákat is összegyűjtötték és lefagyasztották.
Biokémiai vizsgálatok
A vércukorszintet glükométerrel határoztuk meg (One Touch Basic Plus, Lifescan, Oroszország). A glükóz, inzulin, FFA és TG plazmakoncentrációit kereskedelmi készletekkel mértük (Fluitest GLU, Analyticon Biotechnologies, Lichtenfels, Németország, glükózhoz; Patkány/Egér ELISA készlet, EMD Millipore, Missouri, USA, inzulinhoz; DiaSys Diagnostic Systems GmbH (Holzheim, Németország, az FFA; és a DAIKON ‐ DC, Pushchino, Oroszország, a TG esetében). Az éhomi egerek plazmájában nem mértük az inzulin koncentrációt, mivel néhány minta elveszett egy technikai hiba (áramhiány) miatt, amelyet nem tudtunk ellenőrizni.
Relatív kvantifikációs valós idejű PCR
Statisztikai analízis
Minden adatot átlag ± SEM értékként fejeztünk ki. Kétirányú ANOVA-t használtak az összes adat (kivéve az OGTT vércukorszintjét és a plazma inzulinszintjét) életkorával (10, 15 és 30 hét) és a kísérleti körülményekkel (etetett és éheztetett) magyarázó tényezőként. Az OGTT alatti vércukor-koncentrációt kétirányú, ismételt mérésekkel elemeztük az ANOVA-val, életkorral (10, 15 és 30 hét) és a glükóz beadása utáni idővel (0, 15, 30, 60 és 120 perc) magyarázó tényezőként. A plazma inzulin koncentrációit csak etetett állatoknál mértük, és magyarázó tényezőként egyirányú ANOVA-val elemeztük életkorukkal (10, 15 és 30 hét). Duncan több tartományú tesztjét alkalmazták a csoportok közötti post hoc összehasonlításokhoz. Minden elemzéshez a STATISTICA 6 szoftvercsomagot (StatSoft) használtuk. A különbségeket statisztikailag szignifikánsnak tekintették P
Eredmények
Testtömeg, szöveti tömeg és vérparaméterek
A testtömeg az életkor előrehaladtával nőtt (F2,65 = 100,3, P
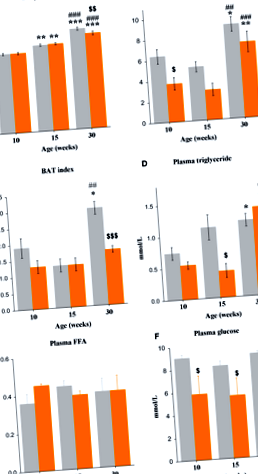
A plazma TG koncentrációja az életkor előrehaladtával nőtt (F2,27 = 7,6, P
A plazma inzulin koncentrációja a táplált egerekben 10 és 30 hét között nőtt (F2,26 = 6,6, P
Az energia-anyagcserével kapcsolatos gének vázizom-expressziója
Táplált egereknél izom Ucp3 a gén expressziója az életkorral megváltozott. Ucp3 A mRNS szintje a 15 hetes egerekben magasabb volt, mint a 10 hetes egerekben (P
Az energia-anyagcserével kapcsolatos gének zsírszöveti expressziója
Táplált egerekben a WAT mRNS expressziója Lipe az életkorral változott (F2,28 = 37,8, P
Vita
A kutatók jelentős adatokat gyűjtöttek, amelyek azt mutatják, hogy normális fejlődés során emberekben (Daviglus et al. 2003; Mizuno és mtsai 2004; Yoneshiro és mtsai 2011) és rágcsálókban (Gruenewald és Matsumoto 1991; Jacobson 2002; Sasaki 2015) középkorú egyének ( az embereknél 40-50 év [Mizuno és mtsai 2004] és az egereknél 9-12 hónap [Flurkey és mtsai 2007; Gruenewald és Matsumoto 1991]) meghatározzák az elhízás és a glükóz anyagcsere zavara gyakoribb előfordulását a fiatalabb korosztályhoz képest. A metabolikus indexek vizsgálata három korcsoportba tartozó egereken, beleértve a fiatalokat (10 hét), a korai felnőtteket (15 hét) és a késői felnőtteket (30 hét) (Flurkey és mtsai 2007) feltárta, hogy az életkorral összefüggő változások a szénhidrát-lipid anyagcserében egereknél jóval a középkor előtt, vagyis a felnőttkori késői stádiumban fordulnak elő. A normális fejlődés során a késői felnőtt egerek bizonyítják az elhízás kialakulását, beleértve a WAT és BAT index kétszeres növekedését, a plazma triglicerid és inzulin szintjének emelkedését, valamint a csökkent glükóz toleranciát. A késői felnőtt korban az energia-anyagcsere változását okozó mechanizmusokat még nem sikerült meghatározni.
Vizsgálatunk feltárta, hogy a későn felnőtt egerek a kezdő elhízással párhuzamosan csökkent glükóz-anyagcserét mutattak, beleértve a megnövekedett plazma inzulinszintet, csökkent glükóz toleranciát a fiatalabb egerekhez képest és csökkent Slc2a4 gén a WAT-ban (a korai kifejlett egerekhez képest). A Glut4 egy inzulinfüggő glükóz transzporter, amelynek aktivitása befolyásolja a glükóz felvételét az egész szervezet szintjén. Kimutatták, hogy az életkorral összefüggő WAT csökkenés Slc2a4 a génexpresszió a csökkent glükóz tolerancia (Li et al. 2014) és az inzulinrezisztencia (Hofmann et al. 1991) kialakulásával jár együtt, míg Slc2a4 a túlzott expresszió javítja az inzulinrezisztenciát (Carvalho et al. 2005). Feltételezhető, hogy a késői felnőtt stádiumban az egerek glükóz toleranciája is csökkent a WAT arányának növekedése miatt, mert az adipocita termékekről ismert, hogy elnyomják az intracelluláris inzulin szignál útvonalakat (Ye 2013). A késői felnőtt korban bekövetkezett káros glükóz-anyagcsere adatai összhangban vannak más vizsgálatok eredményeivel, amelyek a megemelt inzulin- és vércukor-koncentrációt (Stenbit et al. 1997) és az inzulinérzékenység csökkenését mutatják be a 30 hetes C57Bl egerekben (Mizuno és mtsai. 2004).
Az életkorral összefüggő csökkenés Ucp3 génexpresszió az izmokban és Slc2a4 táplált késői felnőtt egerekben megfigyelt WAT-ban nem volt hatással e gének éhgyomorra történő transzkripciós válaszaira, összehasonlítva más korcsoportok válaszával. Böjt közben, Ucp3 az egerekben a génexpresszió minden korban élesen megnőtt, ami megfelel a rágcsálókkal (De Lange és mtsai 2006; Sánchez és mtsai 2009) és emberekkel (Millet és mtsai 1997) végzett egyéb vizsgálatok eredményeinek. Ucp3 a génexpressziós aktiváció az éhezéshez való alkalmazkodás fontos eleme, mivel az UCP3 csökkenti a mitokondriális membránpotenciált, megvédi az izomsejteket a zsírsavak túlterhelésétől és csökkenti a reaktív oxigénfajok túlzott termelését (Amat et al. 2007). Az éhezésről ismert, hogy nemcsak az anyagcsere-rendszer terhelését, hanem érzelmi stresszt is okoz, és emeli a perifériás vér glükokortikoid szintjét is (Bazhan et al. 2017; Viscarra és Ortiz 2013), serkentően Ucp3 gén expresszió egerekben (Amat és mtsai 2007; Nagase és mtsai 2001). Úgy tűnik, hogy a vizsgált életkorban az egereknél az éhgyomri okozta stresszre adott válasz nem különbözött, ami hasonló növekedést eredményezett Ucp3 gén expresszió az izmokban.
Átírási válaszok a böjtre Cpt1 gén a késő felnőtt egerekben a vázizomzatban jelentősen eltért a fiatalabb egerekétől. A koplalás hatására a fiatal egerek jelentősen megnövelték az izmokat Cpt1 génexpresszió. Ez az eredmény összhangban van a patkányizmok más tanulmányainak eredményeivel (De Lange et al. 2006). A korai és késői felnőtt egereknél a koplalás nem változott Cpt1 mRNS szintek. Úgy gondoljuk, hogy a korai felnőtt egerekben a stimuláció hiánya a „plafon” hatással magyarázható, azaz., Cpt1 A táplált egerek mRNS-szintje olyan magas volt, mint a fiatal éhomi egerekben. A koplalás nem növelte az izom Cpt1 mRNS szintjét a korai felnőtt egerekben, mivel a génátírás már a csúcsponton volt, vagy annak közelében volt, néhány életkorhoz kapcsolódó tényező által kiváltott aktiváció miatt. Úgy gondolják, hogy a késői felnőtt egerek változásának hiánya az életkor függvényében bekövetkezett károsodásnak felel meg egy adott tényezőre, amely aktiválódik az éhgyomorra, valószínűleg az FFA-ra. Alacsony izomszint megőrzése Cpt1 Az éhgyomorra történő génexpresszió megakadályozhatja az alkalmazkodást a zsírsavak energiaforrásként történő használata miatt az izmokban.
A felnőtt C57Bl egereket széles körben használják a szénhidrát-lipid anyagcsere különböző aspektusainak tanulmányozására. Meg kell jegyezni, hogy az izmok gén expressziójában, valamint a posztpubertus szakaszban a WAT és a BAT jelentős korfüggő változásai megelőzik a késői felnőtt kort, és hogy az elhízás késői felnőtt korban bekövetkező hatása befolyásolhatja ezeket az eredményeket.
Így ez a tanulmány első alkalommal feltárta, hogy a normális fejlődés során még késői felnőtt korban is a TG hidrolízisben részt vevő gének expressziója, a WAT glükózfelvétel, az izom FFA oxidációja és a BAT termogenezise meredeken csökkent (a korai felnőtt korhoz képest). A perifériás metabolikus szervek enzimjeinek késői felnőtt korban bekövetkező károsodott lipid- és glükóz-metabolizmusban betöltött szerepéről azonban csak a megfelelő fehérjék expressziójának és az enzimaktivitás mérése után lehet következtetni. Az egerek normális fejlődése során elhízást kiváltó mechanizmusok vizsgálata releváns, mivel a későbbi korú elhízás olyan életveszélyes állapotokra hajlamosítja őket, mint az inzulinrezisztencia, a 2-es típusú cukorbetegség és a szív- és érrendszeri betegségek.
- Örökölted a zsírgéneket az igazságot a biológiáról és a testzsír izomzatáról és erejéről?
- Célozható-e táplálék-kiegészítőkkel a testzsír-veszteség és a sovány izomtömeg-növekedés
- Legyen erős a hínár izomzatával; Fitness
- Több görög joghurtot vegyen be étrendjébe a sovány izomtömeg felépítéséhez és a fogyáshoz
- Ezzel a 10 perces edzéssel kapjon hat csomagot az izomzat zsírégetéséhez; Fitness