A szildenafil-citrát hosszú távú biztonságossága és hatékonysága merevedési zavarban szenvedő férfiaknál
James G McMurray
1 Orvosi Társult Kutatóközpont, Huntsville, AL, USA
Robert A Feldman
2 Connecticuti Klinikai Kutatóközpont, Waterbury, CT, USA
Stephen M Auerbach
3 kaliforniai szakmai kutatás, Newport Beach, Kalifornia, USA
Gyógynövény DeRiesthal
4 Pfizer Inc., New York, NY, USA
Neal Wilson
5 Korábban Pfizer Global Research and Development, Sandwich, Egyesült Királyság, jelenleg PPD Inc, Cambridge, Egyesült Királyság
A Multicenter Study Group nevében
A multicentrikus vizsgálati csoport 6 tagját a melléklet sorolja fel
Absztrakt
Bevezetés
1998 márciusában az Egyesült Államok Élelmiszer- és Gyógyszerügyi Hivatala (FDA) jóváhagyta a szildenafil-citrátot (Viagra ®, Pfizer Inc., New York, NY, USA) az erekciós diszfunkció (ED) kezelésére (FDA 1998). 2005 decemberében világszerte több mint 27 millió férfi kapott szildenafilt az ED kezelésére, köztük az Egyesült Államokban becslések szerint 17 millió férfi (Data on file, Pfizer Inc, New York, NY). Így a szildenafil hosszú távú biztonságossága és hatékonysága már értékelhető azoknál a férfiaknál, akik több éve szedik a gyógyszert.
A szildenafil hatékonyságát, biztonságosságát és tolerálhatóságát ED-ben szenvedő férfiak kezelésében számos, legfeljebb 1 éves időtartamú vizsgálat bizonyította. Például 1358 ED-ben szenvedő férfi teljesítette a 4 kettős-vak vizsgálat közül az egyiket, és folytatta a nyílt szildenafil-kezelést a kiterjesztett vizsgálatokban, a kezelés teljes időtartama körülbelül 1 év volt (Morales és mtsai 1998; Steers és mtsai 2001). A jelenlegi vizsgálatban ezek közül a férfiak közül 979 kapott még további 4 évig nyílt, rugalmas dózisú (25, 50 és 100 mg) szildenafilt. Az előzetes (3 éves) eredményekről korábban beszámoltunk (Carson et al 2002; Padma-Nathan et al 2002), és most bemutatjuk a végleges adatokat. A populációba szerves és pszichogén etiológiájú ED-ben szenvedő betegek, valamint e populáció tipikus, egyidejűleg jelentkező egészségi állapotai voltak (azaz magas vérnyomás, cukorbetegség, hiperlipidémia és a kórelőzményben iszkémiás szívbetegség volt). Célunk az volt, hogy értékeljük a szildenafil kezelés hosszú távú biztonságosságát és hatékonyságát ED-ben szenvedő férfiaknál.
Mód
Ez egy 4 éves, nyílt, rugalmas dózisú (25, 50 és 100 mg) szildenafil-vizsgálat volt. Azok a férfiak, akik a 4 kettős-vak, placebo-kontrollos vizsgálat közül az egyikben korábban befejezték a szildenafil- vagy a placebo-kezelést, és ezt követően megfeleltek a szildenafil-kezelésnek, és a kezdeti nyílt kiterjesztés során a szildenafil-kezelésnek megfeleltek, megfeleltek e hosszú távú kiterjesztési vizsgálat. A tanulmányi gyógyszert költség nélkül biztosították. A megfelelést gyógyszeres naplók és a tanulmányban való folyamatos részvétel alapján értékelték.
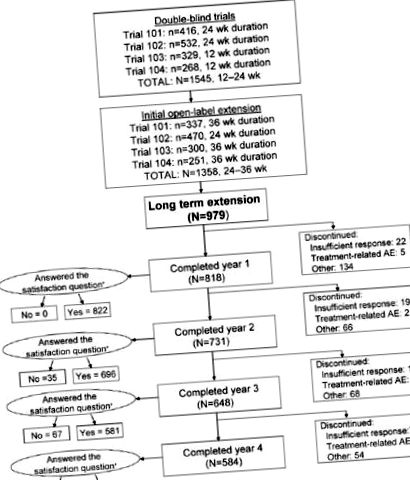
A kettős-vak vizsgálatokba eredetileg 1545 férfit vontak be, ebből 1358 férfi folytatta a kezdeti, nyílt kiterjesztésű vizsgálatokban. A jelenlegi vizsgálat 979 eredeti beteget foglal magában, akik beleegyeztek abba, hogy részt vegyenek a hosszú távú kiterjesztésben (1. ábra). Az eljárások összhangban voltak az emberi kísérletekkel foglalkozó illetékes bizottság (intézményi vagy regionális) etikai normáival.
A betegek száma és a kezelés időtartama az eredeti kettős-vak vizsgálatokban, valamint a nyitott, rugalmas dózisú (25, 50 és 100 mg) szildenafil hosszú távú kiterjesztésű vizsgálat kezdeti nyílt kiterjesztésében és elrendezésében 4 éven át. A szildenafil hosszú távú kiterjesztési vizsgálatba bekerült 979 résztvevő közül 584 (60%) teljesítette mind a 4 évet. A megszakítás okai, az elégtelen klinikai válasz és a kezeléssel összefüggő nemkívánatos események (AE) kivételével, magukban foglalták a kezeléssel nem összefüggő AE-t, a protokoll megsértését, a nyomon követés elvesztését és egyéb (pl. A klinikai vizsgálatban való részvétel iránti érdeklődés elvesztése, veszteség szexuális partner és a jóváhagyás után a szildenafil megengedhetõsége [így a gyógyszer megszerzéséhez már nem kell klinikai vizsgálatban részt venni]). Az elégedettségi kérdés N („Elégedett-e a kezelés erekciójára gyakorolt hatásával?”) Megegyezik a válaszolt férfiak számával. * A megszakított alanyok egy része elégedettségi adatokat szolgáltatott.
A vizsgálat megkezdésekor az FDA kijelentette, hogy elegendő rutinbiztonsági adat áll rendelkezésre a szildenafilról ahhoz, hogy szükségtelenné tegye a szokásos mellékhatások gyűjtését. Ezért csak súlyos adagokat és mellékhatásokat, amelyek az adagolás megváltozásához vagy ideiglenes vagy végleges abbahagyáshoz vezettek, rögzítették és értékelték a kutatók a szildenafil-kezeléssel való összefüggés szempontjából.
Mivel ennek a tanulmánynak a fő hangsúlya a biztonság volt, és a betegek által jelentett eredmények kidolgozása és validálása előtt tervezték az erekció minőségével (pl. Erekció minősége kérdőív (Porst et al 2007)) vagy az ED-vel való elégedettség értékelésére. kezelés (pl. a merevedési zavarok kezelésének elégedettségéről szóló jegyzék (Althof és mtsai 1999)), a hatékonyságot úgy értékelték, hogy évenként vagy a kezelés megszakításakor egyszerű, nem validált általános hatékonysági kérdéseket tettek fel: „Elégedett-e a kezelés hatásával erekció? ” és „Ha igen, javította-e a kezelés a szexuális tevékenységben való részvétel képességét?” A második kérdés az Országos Egészségügyi Intézetek Konszenzus Konferenciájának ED-definícióján alapult: „... képtelenség elérni és/vagy fenntartani a pénisz erekcióját a kielégítő szexuális teljesítményhez.” (NIH Konszenzus Konferencia. Impotencia. NIH Konszenzus Fejlesztő Testület az impotenciáról 1993). Leíró statisztikákat számoltunk ki.
Eredmények
Összességében 979 férfi kezdetben vállalta a részvételt a vizsgálatban, akik közül a legtöbb fehér (89%) és átlagos életkora 58 év volt (1. táblázat). A kettős-vak kísérletek és a kezdeti nyitott kiterjesztés időtartama 0,9–1,2 év (48–60 hét) volt. A nyílt, hosszú távú kiterjesztési vizsgálatban való részvétel medián időtartama 4 év volt, a bevett dózisok mediánszáma 420 (tartomány, 1–1469) (2. ábra), az előnyös dózis 100 mg volt több mint 88 a férfiak% -a. A megtartási arány az első évben 84% (818/979), a második évben 75% (731/979), a harmadik évben 66% (648/979) volt; a teljes 4 éves hosszabbítási vizsgálatot a kezdeti 979 férfi 584 -a (60%) fejezte be (1. ábra). A kezelés abbahagyásának okai között szerepelt a klinikai vizsgálatban való részvétel iránti érdeklődés elvesztése, a szexuális partner elvesztése, a nyomon követés elvesztése, a szildenafil engedélyezésének képessége (tehát a gyógyszer megszerzéséhez már nem kell részt venni egy klinikai vizsgálatban), elégtelen klinikai válasz és nemkívánatos események.
A vizsgálatba bekerült 979 résztvevő rugalmas dózisú (25, 50 és 100 mg) szildenafil alkalmazását 2–1561 nap alatt.
Asztal 1
A 979 férfi kiindulási jellemzői
| Kor, átlagos (tartomány) évek | 58,2 (27–82) |
| Súly, átlag (tartomány) kg | 89,2 (53,5–158,8) |
| Verseny, n (%) | |
| fehér | 873 (89,2) |
| Fekete | 68 (6.9) |
| ázsiai | 8 (0,8) |
| Egyéb | 30. cikk (3.1) |
| ED időtartama, átlagos (tartomány) évek | 4,5 (0,1–35,8) |
| ED etiológia,% szerves/vegyes/pszichogén | 72/17/11 |
| Gyakori kísérő betegségek, n (%) | |
| Magas vérnyomás | 272 (27,8) |
| Diabetes mellitus | 213 (21,8) |
| Hyperlipidemia | 139. (14.2.) |
| Az iszkémiás szívbetegség története | 83. (8.5.) |
Tolerálhatóság
2. táblázat
Nemkívánatos események, amelyek az adagolás megváltozásához vagy ideiglenes vagy végleges abbahagyásához vezettek
| AE-s betegek, n (%) | 37. cikk (3.8.) | 210 (21,5) |
| Megszűnt AE-k miatt, n (%) | 11. cikk (1.1) | 55 (5.6) |
| A leggyakoribb (≥0,5%) AE-k, n (%) | ||
| Fejfájás | 10 (1,0) | 10 (1,0) |
| Dyspepsia | 10 (1,0) | 12. cikk (1.2) bekezdés |
| Rhinitis | 6 (0,6) | 6 (0,6) |
| öblítés | 5 (0,5) | 5 (0,5) |
| A koszorúér rendellenessége | 0 | 24. (2.5) |
| Prosztata rendellenesség | 0 | 16. (1.6) |
| Carcinoma | 0 | 14. cikk (1.4) |
| Miokardiális infarktus | 0 | 11. (1.1) bekezdés b |
| Ízületi gyulladás | 0 | 9 (0,9) |
| A csonttörés véletlen | 0 | 9 (0,9) |
| Véletlen sérülés | 0 | 7 (0,7) |
| Agyi érrendszeri rendellenességek | 0 | 7 (0,7) |
| Pitvarfibrilláció | 0 | 6 (0,6) |
| Kolecisztitisz | 0 | 6 (0,6) |
| Vérmérgezés | 0 | 5 (0,5) |
| Szív elégtelenség | 0 | 5 (0,5) |
| Emésztőrendszeri karcinóma | 0 | 5 (0,5) |
| Csontzavar | 0 | 5 (0,5) |
Minden kezelési évben az évet kezdő férfiak kevesebb mint 1% -a hagyta abba a szildenafil alkalmazását a kezeléssel összefüggő nemkívánatos események miatt, az eredeti 979 résztvevő közül csak 11 (1,1%) a vizsgálat 4 éve alatt (3. táblázat ). A kezelés abbahagyását dyspepsia (n = 4), rhinitis (n = 2), rendellenes látás és fejfájás (n = 1), dyspepsia és rhinitis (n = 1), kipirulás, szédülés és myalgia okozta (n = 1 mindegyik).
3. táblázat
Megszakítás 4 év alatt
| 1 | 0,5 (5/979) | 2,2 (22/979) | 13,7 (134/979) |
| 2 | 0,2 (2/818) | 2,3 (19/818) | 8,1 (66/818) |
| 3 | 0,1 (1/731) | 1,9 (14/731) | 9,3 (68/731) |
| 4 | 0,5 (3/648) | 1.1 (7/648) | 8,3 (54/648) |
Hatékonyság
A vizsgálatban részt vevő 979 férfi közül 932 (95%) hatékonyságát elemezték. Minden év végén az évente csökkenő résztvevők számának legalább 94% -a számolt be elégedettségéről a szildenafil-kezelés erekciójára gyakorolt hatásával, a 4 éves értékelés során csak 3,3 százalékpontos eltérés mutatkozott (4. táblázat). Ezeknek a férfiaknak szinte mindegyike javult szexuális tevékenység iránti képességéről.
4. táblázat
A szildenafil-kezelés eredménye 4 év alatt
| 1 | 98,1 (806/822) | 99,6 (803/806) |
| 2 | 96,6 (672/696) | 99,9 (671/672) |
| 3 | 94,8 (551/581) | 99,6 (549/551) |
| 4 | 96,3 (550/571) | 100 (550/550) |
Minden kezelési évben az évet kezdő férfiak kevesebb mint 3% -a hagyta abba a szildenafil-kezelést az elégtelen klinikai válasz miatt. A vizsgálat négy éve alatt az eredeti 979 résztvevő közül csak 62 (6,3%) szüntette be az elégtelen válasz miatt (3. táblázat).
Vita
- Fogyjon el a merevedési zavarok elvesztése érdekében
- Hogyan kezelheti a fogyás a merevedési zavarokat - Northwoods urológiája
- Sok nőnek hosszú távú fogyása van; Hasplasztika,; Plasztikai és rekonstruktív jelentések
- Hypothalamicus diszfunkció MedlinePlus Medical Encyclopedia
- Zsírleszívás Hogyan működik, típusai, biztonsága, mellékhatásai és előnyei