Az étrendi fehérjebevitel befolyásolja az emberi vázizomfehérje frakcionált szintetikus arányait az állóképességi edzés után
Absztrakt
Eddig egyetlen tanulmány sem határozta meg, hogy a postexercise vázizomfehérje-szintézis modulálható-e a megnövekedett étkezési fehérje krónikus fogyasztására adott válaszként. Elméletileg a megnövekedett vagy magas fehérjebevitel kiterjesztheti a szabad aminosavkészletet, csökkentve a lebontáshoz való támaszkodást a vázizom fehérje szintéziséhez szükséges aminosavak ellátásához. Jelenleg a kulcsfontosságú kérdések nagyrészt feltáratlanok. Először is, növelheti-e a különböző mennyiségű étkezési fehérje krónikus fogyasztása a szabad aminosav-készletet edzés után? És ha igen, akkor az étkezési fehérje megnövekedett mennyiségének fogyasztása hatással lesz-e a vázizom fehérje szintézisére egy állóképességi edzés után? Jelen vizsgálat célja annak megállapítása volt, hogy az étkezési fehérje változó szintjének szokásos fogyasztása megváltoztatja-e a vázizom fehérje szintézisét az állóképességű sportolók akut aerob edzés után. Feltételeztük, hogy a megnövekedett étrendi fehérjebevitel kiterjeszti a szabad aminokészletet, ezáltal fokozva az FSR utómunkálatokat.
Résztvevők.
Miután a Connecticuti Egyetem Intézményi Felülvizsgálati Testülete jóváhagyta a projektet, öt 22–29 éves férfi állóképességi sportolót toboroztak az egyetemi közösségből és a helyi egészségügyi/futóklubokból, hogy részt vegyenek a vizsgálatban. Minden résztvevő teljes kórtörténetet, edzéstervet és feljegyzést készített az étrend beviteléről. Az alanyoknak legalább 56 km/hét futást kellett előírniuk a vizsgálatba való felvételhez. Azokat a személyeket, akik metabolikus vagy kardiovaszkuláris rendellenességekről, emésztőrendszeri rendellenességekről (azaz laktóz intoleranciáról), táplálék/sport kiegészítők vagy anabolikus szteroidok használatáról számoltak be, vagy akik vegánnak tartották magukat, kizárták a vizsgálatból. Tájékozott, írásos beleegyezést kaptak minden alanytól.
Kísérleti terv.
Ez a tanulmány egy crossover tervezés volt, és az önkéntesek saját kontrolljukként szolgáltak. A kezdeti kiindulási vizsgálati időszak után az önkénteseket véletlenszerűen olyan étrendre osztották be, amely testtömeg-kilogrammonként 0,8 g fehérjét (alacsony fehérjetartalmú; LP), 1,8 g fehérjét (mérsékelt fehérje; MP) vagy 3,6 g fehérjét (magas fehérjetartalmú; HP) tartalmaz. súlya (g · kg –1 · nap –1) 4 hétig. Minden étrend-beavatkozás 3 hét után 24 órás nitrogénegyensúlyt és szubsztrát-oxidációt értékeltünk. 4 hét elteltével az izomfehérje FSR-t meghatároztuk a poszt-edzés után. ∼2 hetes „kimosási” időszak után a sportolók átmentek és elfogyasztották a többi étrendet, és az összes mérést megismételték.
Előzetes mérések.
Az alapvizsgálat magában foglalta az aerob kapacitás (V̇ o 2 csúcs), az antropometria (magasság és súly), a testösszetétel (hidrosztatikus mérés), a nyugalmi energia ráfordítás (REE-közvetett kalorimetria), a 3 napos étrend-nyilvántartások és az edzésrekordok értékelését. A magasságot és a súlyt egy mérlegnyaláb-skálán (Health-o-meter, Bridgeview, IL) mértük 0,5, illetve 0,5 cm pontossággal. A testzsír százalékát hidrosztatikus méréssel becsültük meg, és az értékeket a test sűrűségéből számítottuk ki Brozek és mtsai (8) egyenletei alapján. A V̇ o 2 csúcsvizsgálatot a vizsgálat megkezdése előtt végeztük, és légzéssel határoztuk meg a lejárt gázok légzéselemzésével a tesztelés során, egy nyitott áramkörű légzőkészülékkel (MedGraphics CPX/D; Medical Graphics, St. Paul, MN) futópadon. (MedTrack ST55; Quinton, Bothell, WA), amely szellőző áramlásmérőt, oxigénelemzőt és szén-dioxid-analizátort tartalmaz (15). Később a résztvevőket arra kérték, hogy térjenek vissza a futópadra, hogy meghatározzák a terhelés teszteléséhez szükséges megfelelő terhelést a vizsgálat során. A sebességet úgy manipuláltuk, hogy kiszámított V̇o 2 csúcsuk ~ 70% -át kiváltsa.
Alapvető étrendi nyilvántartások.
Háromnapos étrendi nyilvántartásokat gyűjtöttünk a vizsgálat minden résztvevőjétől a kiindulási időszak alatt, hogy értékeljük a kalóriák, szénhidrátok, fehérjék és zsír kezdeti tápanyag-bevitelét. Az összes étrendi rekordot a Nutritionist Pro Software (First Data Bank, 1.1 verzió) segítségével elemezték.
Képzési naplók.
Minden sportoló naplót vezetett, amely részletezte napi és heti összesített számát a futásteljesítmény szempontjából. A résztvevők többsége távfutó volt az egyetemen, és versenyszezonjuk során bekerült a vizsgálatba, ezáltal biztosítva az etetési beavatkozások közötti konzisztens edzésmintákat. Ezeket a folyóiratokat minden étrendi beavatkozás végén összegyűjtöttük és elemeztük.
Nyugalmi anyagcsere.
A REE-t kiértékeltük a kiindulási értéknél, majd 3 hét eltelte után az egyes étrendeket. Az alapszintű REE-t arra használták, hogy pontosabban megjósolják a kalóriaigényt, és kiegészítő információkat szolgáltassanak a súlystabilitás és az energiaegyensúly biztosításához ezeknél a sportolóknál. Az étrendi beavatkozási fázisok során értékelt REE 3. hét segítségével meghatároztuk a diéták hatását a szubsztrát oxidációjára. Huszonnégy órás kiválasztott nitrogénértéket alkalmaztunk indirekt kalorimetriával együtt a szubsztrát oxidációjának becsléséhez.
A REE értékét közvetett kalorimetriával határoztuk meg egy metabolikus kocsi alkalmazásával (MedGraphics CPX/D; Medical Graphics). A teszt reggelén minden résztvevő autóval tért be a laboratóriumba a fizikai aktivitás minimalizálása érdekében. Az összes tesztet egy éjszakai böjt után végeztük, és a résztvevők legalább 10 órás postabszorptív állapotban voltak.
Diétás beavatkozások.
A fehérjebevitelt „alacsony”, „mérsékelt” vagy „magas” fehérjebeviteli szintre állítottuk be (0,8, 1,8 vagy 3,6 g · kg –1 · nap –1). A diétás beavatkozásokat úgy alakítottuk ki, hogy a makrotápanyagok által bevitt összes kalória százaléka megközelítőleg 60% szénhidrátot, 30% zsírt és 10% fehérjét jelentett az LP számára, 55% szénhidrátot, 30% zsírt és 15% fehérjét az MP számára, és 40 % szénhidrát, 30% zsír és 30% fehérje, a HP diétához. A diéták eukalorikusak voltak, izoenergetikus cserével a fehérje és a szénhidrát között. Minden étkezésnél a domináns fehérjeforrás a marhahús volt. Ezenkívül a HP diétán résztvevők napi két, kereskedelemben kapható fehérjeszeletet kaptak (Protein Plus; Met-Rx, Irvine, CA), amelyek ~ 300 kcal és 32 g fehérjét (15 g szénhidrát, 8 g zsír) biztosítottak a fehérje bevitelük növelésére. az előírt szintre. A menükbe bevonták az élelmiszercsere-listákat, hogy megfeleljenek az egyének számára meghatározott étrendi előírásoknak, és biztosítsák a testsúly fenntartását.
A résztvevőket a kijelölt ebédlőben etették a Connecticuti Egyetem Vendéglátás Tanszékén keresztül. A kutatási asszisztensek minden étkezésnél jelen voltak, hogy lemérjék és felszolgálják a megfelelő ételeket minden résztvevő számára. A résztvevõket önmagában nem korlátozták étellel, az étkezéshez elõírtnál több vagy kevesebbet fogyasztottak.
Izotópok.
Valamennyi stabil izotóp törzsoldatát a Connecticuti Egyetem Egészségügyi Központ Laboratóriumi Orvostudományi Tanszéke (Farmington, CT) steril és pirogénmentesnek készítette és igazolta. A vizsgált stabil izotópok mindegyike kereskedelemben kapható termék volt (Cambridge Isotope Laboratories, Cambridge, MA), amelyekgyűrű- 2H5] fenilalanin. Valamennyi izotópot feloldottuk 0,9% -os fiziológiás sóoldatban, és kalibrált fecskendőpumpával (Razel Scientific Instruments, Stamford, CT) infundáltuk. A [2H5] fenilalanin infúziós sebessége 0,05 μmol · kg -1 -1 perc -1 (az alapdózis 2,0 μmol/kg). Az izotópot 0,2 μm-es szűrőn átszűrjük infúzió előtt. Az infúziós protokollokat az egyensúlyi kinetika érdekében hajtották végre, mind a plazma, mind az izomkészletben.
Kísérleti protokoll.
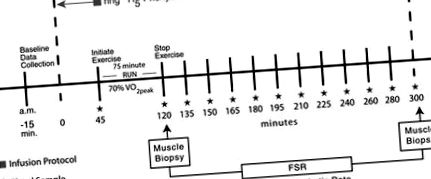
A résztvevők 24 órával a gyakorlat protokollja előtt nem gyakoroltak. Az alanyok a kereskedelemben kapható sportitalokat (Powerade, 45 g szénhidrát) fogyasztottak este minden edzésprotokoll előtt, a megfelelő glikogénkészlet biztosítása érdekében. A futók reggel 6 és 7 óra között jelentettek az Emberi Teljesítmény Laboratóriumban. posztabszorpciós állapotban. Intravénás katétert helyeztünk egy antecubitalis vénába a háttér vérminta és az azt követő infúzió előállítása céljából. A kiindulási vérminta összegyűjtése után megkezdtünk egy alapozott folyamatos infúziót (2 μmol/kg; 0,05 μmol · kg -1 -1 perc –1) [2 H5] fenilalanint (0 perc), és az egész testmozgási protokoll alatt tartottuk a FSR postexercise (1. ábra). Az alanyok 45 percig hevertek kórházi ágyon, ekkor kezdték meg a 75 perces futópad futását 70% V2 o 2 csúcson.
1. ábra.Az infúziós/biopsziás protokollt ábrázoló vázlat. A [2H5] fenilalanin háttérgazdagodás meghatározására szolgáló alapszintű vérvétel után megkezdtük az izotóp infúziót. Az alanyok a 75 perces futást 45 perccel kezdték. A biopsziákat 120 és 300 percnél vettük. Vérvétel a csillagok által jelzett rendes időpontokban történt.
A testmozgás után egy további katétert helyeztek egy kontralaterális kézi vénába az artériás vérvételhez, amely 15 perces időközönként történt. Intravénás sóoldatot tartunk fenn a vonal szabadalmaztatása érdekében. A résztvevő kezét fűtőbetéttel fedték le és ~ 70 ° C-ra hevítették, így artériás vérmintákat lehetett kapni. Korábbi kutatások megállapították, hogy az artériás vérminták szignifikánsan korrelálnak az artériás vérértékekkel (11). Ezt követően a résztvevőket steril körülmények között előkészítették egy izombiopsziára, amelyet a vastus lateralis oldalirányú részéből vettek (~ 20 cm-rel a térd felett). A biopsziázandó területet körülvevő bőrt és szubkután réteget 1% lidokainnal (Elkins-Sinn, Cherry Hill, NJ) lokálisan érzéstelenítettük. Valamennyi biopsziát Bergström 5 mm-es kanülökkel (Depuy Orthopedics, Varsó, IN) szívással készítettük. A szövetmintát azonnal szárazra foltoztuk, eltávolítottuk a látható zsír- vagy kötőszöveteket, és folyékony nitrogénben lefagyasztottuk. Ezután a mintákat további feldolgozásig -80 ° C-on tároltuk. A későbbi biopsziákat ugyanabból a lábból vettük, és az eljárások között enyhe nyomást alkalmaztunk.
Vér.
Az artériás kézi vénából a fenilalanin-dúsítás meghatározásához kapott vérmintákat azonnal kicsaptuk 15% szulfosaliciklus-savat tartalmazó csövekben, és alaposan összekevertük. A teljes vérmintákat centrifugában centrifugáltuk, és a felülúszót további vizsgálatokig -80 ° C-on lefagyasztottuk. A jelzett fenilalanin teljes vérben való dúsulásának meghatározásához a t-A fenilalanin butil-dimetil-szilil (BDMS) származékát Phillips és munkatársai által korábban alkalmazott módszerekkel állítottuk elő. (23) Elemzése t-A BDMS-fenilalanint gázkromatográfia-tömegspektrometriával (Hewlett-Packard 5890, II. Sorozat) elektron-ütés ionizációval és szelektált ion [tömeg/töltés arány (m/z)] ellenőrzése m/z 234, 235, 239 és 240, a m + 0, m + 1, m + 5. és m + 6 ion, ill. Megfelelő korrekciókat hajtottak végre minden olyan spektrum esetében, amely átfedésben volt és hozzájárult a nyomjelző-nyom arányhoz (34).
Izom.
A bemutatott adatok vegyes izomfehérje szintézist képviselnek, és ebben a vizsgálatban nem mértek specifikus izomfehérjéket. Az izomszövet mintáit fehérjéhez kötött és szabad intracelluláris dúsulás szempontjából elemeztük, a korábban leírtak szerint (23).
Számítások.
Az FSR-t a vázizomfehérjében lévő nyomjelző beépülési sebességéből és az izom intracelluláris szabad fenilalanin-dúsításának előfutáraként történő kiszámításával számítottuk a következő egyenlet szerint (lásd a 2. hivatkozást):
Táplálkozási elemzések-diétás beavatkozások.
Az étrendi rekordokat az energia- és makrotápanyagok összetételére elemeztük a Nutritionist Pro Software (First Data Bank, 1.1-es verzió) alkalmazásával. A tápanyagok bevitelét a napi 4 hét étkezési beavatkozás napi átlagaként jelentik.
Plazma aminosavak.
A plazma aminosavakat a kiinduláskor elemeztük (t = 0) 4 hét étrend után fenil-izotiocianáttal végzett származékképzéssel és HPLC-vel (14).
Statisztikai analízis.
Az önkénteseket közös leíró statisztikák írták le a magasság, a súly, az életkor, a testösszetétel és a V2 o 2 csúcsértékek mérésére. Ismételt intézkedések ANOVA-ját alkalmazták annak megállapítására, hogy különbségek vannak-e a különböző kritériumintézkedésekben a kiinduláskor, a postexercise-ben és a helyreállításban az LP, MP és HP között. Amikor jelentős különbségeket észleltek, Tukey post hoc elemzését végezték el. A szignifikancia szempontjából az α-szintet állítottuk be P
Asztal 1. Az alaptantárgy jellemzői
Az értékek átlag ± SE; n = 5 alany.
Diétás beavatkozások.
A 2. táblázat összefoglalja az LP, MP és HP étrendi fehérje beavatkozások átlagos tápanyag-bevitelét. A makrotápanyagok lebontása 48% szénhidrát, 26% zsír és 26% fehérje volt a HP esetében, 60% szénhidrát, 26% zsír és 14% fehérje MP esetében, 66% szénhidrát, 27% zsír és 7% fehérje volt az LP esetében. Az átlagos fehérjebevitel grammban/testtömeg-kilogrammonként 0,87, 1,78 és 3,12, a szénhidrátbevitel 8,3, 7,4 és 5,4 volt LP, MP és HP esetén,.
2. táblázat. Az LP, MP és HP tényleges étrendi bevitele
Az értékek átlag ± SE. LP, alacsony fehérjetartalmú étrend; MP, mérsékelt fehérjetartalmú étrend; HP, magas fehérjetartalmú étrend. P ‡ LP,
A szubsztrát oxidációja.
A szubsztrát oxidációs adatai tükrözik az alany étrendi megfelelőségét. A fehérje oxidációja az étkezési fehérje növekedésével nőtt, az étrendi beavatkozások jelentősen különböztek egymástól (54 ± 7 vs. 25 ± 2 vs. 14 ± 2% a HP, MP és LP esetében, P
3. táblázat. Plazma-aminosav-adatok a kiinduláskor (0 perc)
Az értékek átlag ± SE. Az egységek μM. NEAA, nem esszenciális aminosavak; EAA, esszenciális aminosavak; BCAA, elágazó láncú aminosavak.
* Statisztikailag eltér az LP-től, P
2. ábra.Vegyes izomtöredékes szintetikus sebesség (FSR) edzés után mindhárom étrenden. A magas fehérjetartalmú étrendben az FSR szignifikánsan alacsonyabb volt, mint a mérsékelt fehérjetartalmú (MP) és az alacsony fehérjetartalmú étrendben (*)P
3. ábra.Plazma (A) és izom (B) [2H5] fenilalanin dúsítási adatok mindhárom infúziós protokollhoz (HP, MP és LP).
Számos tanulmány vizsgálta a szokásos fehérjebevitel képességét az egész test fehérje-anyagcseréjének reagálására az állóképesség gyakorlására. Összességében nem találtak szignifikáns különbségeket az egész test szintézisének és az éhezés során bekövetkező lebontások között, amikor a fehérje bevitel 0,9–2,5 g · kg –1 · nap –1 –1 között mozgott, edzés előtt, alatt vagy után (7, 9, 13.) Az egyetlen következetes válasz a leucin oxidációjának növekedése nagyobb fehérjebevitel mellett (7, 13).
Ezen vizsgálatok eredményei alapján nem tűnik úgy, hogy az étrendi fehérjebevitel hatással lehet az egész test fehérjeszintézisének és bomlásának sebességére éhomi állapotban, akár az állóképességi edzés előtt, akár utána. Fontos azonban megjegyezni, hogy ezek a tanulmányok a fehérje hasznosításának egész testére vonatkozó értékelését használták, amelyek valószínűleg nem tükrözik a vázizom fehérje anyagcseréjét (1, 3, 10, 29). Valójában ez a tanulmány egyedülálló, mivel ez az első vizsgálat, amely azt dokumentálja, hogy a szokásos fehérjebevitel változásai hatással lehetnek a vázizomfehérje szintézisére az állóképességből való kilábalás során.
Összességében a tanulmány megállapításai alátámasztják azt a javaslatot, hogy a fehérjeszintézis sebessége részben a szabad aminosavak elérhetőségétől függ (20, 32). Az aminosavakat a szabad aminosavkészletből veszik fel, és felhasználják a fehérjeszintézis elősegítésére. Viszont aminosavakra van szükség ennek a készletnek a feltöltéséhez. Böjt állapotban ezek az aminosavak kizárólag az endogén fehérje lebontásával érhetők el. Ezért a fehérje lebontásának az edzés eredményeként bekövetkező növekedését szükség szerint fel lehet tekinteni, hogy biztosítsuk a szabad aminosavakat, amelyek a szintézis egyidejű növekedésének kiváltásához szükségesek. Az exogén aminosavak szokásos ellátása növelheti ezt a szabad aminosav-készletet, ezáltal lehetővé téve a szintézis folytatását a bomlás megfelelő növekedése nélkül.
Az a tény, hogy az FSR szignifikánsan alacsonyabb volt a HP diétánál, közvetlenül ellentétes eredeti hipotézisünkkel. Korábbi megállapítások alapján, amelyek szerint a rezisztenciát és az aerob edzést követõ akut fehérjetáplálkozás nagyobb mértékben stimulálta a fehérjeszintézist, mint az egyedül a testmozgással (4, 5, 20, 22, 24, 28, 30, 31), feltételeztük, hogy a szokásos A magasabb fehérje fogyasztása a szabad aminosavkészlet krónikus terjeszkedéséhez vezetne, ezáltal nagyobb szintetikus válasz utáni mozgás is lehetséges, még éheztetett állapotban is. Amikor az FSR adatait egyedül vizsgálják, ez nem így történt. További részletes vizsgálatok szükségesek az FBR megnövekedett táplálékfehérje szintjével a vázizom fehérje forgalmának teljes tisztázása érdekében ilyen körülmények között.
Összefoglalva, a jelen vizsgálat a postexercise vázizomfehérje-szintézis első átfogó elemzését nyújtja az étrendi fehérjebevitel különböző mértékű válaszaként. Az a tény, hogy a fehérjebevitel szokásos változása az éheztetett állapotban a vázizom fehérje szintézisének változásával járt, alátámasztja azt az elképzelést, hogy a fehérjebevitel közvetlen szerepet játszik a vázizom fehérje anyagcseréjének szabályozásában. Ezek a megállapítások megerősítik a hosszú távú, jól kontrollált étrendi beavatkozások végrehajtásának szükségességét, amelyek tükrözik a szokásos bevitelt, hogy tovább jellemezzék a fehérje bevitel, az állóképesség és a vázizom fehérje forgalma közötti kapcsolatokat.
Ezt a tanulmányt részben az Országos Marhahús Szövetség és a Connecticuti Egyetem Kutatási Alapítványa támogatta.
LÁBJEGYZETEK
A cikk megjelenésének költségeit részben az oldaldíjak megfizetése fedezte. A cikket ezért ezennel fel kell tüntetni:hirdetés”Szerint a 18 U.S.C. Az 1734. § kizárólag ennek a ténynek a feltüntetésére.
Mélyen köszönettel tartozunk a futóknak, akik olyan szívesen és lelkesen vettek részt ebben a tanulmányban. Nagyra értékeljük a segítséget, amelyet Brian Bennett, Alex Seen, Laura Hanley, Karen McNeil, Connie Cantor és az University Catering nyújt.
- Az étrendi fehérjebevitel hatása a szérum teljes CO2 koncentrációjára krónikus vesebetegségben
- A különféle étrendi energiafogyasztás hatása az ellenállóképzés után az izomtömegre és a testre
- Az étkezési fehérje korlátozás gátolja a tumor növekedését a prosztata és az emlő humán xenograft modelljeiben
- A halakban és hüvelyesekben gazdag étrend elősegítheti a természetes menopauza késleltetését
- Az étrendi zsírbevitel megváltoztató, oxidált kis sűrűségű lipoprotein és plazma szintjének változásai