Diéta, a bél mikrobioma és szívelégtelenség
Absztrakt
A mikroorganizmusok gyűjtését, amelyek együtt élnek a gazdatesten belül vagy a gazdatesten, mikrobiotának nevezik. Az embereknél az ilyen együttélés leginkább a bélben, főleg a vastagbélben tapasztalható. A bélmikrobiom a környezetből származik, és leginkább az étrend módosítja. Előzetes adatok igazolják, hogy a bél mikrobiája közvetlenül befolyásolhatja a szívelégtelenség (HF) kórokozó folyamatait. A HF a bélfal ödémájához és regionális hipoxiához vezet, ami a bél mikrobiális flórájának változását idézi elő, ami elindíthatja vagy fenntarthatja a HF bizonyos patogenetikai folyamatát. Maga a mikrobiota szerkezeti komponense, például lipopoliszacharidok vagy a baktériumok által termelt anyagok, például trimetil-amin-N-oxid szerepet játszik a HF patogenezisében. Ezt a folyamatot a szívbél tengelyének nevezik a HF-ben. A bél mikrobiájának kezelése vagy a mikrobából származó termékek megcélzása a jövőben a HF kezelési lehetőségeivé válhat.
- Minden betegség a bélben kezdődik.
- Hippokratész (Kr. E. 460–370)
Az elmúlt években sok kutató leírta a bél mikrobiota és számos betegség, köztük a szívbetegségek, a magas vérnyomás, a cukorbetegség és az elhízás kapcsolatát. [1,2] Az étrend az egyik fő tényező, amely befolyásolja a bél mikrobiota mintázatát. [3] ] Ez a cikk azt tárgyalja, hogy a bél mikrobiota hogyan befolyásolja a szívelégtelenséget.
Mi az emberi bél mikrobioma?
A gazdatesten belül vagy a gazdatesten együtt létező mikroorganizmusok gyűjteményét mikrobiotának nevezik. [1] Több mint 2000 kommensális organizmus (főleg baktérium) létezik, amelyek együtt élnek az emberi testtel, túlnyomó többségük a bélben. Egészséges felnőtt felnőtt embernek körülbelül 100 billió baktériuma van a bélben, főleg a vastagbélben. [1,4]
A bél mikrobioma a környezetből származik, nem genetikailag szerezhető be, és a bél általában steril az anyaméhben. Például a magzat a császármetszés és a hüvelyi szállítás során különböző mikrobiotára tesz szert. [5] Ezt követően a magzat étrendtől és a környezettől függően különböző típusú mikrobiómákat szerez. [6,7]
Az emberi bélmikrobiomában öt phyla dominál: Bacteroidetes, Firmicutes, Actinobacteria, Proteobacteria és Cerrucomicrobia. [1,8] A bél mikrobiota általában stabil az egyénen és a családon belül. Az egészséges bélben a Bacteroidetes és a Firmicutes anaerob csoportok az összes baktériumfaj több mint 90% -át teszik ki. [8]
Mi dönti el az egyén bélmikrobiómájának mintázatát?
A bél mikrobiota sajátos mintáit enterotípusoknak nevezzük. [9] A bél mikrobiomjának nem kívánt változását dysbiosisnak nevezik. [10] Az enterotípust befolyásoló egyik legfontosabb tényező az egyén hosszú távú étrendje. Például a magas állati fehérje- és zsírtartalmú étrend magas Bacteroides-szintet és alacsony Prevotella-szintet mutat (szintén a Bacteroidetes nemzetség része). [11] Éppen ellenkezőleg, a magas szénhidráttartalmú, alacsony állati fehérje- és zsírtartalmú étrendben alacsony a Bacteroides-szint és magas a Prevotella-szint. A diéta és a bél mikrobiális kölcsönhatásának másik példája megtalálható a japán embereknél. Belük tartalmaz Bacteroides plebeius-t, amely enzimet termel, amely elősegíti a tengeri moszatok emésztését. [12]
Az étrenden kívül a bél mikrobiális mintázatát befolyásoló egyéb tényezők a környezeti változások, a higiénia, az antibiotikumok használata és a betegség állapota. [1,6]
Hogyan befolyásolja a bél mikrobiota a gazdát
A bélmikrobiomnak számos funkciója van. [13] Egyik funkciója a kórokozók kiszorításával, a tápanyagok és receptorok versengésével, valamint az antimikrobiális faktorok termelésével járó védelmi funkció. [1] A bél mikrobiota néhány vitamint is kiválaszt.
A bélmikrobiom egyik legfontosabb funkciója az anyagcsere, mivel elősegíti az élelmiszer-összetevők emésztését. Például a bélbaktériumok részt vesznek a cukrok (pl. A glikánok, amelyek olyan komplex cukrok, amelyeket emberi enzimek nem hasíthatnak el) glikozid-hidroláz által történő lebontásában. A bél mikrobiota két fő katabolikus úton - szacharolitikus vagy proteolitikus - vesz részt az emberi emésztési folyamatban. [14] Mindkét út rövid láncú zsírsavak (SCFA) termeléséhez vezet. A második katabolikus útvonal olyan toxikus molekulákat is termel, mint ammónia, különféle aminok, tiolok, fenolok és indolok, amelyeket a vesék ürítenek, de fel fognak halmozódni, ha veseműködési zavarok vannak. [1,14,15]
Indokolt úgy tekinteni a mikrobiomra, mint egy körülbelül 2–2 kg súlyú „szervre”, jóllehet nincs külön szerkezete. A mikrobiom folyamatosan olyan vegyületeket állít elő, amelyek egy része felszívódik és biológiailag aktív. Így tekinthető endokrin szervnek, amely biológiailag aktív entitásokat termel, amelyek diffundálnak a véráramba és távoli helyeken hatnak. [1]
A bél mikrobiotáját egyetlen réteg bélhám választja el a lamina propriától. A bélhám számos mechanizmust alkalmaz a kommensális baktériumok korlátozására a bél lumenjére és annak megakadályozására, hogy ezek a mikrobiota kijussanak az alatta lévő szövetbe. [16] A bél mikrobiota pedig azért alakult ki, hogy elkerülje a gazda immunrendszerét és megkerülje az antimikrobiális gazdaszervezet válaszát. [16]
A bélsorompó mechanizmusnak kettős szerepe van - véd a mikroorganizmusok inváziója és a bakteriális toxinok felszívódása ellen, ugyanakkor lehetővé teszi az alapvető termékek, elektrolitok és tápanyagok felszívódását is. [17]
A bél mikrobiota sok olyan anyagot termel, amelyek képesek bejutni a véráramba, és ezt követően befolyásolják a patobiológiai folyamatokat. Ezen anyagok permeabilitása a nyálkahártya gát funkcionális és szerkezeti integritásától függ. A lehetséges gátló tényezők közé tartozik a bél hipoperfúziója, fertőzések, toxinok, gyógyszerek és egyéb életmódbeli tényezők. [17] Néha maga a mikrobiota szerkezeti eleme lehet, például lipopoliszacharidok (LPS) vagy peptidoglikánok, amelyek kölcsönhatásba lépnek a gazda nyálkahártya felszíni sejtjeivel mintázatfelismerő receptorokon keresztül. [1,18]
Ezenkívül a mikrobiális organizmusok által termelt molekulák is bejuthatnak, hogy különféle hatásokat okozzanak. Néhány azonosított útvonal magában foglalja a trimetilamin-N-oxid (TMAO) útvonalat, az SCFA útvonalat és az epesav útvonalat. [1] A TMAO prekurzora az l-karnitin vagy kolin, amely jelen van olyan élelmiszer-anyagokban, mint a vörös hús. Ha egy személynek magas a vörös húsbevitele, akkor a TMAO-termelés megnő, ami szerepet játszik a szívbetegségek patogenezisében. [2]
Hogyan tanulmányozzuk a bélmikrobiómát?
A bélmikrobiómát nem könnyű tanulmányozni, mert baktériumok millióit és fajok ezerjét tartalmazza. Gombák és vírusok is vannak jelen, amelyek nehézségeket okozhatnak, mivel genetikai anyaguk megzavarja a szóban forgó baktériumgenom azonosítását. A bélmikrobiális genom tanulmányozásának további kérdése, hogy a mikrobiális közösség a bél különböző régióiban megkülönböztethető, és azért is, mert a horizontális géntranszfer miatt a genom gyakran változik. [19]
A hagyományos módszer a kultúra, de unalmas és időigényes. A baktériumok genomi szekvenálása a következő legmegfelelőbb módszer. Az egyik népszerű módszer a 16S riboszomális RNS (rRNS) gén amplikon elemzése. A metagenómikus szekvenálás, egy másik, egyre népszerűbb módszer, általában drágább, de nagyobb felbontást kínál, lehetővé téve a specifikusabb taxonómiai és funkcionális osztályozást. [20] Wang és mtsai. ezt a következőképpen magyarázta: „A 16S rDNS-szekvencia megkísérli feltárni, hogy„ ki van ott? ”egy adott mikrobiális közösségben, míg a puskás metagenomikus szekvenálás segítségével megválaszolható a„ mit tehetnek? ”kiegészítő kérdés.” [21]
A bél mikrobiota és a szívbetegség társulása
A közelmúltban számos publikáció jelent meg a bél mikrobiota és a szívbetegségek, különösen a szívelégtelenség összefüggéséről. [22–26] A bél mikrobiota változásai az ateroszklerotikus érbetegségek rizikófaktorainak kialakulásához vezethetnek, és közvetlenül befolyásolhatják a patogenetikus betegség folyamatait, például akut koszorúér-szindrómák és szívelégtelenség. [27]
Az elhízás az egyik példa. Patológiája két domináns baktériumosztás, a Bacteroidetes és a Firmicutes relatív bőségének változásával jár. [28] Az elhízott betegeknél magas a Firmicutes szám. Megállapították azt is, hogy az elhízott mikrobiom megnövelt képessége az étrendből származó energia kinyerésére, és hogy az elhízott „tulajdonság” átvihető: a csíra nélküli egerek elhízott mikrobiotával való megtelepedése az összes testzsír jelentősen nagyobb növekedését eredményezi. mint gyarmatosítás sovány mikrobiotával, azonos étrenddel. [29]
Ezen túlmenően a magas vérnyomás és a cukorbetegség összefüggéseket mutat a bél specifikus mikrobiális mintázataival, és a kutatók bizonyos összefüggéseket fedeztek fel e betegségek patogenezisében és a bakteriális kölcsönhatásokban. [22,30,31]
Egy olyan vizsgálatban, amelyben összehasonlították a szívkoszorúér-betegségben (CHD) szenvedőket és azokat, akik nem szenvedtek, kiderült, hogy a CHD-s betegeknél a Bacteroidetes törzs részaránya alacsonyabb volt, a Firmicutes aránya magasabb. [32] Megállapították, hogy a megnövekedett TMAO-szint az incidens súlyos kardiovaszkuláris események (MACE) megnövekedett kockázatával jár együtt egy 4007 betegből álló kohorszban, akiket 3 éven keresztül követtek koszorúér-angiográfián. [33] Egy másik vizsgálatban egy 530 klevelandi klinikai kohorsz, amely mellkasi fájdalommal jelentkezett az sürgősségi osztályon, a bemutatáskor megemelkedett plazma TMAO-szintet mutatott, amely függetlenül társult a MACE-k kockázatához. [34] A Bacteroidetes: Firmicutes arány ismert, hogy minden krónikus betegségben megváltozik, ezért nem biztos, hogy megbízható azonosítója egy adott betegségnek.
Az emelt TMAO-szintek szerepet játszanak az endotheliális és simaizomsejtek aktiválásában, a habsejtek képződésében, valamint a szívizom- és vesefibrózisban. [2] Egy nemrégiben végzett szisztematikus áttekintésben és metaanalízisben (16 publikáció, 19 256 beteg) a TMAO és prekurzorainak megemelkedett koncentrációja a MACE-k megnövekedett kockázatával és minden okból eredő mortalitással társult, függetlenül a hagyományos kockázati tényezőktől. [35] A 26 167 beteg másik metaanalízise és szisztematikus áttekintése szintén pozitív dózisfüggő összefüggést mutatott ki a TMAO plazmaszintje, valamint a megnövekedett kardiovaszkuláris kockázat és mortalitás között. [36]
A mikrobióta társulása szívelégtelenséggel
A bél mikrobiota a szívelégtelenség (HF) patogenezisében is szerepet játszik. HF-ben a csökkent ejekciós frakció miatt csökken a bél véráramlása és alacsony az oxigénszállítás. Ez hajlamosítja a bélt az anaerob baktériumok kórokozó típusainak növekedésére. [37] Krónikus HF-ben szenvedő betegeknél a bélfal ödémája is kialakul a vénás torlódások miatt, amely akadályozza a bél abszorpciós funkcióját, és lehetővé teszi a baktériumok elszaporodását a vastagbél nyálkahártyájának csúcsfelülete mellett szomszédos nyálka rétegben. [36] HF-ben szenvedő betegeknél szintén beszámoltak a cukor cellobióz teszt segítségével megnövekedett béláteresztésről, és ez a megnövekedett permeabilitás korrelál a jobb pitvari nyomással és a C-reaktív fehérje szintjével. [38,39]
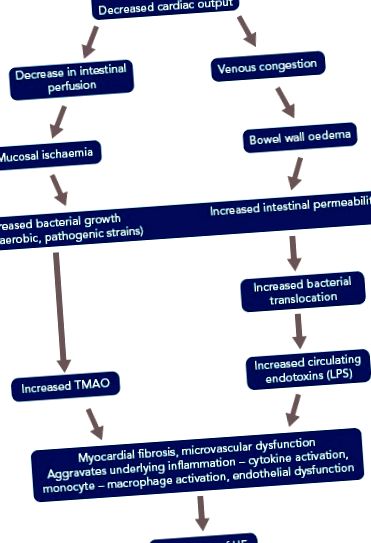
Ezek a baktériumok sok káros anyagot termelnek, beleértve a TMAO-t és az endotoxint (LPS), ami hajlamosítja vagy súlyosbítja a HF-t. Ezek a felfedezések a HF szív-bél tengelyének hipotéziséhez vezettek (1. ábra). [40,41] Magasabb LPS-koncentrációt találtak a dekompenzált HF-ben szenvedő betegeknél, ami korrelál a bélfal ödéma megnövekedett szintjével, amint arról korábban. Az LPS az „újrakompenzáció” után csökken. Sandek és munkatársai szerint ez ok-okozati összefüggésre utal az oedemás bélfal, a hám diszfunkciója és az LPS transzlokációja között. [42]
HF = szívelégtelenség; LPS = lipopoliszacharidok; TMAO = trimetil-amin-N-oxid.
Magas TMAO-szintet találnak HF-ben szenvedő betegeknél, amelyek magasabb hosszú távú halálozást jósolnak, még a hagyományos kockázati tényezők és a kardiorenális indexek kiigazítása után is. [41] Megállapították, hogy a TMAO prognosztikai tényező a HF-ben szenvedő betegeknél, és a magasabb szintek rossz prognózist jósolnak 1 éves követéskor. A TMAO és a hagyományos marker N-terminális pro-agy natriuretikus peptid kombinációja további prognosztikai információkkal szolgálhat. [43]
Miért nő a TMAO szint ilyen mértékben a HF-ben? Úgy tűnik, hogy a baktériumok összetételében bekövetkezett változások a TMAO-szintek elsődleges mozgatórugói. [25] A vesekárosodás és a változó étrendi szokások is hozzájárulhatnak. [25] Hogy a TMAO hogyan befolyásolja a HF patobiológiáját, nem világos. A javasolt elméletek magukban foglalják a citokinek, például a tumor nekrózis-alfa stimulálását, amely súlyosbíthatja a szívizom fibrózisát, a szív mikrovaszkuláris diszfunkcióját, függetlenül annak proateroszklerotikus hatásaitól, neurohormonális rendellenességektől és így tovább, de még nincs egyértelmű válaszunk. [25 ]
Kezelhetjük-e a bélmikrobiómát a betegségek kezelésére?
Van néhány tanulmány a bél mikrobiomjának manipulálásáról, amelyek reményt adnak a kapcsolódó betegségek kezelésében. A manipuláció sokféleképpen érhető el. Módosíthatjuk az étrendet a mikrobiota típusának megváltoztatására, megcélozhatjuk a bél mikrobiota által termelt vegyszereket, vagy közvetlenül megváltoztathatjuk a mikrobiális flórát probiotikumok hozzáadásával.
Ha csökkentjük a vörös hús étrendjét, akkor csökkentjük a kolin és a lecitin bevitelét, ezáltal csökkentjük a TMAO-t, ami pozitív hatással van a szívbetegségek kockázatára. Például a mediterrán étrendre váltás kimutatta, hogy csökkenti a HF markereit. Egy másik módszer nem felszívódó antibiotikumok beadása, amelyek megölik a specifikus mikrobiotát, és ezáltal megváltoztatják a mikrobiális mintázatot.
A probiotikumok egy másik módszer, amely megváltoztathatja a bél mikrobiális mintázatát. A probiotikumok élő hasznos baktériumok (Bifidobacteriumok, Lactobacillusok, Streptococcusok és nem patogén Escherichia coli törzsek), amelyeket a megfelelő bélmikrobiális egyensúly megteremtése érdekében be lehet fogyasztani. Vannak olyan vizsgálatok, amelyek Saccharomyces boulardii-t használtak HF-ben, amelyek előnyöket mutattak. A probiotikumok pozitív hatásai azonban csak a mikrobiális fajok korlátozott csoportjára vonatkoznak, és potenciális veszélyek is fennállnak, beleértve a lehetőséget arra, hogy ezeket a mikrobiotákat opportunista kórokozókká változtassák immunhiányos egyéneknél. [44]
A folyamatban lévő Gut-Heart vizsgálatban 150 olyan beteget randomizáltak, akiknek stabil HF és bal kamrai ejekciós frakciója volt Tang WH, Kitai T, Hazen SL. A bél mikrobiája a szív- és érrendszeri egészségben és betegségekben. Circ Res. 2017; 120: 1183–96. doi: 10.1161/CIRCRESAHA.117.309715. [PMC ingyenes cikk] [PubMed] [CrossRef] [Google Tudós]
- Az étrend és a táplálkozás befolyásolja a vastagbél nyálkahártyájának mikrobiomját; News-Medical
- Diéta és az iszkémiás szívbetegségek megelőzése transzlációs megközelítés - teljes szöveg nézet
- Elizabeth Taylor 80-as évekbeli diétája nem a gyengék számára készült
- Igyál a szívedhez A 10 legjobb ital a szíved egészségének megőrzéséhez - Fogyókúra - Szívbetegség
- Napi két vagy több diétás üdítőital fogyasztása növeli a szívroham-vizsgálat kockázatát