Karnitin-palmitoil-transzferáz II-hiány
Társított adatok
Absztrakt
Háttér:
A karnitin-palmitoil-transzferáz II (CPT II) hiánya fontos oka a visszatérő rabdomiolízisnek gyermekeknél és felnőtteknél. A jelenlegi kezelés magában foglalja az étrendi zsírkorlátozást, fokozott szénhidrátfogyasztással és testmozgás korlátozással az izomfájdalom és a rabdomiolysis elkerülése érdekében.
Mód:
CPT II enzimvizsgálat, DNS-mutáció elemzés, a vérben és a tenyésztett fibroblasztokban, vizeletben található szerves savakban található acilkarnitinek kvantitatív elemzése, a standardizált 36 tételes rövid formájú egészségügyi állapotfelmérés (SF-36) 2. verziója és a testzsír-összetétel bioelektromos impedanciája. Az összes beteg számára a teljes napi kalóriabevitel 30-35% -át kitevő triheptanoin diétás kezelést alkalmaztak.
Eredmények:
Hét CPT II-hiányos beteget vizsgáltak 7-61 hónapig a triheptanoin (anaplerotikus) diétán. Ötnek volt korábbi rabdomiolízis epizódja, amely kórházi kezelést és izomfájdalmat igényelt az étrend előtt (két fiatalabb betegnél nem volt rhabdomyolysis). A diéta alatt csak két betegnél tapasztaltak enyhe izomfájdalmat mozgás közben. Rövid nem megfelelő időszakokban két betegnél rabdomiolízis lépett fel a testmozgással. Senki sem tapasztalt rabdomiolízist vagy kórházi kezelést diéta közben. Minden beteg visszatért a szokásos fizikai tevékenységekhez, beleértve a megerőltető sportot is. A mozgáskorlátozás megszűnt. A korábban rendellenes SF-36 fizikai összetett pontszámok normalizálódtak, amely a terápia időtartama alatt mind az öt tüneti betegnél fennmaradt.
Következtetések:
A triheptanoin-diéta hatékony terápiának tűnik a felnőttkori karnitin-palmitoil-transzferáz-II hiány esetén.
SZÓJEGYZÉK
MÓD
Diagnosztikai módszerek.
CPT II enzim vizsgálatot, 4 in vitro palmitát oxidációt, 5,6 DNS elemzést, 7,8 acilkarnitin elemzést, 3 plazma zsírsav metabolitot (keton testet), 9 és fehérje mérést 10 végeztek diagnosztikai és monitorozási célokra. Minden egyes betegnél elvégeztük a 36 tételes rövid formájú egészségügyi állapotfelmérés (SF-36) 2. verzióját, 11 bioelektromos impedancia mérést, valamint soros vér- és vizeletkémiai méréseket (további részletekért lásd az e-Methods című részt a Neurology® webhelyen www.neurology.org címen).
Betegleírások.
Hét CPT II-hiányos beteget vontak be ebbe a vizsgálatba, 10 és 55 év közötti életkorban. Közülük három (3., 4. és 5. beteg) testvér volt. Mások között volt egy 55 éves nő (1. beteg), egy 54 éves férfi (2. beteg), egy 30 éves férfi (6. beteg) és egy 14 éves fiú (7. beteg). . Az enzimvizsgálatok és a DNS-elemzések rövid klinikai összefoglalói, eredményei kiegészítő anyagként állnak rendelkezésre (lásd: e-betegek).
Klinikai protokoll.
Ez a tanulmány a CPT II hiányának igazolását igényelte mutációanalízissel vagy izom-, fibroblasztok vagy friss limfociták biopsziáiból származó enzimvizsgálatokkal, mielőtt a betegeket felvehették volna. Valamennyi beteg aláírta a Baylor Egyetem Orvosi Központjának Intézményi Felülvizsgálati Testületének 099-135. Számú protokollja alapján a bejelentett beleegyezést. 59,303.
Kezdetben a betegeket 5 napig értékelték, amikor kiindulási klinikai és laboratóriumi adatokat kaptak. A triheptanoin-étrendet a második nap kezdte az igény szerinti dózismódosítással és a rendellenesség kezelésével kapcsolatos napi oktató foglalkozásokkal. Ezután a betegeket kb. 2., 6., 12. és 18. hónapban ismételt klinikai és laboratóriumi vizsgálatok követték. 18 hónap elteltével választhattak, hogy visszatérnek a hagyományos terápiához, vagy korlátlanul folytatják a triheptanoin diétát. Ezek a betegek úgy döntöttek, hogy meghosszabbítják részvételüket, amely jelenleg 40 hónaptól 61 hónapig terjed, további biztonsági és hatékonysági információkkal szolgálva a triheptanoin étrendről.
A táplálkozási szükségletek az összes beteg számára ajánlott napi adag irányelveken alapultak. Az étrend átlagos napi százalékos összetétele a protokoll alatt a következő volt: fehérje 13,1%, szénhidrát 37,2% és zsír 20%. A triheptanoin (8,3 kcal/g) a 30% -ot képviselte. Felnőttek és serdülők esetében a napi adag 1-2 g/testtömeg-kg volt. 12 évesnél fiatalabb gyermekeknél a triheptanoin napi adagja általában 3-4 g/kg volt, nagyobb napi kalóriaigényük miatt. Minden beteg négy egyenlő adagban (három fő étkezés és lefekvés előtt) fogyasztotta ezt a napi olajmennyiséget. A triheptanoint keverték az előnyben részesített ételekben, például joghurtban, pudingban vagy italokban. Minden betegnek azt tanácsolta, hogy korlátozza az egyszerű cukrok fogyasztását a túlzott súlygyarapodás megakadályozása és a triheptanoin oxidációjának optimalizálása érdekében. Továbbá azt tanácsolták nekik, hogy 20-30 perc alatt lassan fogyasszák az olajat, hogy elkerüljék a gyomorpanaszokat.
EREDMÉNYEK
Diagnosztikai tesztelés.
A diagnózis megszerzése rendkívül késleltetett (évtizedek). A szérum kreatin-foszfokináz (CPK) szintje és a vér acilkarnitin analízise csak rendellenes volt a rhabdomyolysis epizódjai alatt. Csak a 4. enzimvizsgálat és a 6. in vitro fibroblaszt-analízis volt következetesen megbízható a diagnózis szempontjából (lásd e-betegek és e-módszerek).
Diétás triheptanoinra adott válasz.
A triheptanoint négy egyenlő adagban adták be (a három fő étkezés és lefekvés előtt) a triheptanoin gyors metabolizmusa miatt (3-4 óra), ha enterálisan adták be. 3 Az 1. táblázatból megemelkedett propionilkarnitin vérszintje összefoglalja a rhdomyolysis és az izomfájdalom kórházi kezelését a triheptanoin diéta alatt és után. A 4. beteg kivételével mindannyian kórházba kerültek, és a triheptanoin diéta megkezdése előtt az izomfájdalmak elégségesek voltak a testmozgás korlátozására. Az étrend korábbi kezelése alacsony zsírtartalmú volt, és minden betegnél megnőtt a szénhidrát. A 14 évesnél fiatalabbaknál további MCT olaj-kiegészítés volt, amely a napi kalóriabevitel 6% -tól 10% -áig terjedt.
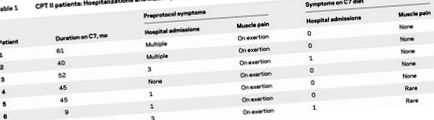
Asztal 1 CPT II betegek: kórházi kezelések és izomfájdalom a triheptanoin diéta előtt és után
A triheptanoin-diéta megkezdése után a legtöbb beteg az első hét végére némi javulást tapasztalott a napi tevékenységekben. 1-2 hónapon belül még erőteljesebb javulások történtek a testtűrés terén. Azoknál a betegeknél, akik betartották a triheptanoin étrendet, egyiket sem rabdomiolízissel kórházba hozták, és csak ketten tapasztaltak enyhe izomfájdalmat testmozgással. Mind a hét beteg versenyezhetett a csapatsportokban (röplabda, kosárlabda, torna, úszás és tae kwon do). Az idősebb betegek (1., 2. és 6. sz.) Úszásban, aerobikban, síelésben és túrázásban vettek részt. Ezek a tevékenységek a korábbi étrendkezelés során nem voltak lehetségesek. Következésképpen a testmozgás korlátozása már nem volt szükséges. Az izomfájdalom megelőzése érdekében egy triheptanoin adagot ajánlott bevenni 30 perccel a megerőltető fizikai aktivitás előtt.
Két beteg (3. és 7. sz.) Azonban 1-2 hétig abbahagyta az olaj szedését. Mindkettő megerőltető testmozgás után kórházi kezelést igényelt. Mindegyik megújult testtűréssel tért vissza a triheptanoin diétához.
SF-36 kérdőívek.
Ezeket a kiinduláskor és az azt követő látogatások alkalmával adták be. A 2. táblázat a rendelkezésre álló szekvenciális fizikai összetett pontszámokat (PCS) mutatja minden egyes betegnél a kiinduláskor és a diéta kezdete után 33 hónapig. A PCS pontszámok a két viszonylag tünetmentes betegnél, nos. A 4. és 5. ábra normál értéket mutatott a kiindulási értéknél, és normális maradt 28 hónapos kezelés után. Idősebb testvérük, a 3. beteg normális PCS pontszámot ért el 6 hónappal. Mindhárom fájdalommentes maradt 45 hónap (4. és 5. beteg) és 52 hónap (3. beteg) után az étrenden. A másik négy betegnél a PCS-pontszám szignifikánsan javult a kiindulási értéktől kezdve a +1 SD-től (7. beteg) egészen a +3 SD-ig (2. beteg), megközelítve vagy meghaladva az 50-es normál pontszámot (2. táblázat).
2. táblázat Kezdeti és ezt követő SF-36 (PCS) pontszámok
Biztonsági ellenőrzés.
Úgy tűnt, hogy a triheptanoin-diéta nem bizonyítja a toxicitást. A széria laboratóriumi eredmények egyikében sem voltak következetes rendellenességek, kivéve a CPK variációit, amelyek az aszpartát-aminotranszferáz (AST) és az alanin-aminotranszferáz (ALT) enyhe emelkedésével jártak, amikor a betegek enyhe kényelmetlenséget tapasztaltak.
A lipidprofilok általában nem voltak figyelemre méltók, kivéve az 1. és 2. betegeket (mindkettő 50 évnél idősebbek), akiknek a kiindulási állapotban és a C7 diéta során kóros profilja volt. Az 1. beteg esetében a koleszterinszint szakaszosan emelkedett, és a trigliceridek kezdetben emelkedtek, majd később normalizálódtak. Az alacsony sűrűségű lipoprotein (LDL) koleszterin a kiindulási értéknél normális volt, de utána rendellenes. A 2. páciens az étrend során hiperkoleszterinémiás volt, és az LDL tartósan emelkedett volt. A triheptanoin szedése során a többi beteg egyikében sem volt lipid-rendellenesség.
A kiindulási és a triheptanoin-diéta alatti vérkémia normális volt a glükóz, kálium, szén-dioxid, anionrés, kreatinin és albumin szempontjából. A vér karbamid-nitrogénje (BUN) enyhén, szakaszosan emelkedett a 2., 3. és 5. betegeknél. Szintjük csak 18–23 mg/dl volt, összehasonlítva a 7–17 mg/dl referenciatartománysal. A kreatinin szintje soha nem emelkedett ezen kisebb BUN-rendellenességekkel összefüggésben. Az AST és az ALT szint alapvetően normális volt a diéta alatt. Ahogy az várható volt, az AST csak enyhén emelkedett a megnövekedett CPK-szinttel együtt. A CPK számos „szubklinikai” emelkedést mutatott (nem észlelt kellemetlenséget az izmokban). Csak egy betegnél (5. sz.) Volt kóros szint minden látogatás alkalmával, 166 és 537 NE/l között (referencia tartomány 30–135 NE/L). Az összes CPK-érték teljes tartománya ezeknél a betegeknél a diéta ideje alatt 35–869 NE/l volt.
A vizsgálat során egyik betegnek sem volt hematológiai rendellenessége.
A vér palmitoil-karnitin szintje ritkán volt kóros, és az oleoil-karnitin szintje csak néha emelkedett enyhén, de nem volt diagnosztikus a CPT II hiány szempontjából. A vizeletből származó szerves sav mennyiségi kiválasztási profiljai nem mutattak tartós rendellenességeket (a részleteket lásd az e-1 táblázatban).
VITA
A gyermekkori vagy felnőttkori CPT II hiányos formában szenvedő betegeknél a rabdomiolízishez kapcsolódó súlyos izomfájdalom ismétlődő epizódokat tapasztalt, a szérum CPK és a mioglobinuria rendkívüli mértékben megemelkedve. Ezeket az epizódokat gyakran koplalás, fertőzés vagy túlzott testmozgás váltja ki. Amint arról ebben és más tanulmányokban is beszámoltunk, 1 a diagnózist nehéz lehet megállapítani, gyakran évtizedekig. Az izombiopsziákból, a fibroblaszt tenyészetekből és a limfocitákból származó CPT II aktivitás enzimvizsgálata egységesen végleges. A „közös” DNS-mutáció, az S113L elemzése nem mindig volt megbízható, és az acil-karnitin-elemzés vagy a szérum CPK sem volt megfelelő, amint azt a pácienseink eredményei mutatják, kivéve a rhabdomyolysis epizódjait. A maradék CPT II aktivitás felelős lehet e rendellenesség korai felismerésének nehézségéért.
A terápia az étrendi zsírbevitel csökkentésére összpontosított, miközben növelte a szénhidrátot, elsősorban a hosszú láncú acil – koenzim A (CoA) és az acilkarnitin-intermedierek rendellenes felhalmozódásának csökkentése érdekében. Rabdomiolitikus krízis során a mioglobinuriával társuló túlzott lipolízis az elsődleges probléma. Az akut terápia magában foglalja a glükóz infúziót (gyakran inzulin csepegtetéssel) a lipid mobilizáció, valamint a nagy mennyiségű folyadék és lúgosítás csökkentése érdekében, hogy fokozza a myoglobin vese kiválasztását. A zsír étrendi korlátozása, még a közepes láncú egyenletes szén-dioxid-trigliceridek (MCT-olaj) helyettesítésével is, jóllehet megalapozott indok, nem sikerült, mert a testmozgás korlátozása szükséges, az izomfájdalom továbbra is fennáll, és ismétlődő kórházi kezelések fordulnak elő.
Ábra A triheptanoinból származó heptanoát metabolikus sorsa
A máj és az izom kölcsönhatása katalitikus köztitermékek előállítására a citromsav-ciklushoz (CAC). ATP = adenozin-trifoszfát; BHP = β-hidroxi-pentanoát; BKP = β-ketopentanoát; BKP-CoA = β-ketopentanoil-koenzim A; CoA = A koenzim.
A CPT II-hiányban szenvedő gyermekek és felnőttek napról napra pontosan tudják fizikai korlátaikat, amit izomgyengeség, fájdalom és fájdalom periódusai bizonyítanak, enyhe vagy közepes testmozgással vagy betegségekkel kapcsolatban.
A két viszonylag tünetmentes gyermek kivételével (4. és 5. beteg) ebben a vizsgálatban minden beteg már a terápia negyedik napján tudatában volt a fokozott fizikai állóképességnek izomfáradtság vagy fájdalom nélkül. A diétaterápia kezdete és betartása óta egyikük sem igényelt kórházi kezelést rabdomiolitikus epizódok miatt. Minden beteg visszatért a korlátlan testmozgáshoz. Ezek a tevékenységek magukban foglalták a kosárlabdát, a röplabdát, a síelést, az aerobikot és az olimpiai típusú napi úszási protokollokat. A kiindulási értékeléseikkel összehasonlítva, az SF-36 kérdőív PCS-je ezen öt tüneti beteg esetében már 2 hónap alatt normális szintre javult, és az étrenden 33 hónapig normális maradt (2. táblázat).
Ez a tanulmány a CPT II hiány sikeres kezeléséről számol be anaplerotikus diéta terápia segítségével triheptanoinnal, ellentétben a betegek alacsony zsírtartalmú/magas szénhidráttartalmú étrenddel kapcsolatos korábbi tapasztalataival. Ezenfelül egyik betegben sem volt bizonyíték a toxicitásra, a túlzott súlygyarapodásra vagy a testzsír kóros összetételére, amely 61 hónapig terjedt. Ezen betegek egyike sem szenvedett visszatérő rabdomiolízis epizódokat, vagy diéta közben kórházi kezelést igényelt. A testmozgás korlátozása megszűnt, és az SF-36 pontszámok azt jelezték, hogy a testfájdalom nélkül visszatérnek a normális életmódhoz.
ELISMERÉS
A szerzők köszönetet mondanak a SASOL, GmbH-nak (Witten, Németország) az ebben a vizsgálatban használt triheptanoinolaj adományozásáért és J. Bezansonnak az SF-36 elemzéshez nyújtott segítségért. A szerzők köszönetet mondanak a Baylor Egyetemi Orvosi Központ Gyermekek Házának munkatársainak is a vizsgálatokhoz nyújtott segítségükért.
Kiegészítő anyag
Megjegyzések
Levelezési és újranyomtatási kérelmek Dr. Charles R. Roe-hoz, a Baylor Egyetem Orvosi Központ Metabolikus Betegség Intézetéhez, 3812 Elm St., Dallas, TX 75226 ude.htlaehrolyab@rselrahc
A Baylor Egyetemi Orvosi Központ Kutatási Alapítványának támogatásai és az NIH DK069752 (H.B.) támogatása.
Közzététel: A szerzők nem közöltek közzétételt.
2007. november 2-án kapott. Végleges formában 2008. április 10-én fogadta el.
- Alfa-1 antitripszin hiány
- 5 étel a magnéziumhiány elkerülésére
- Vérszegénység a D-vitaminhiányban, az OMICS International
- Antitrombin hiány - NORD (Nemzeti Ritka Rendellenességek Szervezete)
- 21-hidroxiláz-hiány miatt veleszületett mellékvese-hiperpláziában szenvedő felnőtt megközelítése