Refsumi betegség - az intesztinális lipáz-gátló, az Orlistat alkalmazása komplex rendellenesség újszerű terápiás megközelítéseként
1 Klinikai Biokémiai Osztály, Royal Prince Alfred Hospital, Sydney, Camperdown, NSW 2050, Ausztrália
2 Orvostudományi Tanszék, Sydney Egyetem, NSW 2006, Ausztrália
3 Biokémiai Tanszék, John Hunter Kórház, Newcastle, NSW 2305, Ausztrália
4 Lysosomális, peroxiszomális és kapcsolódó genetikai rendellenességek nemzeti referáló laboratóriuma, SA patológia a Női és Gyermekkórházban, North Adelaide, SA 5006, Ausztrália
5 Molekuláris és Orvostudományi Egyetem, Adelaide Egyetem, Adelaide, SA 5005, Ausztrália
Absztrakt
A Refsum-kór örökletes anyagcserezavar, amelyben az elágazó láncú zsírsavak metabolitja a megfelelő oxidatív enzimek hiánya miatt felhalmozódik. A betegeknél a plazma fitánsavszintje és a fitánsav koncentrációja különféle szövetekben progresszív szövetkárosodáshoz vezet. A retina degenerációja vagy a retina dystrophiája, amely a felnőttkori retinitis pigmentosa kialakulásához kapcsolódik, további tünetek közé tartozik a krónikus polyneuropathia, a cerebelláris ataxia, a sensorineuralis halláskárosodás, az anosmia, az ichthyosis, valamint a csontváz, a szív, a máj és a vese rendellenességei. A jelenlegi irányítás magában foglalja az elágazó láncú zsírsavak étrendi forrásainak elkerülését és a rendszeres plazmaferezist annak érdekében, hogy megakadályozzák ezen vegyületek felhalmozódását a progresszív neurológiai hiány enyhítésére. Két Refsum-kórban szenvedő testvért, akik az optimális étrend és a plazmaferezis ellenére progresszív tüneteket tapasztaltak, új terápiával kezdték. Beszámolunk a bél lipáz inhibitor, az Orlistat hatásáról, amely jelentős csökkenéshez vezetett (
2 mintán párosítatlan t-teszt) az átlagos preplazmaferezis fitánsavszintek a legtöbb dermatológiai és neurológiai tünet progressziójának késleltetésével.
1. Bemutatkozás
A Refsum-kórt, más néven heredopathia atactica polyneuritiformis (HAP) nevet Sigvald Refsum norvég neurológus írta le 1946-ban. Ez egy ritka komplex rendellenesség, amely sok szervet érint. Autoszomális recesszív öröklődési mintázata van a 10p13 kromoszóma mutációi miatt. A hordozókat ez nem befolyásolja, azonban tünetmentesen enyhén megemelkedett fitánsavszintet mutathatnak, míg a Refsum-kórban szenvedő betegeknél szignifikánsan magasabb (normál
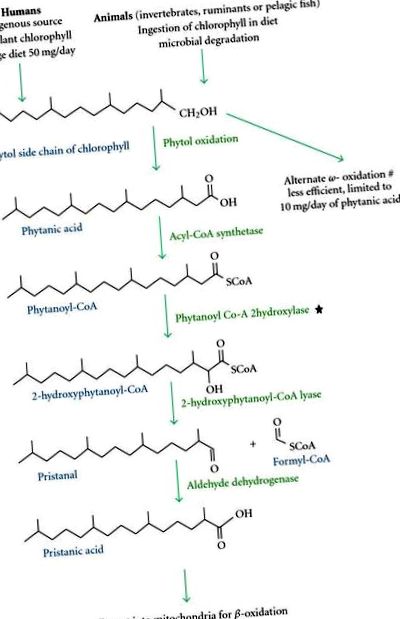
-oxidációs út a phytanoil-CoA hidroxiláz (PAHX) peroxiszóma enzim hiánya miatt [2–5] (1. ábra). Alapvető fontosságú, hogy a BCFA-helyzetében levő 3-metilcsoportot egy
-oxidációs lépés, amelyet PAHX aktivál (az endoplazmatikus retikulumon belül) az -oxidációs útvonal folytatása érdekében. A fitánsav metabolizmusának leghatékonyabb mechanizmusa a peroxiszomális -oxidáció. Ennek eredményeként a fitánsav magas szintje felhalmozódik a vérben és más szövetekben, különösen a zsírszövetben, az idegszövetben és az asztrocitákban, ahol a mitokondriumokban oxidatív stresszt és krónikus expozíció során oxidatív károsodást okoznak [3, 6, 7]. A betegek egy részében a PEX7-peroxin 7 receptor fehérjét kódoló második gén mutációját, amely szerepet játszik a fehérjék peroxiszomális importjában, a Refsum-kór fenotípusának okaként azonosították [2, 5].
-oxidációs utak a peroxiszómákban és a mitokondriumokban. ⋆ Refsum-betegségben szenvedő betegeknél az enzimhiányt jelenti. # a kevésbé hatékony alternatívát jelöli
Az embereknek másodlagos, kevésbé hatékony útjuk van a fitánsav-oxidáció útján történő metabolizmusához, amelyet ezek a betegek nem érintenek [2, 5] (1. ábra). Az -oxidáció képessége azonban korlátozott, és csak az étrendi korlátozással járó csökkentett fitánsav-ellátás feldolgozására elegendő. Állatkísérletekben beszámoltak arról, hogy a fibrátos gyógyszerek kiválthatják a fitánsav-anyagcsere ezen oxidációs útját [2].
1.1. Jelenlegi menedzsment
A Refsum-kórban szenvedő betegek multidiszciplináris monitorozást igényelnek a szív-, szem- és neurológiai megnyilvánulások kimutatásához. Az emberek nem szintetizálják a fitánsavat, szinte kizárólag étrendjükből nyerik. A fitánsav megtalálható a húsban, a nyílt tengeri halakban és a tejtermékekben [2]. Az emberek a fitolot, a zöld leveles zöldségekben található klorofill oldalláncát fitánsavvá is átalakítják. A fitánsavtól teljesen mentes étrendet lehetetlen elérni. A Refsum-kór kezelése a fitánsav bevitelének étrendi korlátozását igényli a 2. ábra szerint
A diagnózis szérum fitánsav mérésével történő megerősítését követően mindkét testvér alacsony fitán étrendet és plazmaferezist kezdett el. A fitánsav plazmaszintjét az alapvonalon, étrendi kezeléssel és plazmaferezissel együtt a 3. ábra (a) mutatja. Ennek az intenzív kezelésnek a ellenére a két testvérnek továbbra is progresszív tünetei voltak és a plazma fitánsavszintjének hiányos kontrollja volt (meghaladja a normál felső határának tízszeresét). Lényegesen alacsonyabb kezelési célokat javasoltak a szövődmények vagy a betegség progressziójának minimalizálása érdekében.
Ebben a szakaszban a Sydney-i Royal Prince Alfred Kórház lipid- és anyagcserezavar-klinikájára irányították őket a kezelés további optimalizálása érdekében.
2.1. Módszer
Az AF és a VF az étkezés előtt naponta háromszor kezdte az Orlistat szokásos 120 mg-os adagját. Betartásuk azonban nem volt teljes, és az első hónapokban csak napi két adagot kezeltek. Megfelelő alacsony fitánsav-étrendet folytattak megfelelő kalóriabevitel mellett, hogy elkerüljék a fogyást és a rendszeres (3 hetente) plazmacserét. A fitaninsav előtti plazmaferezis előtti átlagos szinteket kiszámoltuk az Orlistat-terápia előtti (2000. április – 2005. június) és (2005. június – 2010. január) időszakokra (3. ábra (b)). A táplálkozás biokémiai markereit, beleértve a zsírban oldódó vitaminszinteket, a kiinduláskor és rendszeres időközönként figyelték, de kiegészítőkre nem volt szükség. A fitánsavat gázkromatográfiával mértük 25 m × 0,32 mm i.d. SGE BP-20 kapilláris oszlop; nonadekánsav (19: 0) metilésztert használtunk belső standardként és fitánsav metilészterrel kalibráltuk (Ultra Scientific, USA).
3. Eredmények
AF-ben a fitánsav átlagos plazmaszintje (3. ábra (b)) a táplálkozás és a plazmaferezis során 3 hetente 14,8 mg/dl (SD 10 mg/dl) volt, ami 6,7 mg/dl-re (SD 2,8 mg/dl) esett. nem vakított orlisztát terápia hozzáadása (P -Teszt). Beszámolt a polyneuropathia, az ataxia, az ichthyosis, az irritábilis bél szindróma és a szívritmuszavar tüneteinek klinikai javulásáról. VF-ben az átlagos plazmas fitánsavszint (3. ábra (b)) az étrenden és a plazmaferezisnél 19,0 mg/dl (SD 13,0 mg/dL) volt, 8,2 mg/dL-re (SD 5,5 mg/dl) esett a vak nélküli orlisztát-terápia során (P -Teszt). Ez az ataxia, a halláskárosodás és a viszketés tüneteinek javulásával járt. A VF azonban továbbra is progresszív látásromlást szenvedett, ami javult a kétoldali szürkehályog-műtétet követően. Ebben az időszakban az AF és a VF a legtöbb időt stabilan tartotta, rövid testsúlycsökkenési időszakokkal, amelyek a mért fitánsavszint enyhe emelkedésével jártak, és a súly stabilizálódásával megoldódtak (3. ábra (a)).
4. Megbeszélés
Az orlisztát hasznos lehet más anyagcserezavarok kezelésében, amelyekben a bélből származó lipidben oldódó anyagok hozzájárulnak a patológiához. A szitoszterinaemia specifikusabb kezelése az NPC1-L1 inhibitoron, az ezetimiben keresztül érhető el. Orlistat-ot alkalmaztunk masszív hipertrigliceridémiával társuló chilomicronaemia kezelésére, amely az akut hasnyálmirigy-gyulladás kockázatával jár. Ezek a betegek az Orlistat terápia alatt nem voltak hasnyálmirigy-gyulladásban, de a triglicerid szint és ennek az állapotnak a klinikai lefolyása köztudottan változó. Nagyszabású, randomizált klinikai vizsgálatra lenne szükség az Orlistat alkalmazásával annak felmérésére, hogy fennáll-e a hasnyálmirigy-gyulladás megelőzése chilomicronaemia esetén. Ez az Orlistat terápiás hatásának jelentése a Refsum-kórban megerősítést igényel más betegeknél. Az Orlistat alkalmazása a fitánsav plazmaszintjének csökkentésére lehetővé teheti az étrend terápia és a plazmaferezis intenzitásának csökkenését, ami jelentős előnyöket jelentene a beteg számára, és csökkentené az egészségügyi rendszerek költségterheit. Kedvezően módosíthatja a Refsum-kór klinikai megnyilvánulásainak progresszióját is.
Összeférhetetlenség
A szerzők összeférhetetlenségről nem számolnak be.
Köszönetnyilvánítás
A szerzők köszönettel tartoznak a Gyermek-, Ifjúsági és Női Egészségügyi Szolgálatnak, a genetikai orvoslás osztályának, Észak-Adelaide, Dél-Ausztráliába a fitánsav elemzéséért, a Newcastle-i John Hunter Kórház plazmaferezis egységének, az RPA Kórház Kórházi Gyógyszerbizottságának az Orlistat ellátásáért . Elismerik továbbá az e betegeket gondozó multidiszciplináris csoportok közötti folyamatos koordinációt és együttműködést.
Hivatkozások
- A. J. Wills, N. J. Manning és M. M. Reilly, „Refsum-kór” Az Orvosok Szövetségének havi folyóirata, köt. 94. sz. 8, 403–406., 2001. Megtekintés: Google Scholar
- A. S. Wierzbicki, M. D. Lloyd, C. J. Schofield, M. D. Feher és F. B. Gibberd: „Refsum-kór: a fitánsavat befolyásoló peroxiszomális rendellenesség α-oxidáció," Journal of Neurochemistry, köt. 80. sz. 5, 727–735., 2002. Megtekintés: Publisher Site | Google ösztöndíjas
- P. Schönfeld és G. Reiser: „Az elágazó láncú fitánsav rotenon-szerű hatása oxidatív stresszt indukál a mitokondriumokban”. A Journal of Biological Chemistry, köt. 281. sz. 11., 7136–7142., 2006. Megtekintés: Kiadói webhely | Google ösztöndíjas
- M. A. McDonough, K. L. Kavanagh, D. Butler, T. Searls, U. Oppermann és C. J. Schofield: „Az emberi fitanoil-CoA 2-hidroxiláz szerkezete meghatározza a Refsum-betegség molekuláris mechanizmusait”. A Journal of Biological Chemistry, köt. 280. sz. 49, 41101–41110, 2005. Megtekintés: Kiadói webhely | Google ösztöndíjas
- D. M. Van Den Brink, P. Brites, J. Haasjes et al., „A PEX7 azonosítása a Refsum-betegségben részt vevő második génként” American Journal of Human Genetics, köt. 72. sz. 2, 471–477., 2003. Megtekintés: Publisher Site | Google ösztöndíjas
- G. Reiser, P. Schonfeld és S. Kahlert: „Az elágazó láncú zsírsav fitánsav toxicitási mechanizmusa, a Refsum-kór egyik markere, asztrocitákban mitokondriális károsodással járnak”. International Journal of Developmental Neuroscience, köt. 24. sz. 2-3., 7136–7142., 2006. Megtekintés: Google Scholar
- S. Idel, P. Ellinghaus, C. Wolfrum et al., „Az elágazó láncú zsírsavak nitrogén-oxid-függő apoptózist indukálnak az érrendszeri simaizomsejtekben”. A Journal of Biological Chemistry, köt. 277. sz. 51, p. 49319–49325, 2002. Megtekintés: Publisher Site | Google ösztöndíjas
- K. Ruther: „Felnőtt Refsum-kór, a retina disztrófiája terápiás lehetőségekkel, elvont” Ophthalmologe, köt. 102. sz. 8, 772–777., 2005. Megtekintés: Google Scholar
- B. C. Ramsay, K. Meeran, D. Woodrow és mtsai., „Refsum-kór bőrszempontjai”, A Royal Society of Medicine folyóirata, köt. 84. sz. 9, 559–560, 1991. Megtekintés: Google Scholar
- T. C. Britton és F. B. Gibberd: „Heredopathia atactica polyneuritiformis (Refsum-kór) család” A Royal Society of Medicine folyóirata, köt. 81. sz. 10, 602–603., 1988. Megtekintés: Google Scholar
- J. P. R. Dick, K. Meeran, F. B. Gibbert és F. C. Rose: „Hipokalaemia akut Refsum-kórban” A Royal Society of Medicine folyóirata, köt. 86. sz. 3, 171–172., 1993. Megtekintés: Google Scholar
- Polyarthritis klinikai megközelítése az orvosi ízületi betegségeknek (Proceedings) DVM 360
- Újszerű megközelítés a peptikus fekély perforációs műtétjén - Ahmadinejad - 2020 - Klinikai esetjelentések -
- Omega-3 zsírsavak; Ígéretes újszerű terápia az alkoholmentes zsírmáj betegség klinikájához
- Orlistat nem konjugált hiperbilirubinémia kezelése Crigler-Najjar betegségben A randomizált
- A nyálka megerősítése új terápiás megközelítés a fekélyes vastagbélgyulladás esetén