A Helicobacter pylori-val összefüggő gyomorrák diétás megelőzése kimchivel
Migyeong Jeong
1 CHA Rákmegelőzési Kutatóközpont, CHA Rák Intézet, CHA Egyetem, Szöul, Korea
Jong-Min park
1 CHA Rákmegelőzési Kutatóközpont, CHA Rák Intézet, CHA Egyetem, Szöul, Korea
Young-Min Han
1 CHA Rákmegelőzési Kutatóközpont, CHA Rák Intézet, CHA Egyetem, Szöul, Korea
Kun Young Park
2 Táplálkozási Főiskola, Busan National University, Busan, Korea
Don Haeng Lee
3 Gasztroenterológiai Tanszék, Orvostudományi Kar, Inha Egyetem, Incheon, Korea
Joon-Hwan Yoo
4 Emésztőrendszeri központ, CHA Egyetem Bundang Orvosi Központ, Seongnam, Korea
Joo Young Cho
4 Emésztőrendszeri központ, CHA Egyetem Bundang Orvosi Központ, Seongnam, Korea
Ki-Baik Hahm
1 CHA Rákmegelőzési Kutatóközpont, CHA Rák Intézet, CHA Egyetem, Szöul, Korea
4 Emésztőrendszeri központ, CHA Egyetem Bundang Orvosi Központ, Seongnam, Korea
Társított adatok
Absztrakt
BEVEZETÉS
A Helicobacter pylori (H. pylori) fertőzést a gyomorrák első kockázati tényezőjének, az I. osztályú rákkeltő anyagnak tekintik, de ez nem magyarázza a gyomor karcinogenezisének teljes képét, mert további módosítások, például környezeti vagy genetikai tényezők, dohányzás, alkohol, étrend, a higiénia és a bakteriális vagy gazda genetikai háttere is szerepet játszik a karcinogenezisben. Nincs egyértelmű bizonyíték a rákmegelőzés támogatására egyedül a H. pylori felszámolásával [1], bár a H. pylori fertőzés a gyomorrák fontos kockázati tényezője. Az étrend módosítása a rákkeltő utak gátlására gyakorlati stratégiák lehetnek a gyomorrák megelőzésében a felszámolás mellett [2]. A gyomor karcinogenezisében azonban az étrendi tényezők maguk is kétélű kardok, amelyek szerepet játszanak a karcinogenezisben, de esetleg megelőzőek másokon. Például bebizonyosodott, hogy a vörös és a feldolgozott húsbevitel a gyomor nem cardia rákának megnövekedett kockázatával jár, míg a zöldségek és a gyümölcsök védőfaktorok, különösen H. pylori antitest-pozitív egyéneknél [3]. Habár a kohorszon alapuló bizonyítékok még mindig hiányoznak, antioxidánsokkal vagy táplálék-gyógyszerekkel kapcsolatos néhány étrendi megközelítés áll rendelkezésre a H. pylori-hoz társuló gyomorbetegségek megelőzésére.
A H. pylori fertőzés étrendi beavatkozásaként új rákmegelőző kimchi (cpKimchi) receptet találtunk ki, és feltettük azt a hipotézist, hogy a cpKimchi étrendi beavatkozása megakadályozhatja a H. pylori-hoz társuló gyomorrákot egérmodellben. A cpKimchi generálása mustárlevelet, körtét, gombát, kínai paprikát és tengeri gubanclét adott szabványosított kimchi receptre (lásd az 1. kiegészítő táblázatot), amelyet előzetes tanulmányunk választott.
EREDMÉNYEK
SKimchi és cpKimchi különböző biológiai hatásai H. pylori-fertőzött sejtmodellben
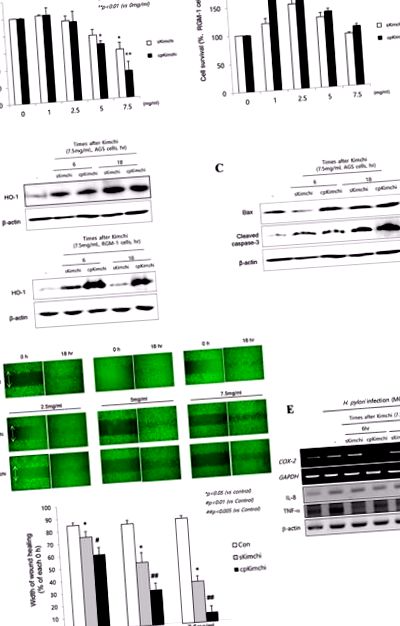
A. A sejtek túlélése MTT vizsgálattal Az MTT vizsgálatot AGS sejtekben (bal oldali) és RGM-1 sejtekben (jobb oldalon) végeztük 1, 2,5, 5 és 7,5 mg/ml koncentrációjú sKimchi és cpKimchi oldható kivonatokkal. Jelentős citotoxicitást figyeltek meg 5 mg/ml-nél nagyobb koncentrációjú kimchi esetén csak az AGS sejtekben, az RGM-1 sejtekben sem, még az 5 mg/ml feletti kimchi után sem B. Minden kimchi-kivonat után a HO-1 Western-blotja C. Western-blot a Bax-hoz és a hasított kaszpáz-3-hoz D. Sebgyógyulási vizsgálat AGS-sejtekben Korábbi tanulmány kimutatta, hogy a cpKimchi szelektív citotoxicitást eredményezett a rákos sejtekben, sebgyógyulási vizsgálat, miután minden kimchi-kivonatot beadtak AGS-sejtekben. A sebgyógyulás jelentős késését figyelték meg a cpKimchi kivonatokkal kezelt csoportban. E. RT-PCR és Western blot a COX-2, IL-8 és TNF-a számára H. pylori fertőzés jelenlétében (MOI = 10). A cpKimchi szignifikánsan gyengítette a H. pylori által kiváltott COX-2 és TNF-a expressziót.
A cpKimchi hatékonyságának és mechanizmusainak javítása H. pylori-fertőzött krónikus atrófiás gastritisben
Attenuált krónikus gyomorhurut 24 hetes étrendi cpKimchi bevitel mellett
A. A COX-2 és a gyulladásos mediátorok változásai csoportonként A Western blot és a nyálkahártya COX-2 expressziójának RT-PCR elemzésével a COX-2 szignifikánsan növekedett a H. pylori fertőzés után, de expressziója szignifikánsan csökkent a cpKimchi-vel kezelt csoportban. Az IL-1β, VEGF, IL-6, MMP-2 RT-PCR-jét csoportonként mutattuk ki, és a cpKimchi szignifikánsan csökkentette ezeket a H. pylori-indukálta gyulladásos mediátorokat. B. A COX-2 expressziók és a makrofág infiltrációk immunhisztokémiai változásai a COX-2 és F/80 csoport expressziója szerint szignifikánsan megnőttek a H. pylori fertőzött kontrollcsoportban. Azonban a cpKimchi krónikus, 36 hetes ivóvízben történő bevitele szignifikánsan csökkentette a COX-2 expressziót, valamint a makrofágok beszivárgását (p 9 kolóniaképző egységek (CFU)/ml. Minden kísérletben 72 órán át TS agar lemezeken növesztett tenyészeteket alkalmaztunk.
H. pylori-fertőzött egerek modellje
Állatok
Bruttó index
Az állatok leölése után az izolált gyomrokat a nagyobb görbület mentén szétvágtuk és jéghideg sóoldattal mostuk. A durva nyálkahártya-károsodás mértékének vizsgálatához a gyomor nyálkahártya-oldalait digitális fényképezőgép segítségével lefényképezték, és a nyálkahártya egy részét azonnal rögzítették 10% -os formalinos oldattal. A gyomornyálkahártya súlyos károsodását három gasztroenterológus értékelte, akiket vakítottak a kezelésekre, durva fekélyindex alkalmazásával [33]. Ezeket a sérüléstípusokat a következőképpen határoztuk meg; I. típus, ödéma, hiperémia vagy egyetlen submucosalis punctiform vérzés; II. típus, submucosalis hemorrhagiás elváltozások jelenléte kis erózióval; típusú III, mély fekély jelenléte erózióval és invazív elváltozásokkal.
Hisztopatológia
A hisztopatológiai elemzéshez a gyomrot 10% semlegesített, pufferolt formalinban rögzítettük, standard módszerrel feldolgoztuk és paraffinba ágyazottuk. A 4 μm vastagságú szakaszokat ezután hematoxilinnal és eozinnal (H&E) festették [34]. A corpus és az antrum mirigy nyálkahártyáit szövettanilag vizsgáltuk. A H. pylori-fertőzés kóros változásait, például gyulladásos sejtek beszivárgását, eróziós elváltozásokat, fekélyképződést, diszpláziát, adenoma képződést (rák előtti elváltozás) három gasztroenterológus osztályozta, akiket elvakítottak a kezelésekre, a szövettani sérülés indexét használva. [35]. Ebben a vizsgálatban a gyulladást a gyulladásos sejtek behatolásának fokozataként határozták meg: 0: nincs, 1: a lamina propria alatt, 2: a nyálkahártya fele 3: a hámmirigy rétegéig (az összes nyálkahártya). Az eróziót az eróziós elváltozás arányaként határoztuk meg, 0: nincs, 1: a hámmirigy-réteg elvesztése (1/3 arány), 2: a nyálkahártya két-három része (2/3 arány) 3: az összes nyálkahártya (3/3 arány) (2. kiegészítő táblázat)
Western blot elemzés
A kivont gyomorszöveteket kétszer mossuk PBS-sel, majd jéghideg sejtlízis pufferben (Cell Signaling Technology, Denver, MA) lizáljuk, amely 1 mM fenil-metil-szulfonil-fluoridot (PMSF, Sigma Aldrich, St Louis, MO) tartalmaz. 20 perces inkubálás után a mintákat 10 000 × g-vel 10 percig centrifugáltuk. Ezután a felülúszókat összegyűjtötték. A lizátumokban lévő fehérjéket nátrium-dodecil-szulfát-poliakrilamid gélelektroforézissel (SDS-PAGE) választottuk el, és polivinilidén-fluorid (PVDF) membránokra vittük át, amelyeket primer antitestekkel inkubáltunk, mossunk, peroxidáz-konjugált szekunder antitestekkel inkubálunk, újból mossuk, majd felhasználással vizualizáljuk. fokozott kemilumineszcencia (ECL) rendszer (GE Healthcare, Buckinghamshire, Egyesült Királyság).
Immunhisztokémiai festés
Miután a paraffin blokkokat viaszmentesítettük és osztályozott alkohollal rehidratáltuk, a szövetrészeket 10 mM citrátpufferrel töltött nyomóedényekben melegítettük mikrohullámú sütőben 10 percig. A tárgylemezeket 15 percig vízben hűtöttük és PBS-ben mostuk. A tárgylemezeket egy éjszakán át inkubáltuk az elsődleges antitesttel. Inkubálás után egy későbbi reakció képződött VECTOR kit alkalmazásával (Vector Laboratories, Inc., Burlingame, CA). Végül a tárgylemezeket 3, 3ȃ-2-diaminobenzidinnel (Invitrogen Life Technologies) inkubáltuk és ellenfestettük hematoxilinnel (Sigma-Aldrich). Az antitest pozitív sejtek számát a szubmezoteliális terület 5 mezőjében határoztuk meg, amelyeket véletlenszerűen választottunk ki minden egérben, és × 100 nagyítással vizsgáltuk. Az értékeket átlagként ± S.E.M.
PAS festés
Perjódsav- és Schiff-festéshez a glikokonjugátumok hisztokémiai festését Pandurangan módszere szerint hajtjuk végre [36], 2% periódusos sav és Schiff (PAS) reagens használatával sötétben 20 percig. Ennek eredményeként a PAS festési pontszám 10 (kiváló tartósítás) és 0 (rossz tartósítás) között volt.
TUNEL assay
Az apoptózis kimutatására a gyomorszöveteket terminális dezoxinukleotidil-transzferáz-mediált dUTP nick-end jelölés (TUNEL) módszerrel festettük, a DeadEnd ™ fluorometrikus TUNEL rendszert használva (G3250 #, Promega, USA).
In vitro H. pylori-fertőzött sejtmodell
Sejtkultúra és citotoxicitási vizsgálat
A patkány gyomor hámsejtjeit (RGM-1) H. Matsui professzortól (Tsukuba Univ., Japán) kaptuk, az AGS sejteket az ATCC-től (Manassas, VA) szereztük be, ahol a sejteket megfelelően tárolták és rutinszerűen hitelesítették (beleértve a DNS-t is) ujjlenyomat). Laboratóriumunkban végzett újraélesztés után az összes sejtet 6 hónapnál nem hosszabb ideig használtuk fel. Az AGS-sejteket RPMI-1640 táptalajban (Gibco BRL, Gaithersburg, MD) és az RGM-1 sejteket tenyésztettük DMEM tápközegben. Minden táptalaj 10% magzati szarvasmarha-szérummal (Gibco BRL) kiegészítve 37 ° C-on, 5% CO2-ban. A sejtek életképességét MTT kolorimetriás vizsgálattal értékeltük. MTT [3- (4, 5-dimetil-tiazol-2-il) -2,5-difenil-tetrazolium-bromidot] a Sigma Chemical Co.-tól (St. Louis, MO) vásároltunk. Az 50 g szűrletet 1 liter vízzel összekeverjük, majd liofilizáljuk. A sejteket 96 lyukú lemezekre szélesztettük 104 sejt/ml koncentrációban, és hagytuk 24 órán át tapadni. Kimchi kivonatot alkalmaztunk a vizsgálati üregekben különböző koncentrációkban 24 órán át.
A sejtmigráció élő sejtképpel figyelhető meg
Dózisfüggő sKimchi-vel és cpKimchi-vel kezelt AGS-sejteket pipetta hegyével megsebesítettük, és a ScopeTek MDC200 (CHA Egyetem, Szöul, Korea) alatt megfigyeltük, amelyben a sejtek növekedését 18 órán keresztül ellenőriztük és 3 perc intervallummal rögzítettük. Három különböző csoportot figyeltek meg; Nincs kezelés, az sKimchi dózisfüggő kezelése és a cpKimchi kezelése. A 18 óra után készült állóképpel a sejtek növekedésének átlagos sebességét a csoport szerint kiszámoltuk, és megjelenítettük a sejtvándorlások átlagos szintjét.
ELISA assay
A gyomor összegyűjtését követően 10 mM nátrium-foszfát-pufferben, pH 7,4 (1 ml) homogenizáltuk. Centrifugálás (9000xg) után a felülúszó PGE2-szintjét ELISA-val mértük, és a koncentrációt pg/mg fehérje értékben fejeztük ki. A folyamatokat a Prostaglandin E2 expressz EIA kit kézirata szerint végeztük (Cayman, Ann Arbor, MI).
Western-blot a HO-1, a Bax, a PARP és a hasított capspase-3 esetében
A kivont sejteket kétszer mossuk PBS-sel, majd jéghideg sejtlízis pufferben (Cell Signaling Technology, Denver, MA) lizáljuk, amely 1 mM fenil-metil-szulfonil-fluoridot (PMSF, Sigma Aldrich, St Louis, MO) tartalmaz. 20 perces inkubálás után a mintákat 10 000 × g-vel 10 percig centrifugáltuk. Ezután a felülúszókat összegyűjtötték. A lizátumokban lévő fehérjéket nátrium-dodecil-szulfát-poliakrilamid gélelektroforézissel (SDS-PAGE) választottuk el, és polivinilidén-fluorid (PVDF) membránokra vittük át, amelyeket primer antitestekkel inkubáltunk, mossunk, peroxidáz-konjugált szekunder antitestekkel inkubálunk, újból mossuk, majd felhasználással vizualizáljuk. fokozott kemilumineszcencia (ECL) rendszer (GE Healthcare, Buckinghamshire, Egyesült Királyság).
Statisztikai analízis
Az eredményeket átlagként fejezzük ki (szórás (SD). A statisztikai elemzéseket a GraphPad Prism (GraphPad Software, La Jolla, CA, USA) és az SPSS szoftver (12.0 verzió; SPSS Inc., Chicago, IL, USA) segítségével végeztük. A csoportok közötti szignifikanciát Mann-Whitney U teszttel határoztuk meg. A statisztikai szignifikanciát p-nél elfogadtuk (1.4M, pdf)
Köszönetnyilvánítás
Köszönjük Dr. Eun-Hee Kim technikai segítségét.
Lábjegyzetek
PÉNZÜGYI TÁMOGATÁS
Ezt a kutatást a Koreai Heath Ipari Fejlesztési Intézet (KHIDI), valamint az emésztési rendellenességeket célzó egészségügyi termékek fejlesztésének nemzeti hatékonysági értékelésének központja (NCEED) támogatta, és a Koreai Élelmiszerek Globalizációja K + F program támogatásával támogatták. a Koreai Köztársaság Élelmezési, Mezőgazdasági, Erdészeti és Halászati Minisztériuma által.
- Az étrendi magatartás, a fizikai aktivitás és a rák elleni védekezés és a népesség energiamérlege
- Az étrendi zsírbevitel és a szív- és érrendszeri betegségek megelőzése szisztematikus felülvizsgálat
- Az étrendi emulgeálószerek által kiváltott alacsony fokú gyulladás elősegíti a vastagbél karcinogenezis rákkutatását
- Az étrendi rost segíthet a gyermekkori elhízás megelőzésében Dr
- Gyomorproblémák - A gyomorproblémák tünetei, kezelése és megelőzése