A hiperandrogenémia és a metabolikus szindróma közötti összefüggés kórosan elhízott nőknél
Absztrakt
Háttér
A női hasi elhízás hyperandrogenémiához (HA) társul, de kevés tanulmány foglalkozott a HA és a metabolikus szindróma (MetS) lehetséges összefüggésével az elhízott nők körében. Egyes tanulmányok azt mutatják, hogy az inzulinrezisztencia különböző mechanizmusok révén okozhatja a HA-t. Másrészt kétirányú kapcsolatot javasoltak a HA és az inzulinrezisztencia között. Ezért azt a célt kívántuk megvizsgálni, hogy a kórosan elhízott, HA-s nőknél nagyobb-e az esély a MetS-re és annak összetevőire, mint a HA-val nem rendelkezők (kontrollok), függetlenül a policisztás petefészek-szindróma (PCOS) státusától.
Mód
Ez a keresztmetszeti vizsgálat 1900 egymást követő kezelést tartalmazott, kórosan elhízott, 0,6 definiált HA-t keresve. A korábban diagnosztizált PCOS-ban szenvedő nők, valamint azok, akiknek klinikai vagy biokémiai hiperandrogenizmussal kombinált oligo-/anovulációja volt, PCOS-ként definiáltak. A HA és a MetS közötti sokszintű asszociációkat logisztikai regresszióanalízissel értékeltük.
Eredmények
1900 betegesen elhízott nőből 1089 (57%), 846 (45%) és 312 (16%) MetS, HA és PCOS volt. A kontrollokkal (HA nélkül) összehasonlítva a HA-val rendelkező nők fiatalabbak voltak (34 [1] év vs. 39 [2]), o
Háttér
A policisztás petefészek szindróma (PCOS) a leggyakoribb női endokrinopathia, amely a reproduktív korú nők 8–12% -át érinti [1], és az elhízott nők 10–35% -át [2–4]. A PCOS meddőséggel, hiperandrogenémiával, csökkent glükóz toleranciával és 2-es típusú cukorbetegséggel jár együtt [5]. Úgy gondolják, hogy a megnövekedett androgének és inzulin szintje hozzájárul a PCOS patofiziológiájához [5]. A hiperandrogenémia (HA) az emelkedett szabad tesztoszteronszinttel rendelkező PCOS biokémiai jellegzetességét képezi, ami az oligomenorrhea-ban szenvedő nők kóros laboratóriumi eredményeinek többségét adja [6].
A túlsúly a HA-val társul [7]. Ezenkívül az elhízott nőknél fellépő hiperinsulinémia közvetlenül növelheti a szabad tesztoszteron szintet azáltal, hogy csökkenti a nemi hormon kötő globulin szintézisét a májban [8]. Másrészt a rágcsáló modellek kimutatták, hogy a HA elősegíti az inzulinrezisztenciát, csökkenti az energiafelhasználást, és ennek megfelelően növeli a hasi elhízás és az anyagcsere kockázati tényezők kockázatát [9, 10]. Több mint 2500, 42 és 52 év közötti amerikai nőből álló többnemzetiségű mintában az oligomenorrhoea csak akkor társult a metabolikus szindrómához (MetS), ha egybeesett a HA-val [11]. Ezzel szemben a HA-ban szenvedő nőknél jelentősen megnőtt a MetS kockázata, függetlenül a menstruációs gyakoriság állapotától [11].
A petefészkek reakciója a luteinizáló hormonra (LH) a megnövekedett androgének forrása a PCOS-ban [12]. Emellett a mellékvese-szteroidok megnövekedett válasza PCOS-ban szenvedő nőknél csak az ACTH mellékvese-stimulációjával tartható fenn, ami a fokozott mellékvese androgéntermelés másodlagos hatására utal, nem pedig a mellékvese veleszületett enzimhiányára [13].
Nem világos, hogy a HA hogyan befolyásolhatja a szív- és érrendszeri betegségeket. A hasi elhízott, PCOS-ban szenvedő nőket a szív- és érrendszeri betegségek nagy kockázatának tekintik, és pozitív összefüggést jelentettek a koszorúér-betegség és a klinikai hiperandrogenizmus (hirsutizmus és pattanások) között [14]. Másrészt egy populációalapú tanulmány kimutatta, hogy a premenopauzás túlsúlyos, PCOS-ban szenvedő nőknél nem volt nagyobb a koszorúér-betegség kockázata, mint a PCOS-nál nem szenvedőknél [15]. Ennek ellenére a PCOS-ban és HA-ban szenvedő nőknél gyakoribb az elhízás és a káros anyagcsere-rendellenességek aránya, mint a HA-val nem rendelkezőknél [16]. Legjobb tudomásunk szerint egyetlen korábbi tanulmány sem értékelte a HA hatását a MetS-re függetlenül az elhízott nők körében a PCOS jelenlététől vagy hiányától.
A vizsgálat elsődleges célja annak megvizsgálása volt, hogy a premenopauzás betegségben szenvedő, kórosan elhízott, HA-val rendelkező nőknél nagyobb az esély a MetS-re és annak összetevőire (alacsony HDL-koleszterinszint, hipertrigliceridémia, emelkedett vérnyomás és dysglykaemia), mint a HA nélküli nők, függetlenül a PCOS státusztól.
Mód
Tervezési és tanulmányi populáció
2005. november 28. és 2014. július 28. között összesen 2681 egymást követő, kórosan elhízott nőt kerestek fel a norvégiai Vestfold Hospital Trust Morbid Elhízás Központjában. A mind a menopauza előtti, mind a posztmenopauzás nők biológiai elfogultságának elkerülése érdekében kizártunk 743 ≥50 éves nőt [17–19]. A HA-ról 38 nő hiányzott (a PCOS hiányzik n = 34 és a PCOS jelen van n = 4), így 1900, kórosan elhízott, reproduktív korú nő szerepel e keresztmetszeti elemzésben. A tanulmányt az Orvosi és Egészségügyi Kutatásetikai Regionális Bizottság hagyta jóvá (S-05175). A résztvevőket írásbeli, tájékozott beleegyezés benyújtása után vették fel, és a tanulmányt a Helsinki Nyilatkozattal [20] összhangban végezték el.
Definíciók
A MetS-t a Nemzetközi Diabetes Szövetség epidemiológiai és megelőzési munkacsoportjának közös időközi nyilatkozata alapján határoztuk meg; Nemzeti Szív-, Tüdő- és Vérintézet; American Heart Association; Szív Világszövetség; Nemzetközi Ateroszklerózis Társaság; és az elhízás vizsgálatának nemzetközi szövetsége (2009); ha a WC ≥ 80 cm, a négy kritérium közül legalább kettővel együtt: 1) alacsony HDL-koleszterinszint; A HDL-koleszterin 0,6) meghatározása szerint HA [25] volt. Azoknál a nőknél, akiknél korábban diagnosztizálták a PCOS-t, és azoknál, akiknek FTI-ja> 0,6 vagy hirsutismusuk kombinálódott oligo-/anovulációval, PCOS-t definiáltak [16, 26].
Adatgyűjtés
A betegek súlyát és magasságát könnyű ruházatban, cipő nélkül mérték, és ezt követően kiszámították a BMI-t (kg/m 2). A WC-t félúton mértük a legalacsonyabb borda margó és a csípőcsík között. A vérnyomást megfelelő mandzsettával mértük legalább 5 perc pihenés után, a páciens függőleges helyzetben ülve. Három mérést regisztráltunk, és a második és a harmadik mérés átlagát használtuk a vizsgálatban. Minden antropometriai és vérnyomásmérést képzett tanulmányi személyzet végzett.
Laboratóriumi elemzés
A vérmintákat éjszakai böjt után venipunktúrával nyertük, és Vacutainers® gélcsövekbe gyűjtöttük. A szérumot két órán belül elválasztották a sejtektől.
Statisztikai analízis
Az adatokat átlagként (SD) vagy arányként adjuk meg. Folyamatos és kategorikus változókat hasonlítottunk össze független t-próba és χ 2 teszt vagy adott esetben Fisher pontos próbája segítségével. A korrelációkat Pearson-féle korrelációs együtthatóval (r) számoltuk a normálisan elosztott változókra, és Spearman-féle Rho-val (ρ) a nem normálisan elosztott változókra. A demográfiai, antropometriai és metabolikus változásokat elemeztük, beleértve a teljes vizsgálati populációt és a PCOS jelenlétére vagy hiányára való rétegzés után.
A MetS-t és komponenseit függő változóként, a HA-t mint elsődleges magyarázó változót modelleztük. A HA és a MetS közötti összefüggést kiigazítottuk a jelentős logward regressziós megközelítéssel azonosított zavarók vonatkozásában. A 0,10 alatti p-értékű változókat bekerültük a végső modellbe (Wald-teszt). Következésképpen, koszorúér-betegség (igen/nem), prednizolon-használat (igen/nem), krónikus obstruktív tüdőbetegség (igen/nem), ízületi fájdalom (igen/nem), ösztrogének vagy gesztagénes gyógyszerek alkalmazása (igen/nem) és pajzsmirigy-stimuláló hormont távolítottak el a regressziós modellből. A modelleket a végső multivariábilis elemzés során a következő kovariánsokhoz igazítottuk: életkor (évek), cukorbetegség családtörténete (igen/nem), húgysav (μmol/L), szorongás vagy depresszió (igen/nem), kolelithiasis (igen/nem) nem), a dohányzás története (jelenlegi vagy korábbi/soha), fizikai aktivitás (≥1 óra intenzív fizikai aktivitás/hét), mellékpajzsmirigy-hormon (pmol/L) és D-25-OH-vitamin (nmol/L). Úgy döntöttünk, hogy nem alkalmazkodunk a WC és a HOMA IR-hez annak érdekében, hogy elkerüljük a HA és a MetS közötti oksági útban ismert változók által bekövetkező túlzott beállítási torzítás lehetőségét [10, 28].
Egy- és többváltozós logisztikus regressziós modelleket alkalmaztunk a HA és MetS és annak összetevői közötti összefüggések (hipertrigliceridémia, alacsony HDL-koleszterinszint, emelkedett vérnyomás és dysglykaemia) értékelésére mind a 1900 betegben. Ezenkívül az elemzéseket megismételtük egy PCOS nélküli elhízott nők alcsoportjában és egy másik PCOS-os csoportban. Az életkor és a PCOS szerinti lehetséges hatásmódosításokat úgy vizsgáltuk, hogy a kor * HA és a PCOS * HA termékeket interakciós kifejezésekként vettük be a multivariábilis elemzésekbe, MetS-sel mint függő változóval.
Az illeszkedés jóságát a Hosmer és a Lemeshow teszttel teszteltük. A 0,05 alatti P-értékeket statisztikailag szignifikánsnak tekintettük. Az elvégzett statisztikai vizsgálatok jelentős száma miatt azonban különös figyelmet kell fordítani a kisebb, azaz a 0,01 alatti P-értékekre. Az elemzéseket az IBM SPSS statisztikák 20 felhasználásával hajtották végre.
Eredmények
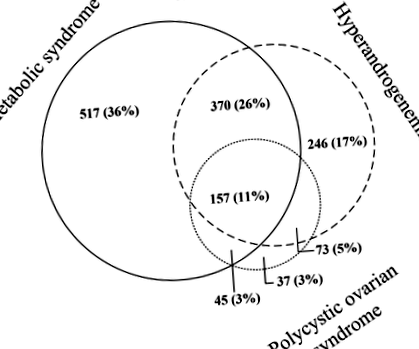
Az 1900 betegségesen elhízott, 50 év alatti (átlagéletkor 37 [SD 8] év) nők közül összesen 1089 (57%), 846 (45%) és 312 (16%) volt MetS, HA és PCOS. Összesen 1445 nőnél volt metabolikus szindróma (MetS), hiperandrogenémia (HA) vagy policisztás petefészek-szindróma (PCOS), míg 455 nőnek nem volt sem MetS, HA vagy PCOS. A nők MetS, HA és PCOS átfedését az 1. ábra mutatja be.
Az ábra átfedést mutat az 1445 nő között, amelyekre jellemző a metabolikus szindróma, a policisztás petefészek szindróma és a hiperandrogenémia (HA). A fenti állapotok nélküli nőket (n = 455) nem vették fel az 1. ábrára
A teljes vizsgálati populációban a HA-val rendelkező nők fiatalabbak voltak (átlagos [SD] életkor 34 [1] vs. 39 [2] év), o 1. táblázat: A beteg jellemzői a policisztás petefészek-szindróma (PCOS) és a hiperandrogenémia (HA) jelenléte vagy hiánya szerint
A HA-val rendelkező nők aránya 80% -ról csökkent (2. ábra
Az FTI gyengén korrelált a HDL-koleszterinnel, a szisztolés és a diasztolés vérnyomással (r = 0,10, o 0,111). Nem találtunk szignifikáns kölcsönhatást a HA és az életkor között (o = 0,834) vagy HA és PCOS között (o = 0,527).
Az egyváltozós elemzésben a HA a MetS 1,5-szeresére emelkedett esélyével társult (OR 1,45 [95% CI 1,20, 1,74]). Ez az összefüggés statisztikailag szignifikáns maradt a lehetséges zavaró tényezők kiigazítása után (1,61 [1,27, 2,02]) (2. táblázat és 3A. Ábra). Ezenkívül a HA a dysglykaemia (1,65 [1,28, 2,11]), az alacsony HDL-koleszterinszint (1,58 [1,27, 1,97]) és a hipertrigliceridémiával (1,43 [1,15, 1,79]) kb. A HA nem társult emelkedett vérnyomással (1,06 [0,85, 1,34]). 1588 PCOS nélküli nő részanalízise azt mutatta, hogy a HA továbbra is szignifikánsan társul MetS-sel (OR 1,52 [95% CI 1,18, 1,96), dysglykaemiával (1,71 [1,30, 2,25]), alacsony HDL-koleszterinnel (1,55 [1,22, 1,98] ) és hipertrigliceridémia (1,36 [1,06, 1,74]) (3B. ábra). Ezzel szemben a HA nem kapcsolódott szignifikánsan a MetS-hez, sem annak összetevőihez a PCOS-ban szenvedő nőknél (3C. Ábra).
Az ábra mutatja a metabolikus szindróma (MetS) és összetevőinek 95% -os konfidencia intervallummal (OR [95% CI]) a változékony szorzók arányát kórosan elhízott, hiperandrogenémiában szenvedő nőknél, összehasonlítva a hiperandrogenémia nélküli (HA) nőkkel (referencia). Az A panel a vizsgálatba bevont összes nőt magában foglalja (n = 1900), míg a B és C panel az alanalízisekben szereplő nőket tartalmazza; PCOS hiányzik (n = 1588) és a PCOS jelen van (n = 312)
Vita
A premenopauzás fehér, kórosan elhízott nők vizsgálatának legfőbb és újszerű megállapítása az volt, hogy a HA a MetS 61% -kal megnövekedett korrigált esélyeivel társult, és hogy ezt az összefüggést főként a dysglykaemia és a dyslipidemia megnövekedett esélyei vezérelték. Bár a HA prevalenciája csökkent, míg a MetS prevalenciája az életkor előrehaladtával nőtt, a HA továbbra is a MetS és összetevői, a dysglykaemia és a dyslipidemia független előrejelzője maradt.
Hyperandrogenemia és a metabolikus szindróma
Jelen tanulmány eredményei összhangban állnak egy másik keresztmetszeti vizsgálattal, amely 2543 többnemzetiségű túlsúlyos pre- és perimenopauzális nőt tartalmaz, akik átlagosan tíz évvel idősebbek voltak, mint a jelen vizsgálat résztvevői (46, illetve 37 év), [11]. Az előző vizsgálatban a HA-val rendelkező nőknek, a menstruációs ciklusoktól függetlenül, 1,5-szer nagyobb volt a MetS kockázata a HA-val nem rendelkezőkhöz képest [11]. Az oligomenorrhoában és a HA-ban szenvedő nőknél a MetS esélye kétszer nagyobb volt [11]. 1588 PCOS nélküli súlyosan elhízott nő alelemzésében a HA továbbra is a MetS, a dysglykaemia, az alacsony HDL-koleszterinszint és a hipertrigliceridémia előrejelzője volt. Ezzel szemben a premenopauzában lévő nők nemrégiben végzett tanulmányában nem derült ki összefüggés az androgénfelesleg, a menstruációs rendellenességek és az előforduló MetS vagy az ön által bejelentett szív- és érrendszeri betegségek között [28].
Lehetséges mechanizmusok, amelyek összekapcsolják a hiperandrogenémiát az inzulinrezisztenciával és a zsigeri elhízással
Állati (rágcsáló) vizsgálatok azt mutatják, hogy az androgének a vázizomzatra és a zsírszövetre gyakorolt közvetlen hatások révén inzulinrezisztenciát produkálhatnak, amelyet az inzulinreceptor – glikogénszintézis változásai, az adipokin szekréció megváltoztatása és a zsigeri adipozitás növelése közvetít [9]. Ráadásul egy 13 elhízott és 30 nem elhízott nőből álló kisméretű tanulmány kimutatta, hogy az antiandrogén kezelés csak a nem elhízott nőknél fordította meg a perifériás inzulinrezisztenciát, míg a központi elhízásnak közvetlen szerepe lehet az androgén hiperszekréciójában [29, 30]. Szintén egy fiatal, túlsúlyos nőkről szóló nemrégiben végzett tanulmány azt sugallta, hogy a testzsír és a HA közötti kapcsolatot elsősorban az inzulinrezisztencia közvetíti [24]. A testzsír, az inzulinrezisztencia és a HA kölcsönhatásai hozzájárulnak a komplex mintázathoz, ami megnehezíti az egyes komponensek szerepének meghatározását. Bár Tosi et al. lehet, hogy nem hasonlítható közvetlenül a mieinkhez, gyenge, de szignifikáns összefüggést jelentünk az inzulinrezisztencia, valamint a HOMA IR és az FTI között. Ennek megfelelően, bár a HA függetlenül kapcsolódott a MetS-hez, az inzulinrezisztencia részben közvetíthette ezt a hatást.
A hiperandrogenémia és a diszlipidémia közötti összefüggés
Vizsgálatunk szignifikáns inverz kapcsolatot mutatott ki a HA és a HDL-koleszterin szint között, amely összhangban áll a PCOS-ban szenvedő nők korábbi tanulmányaival [31, 32]. Csökkent HDL-koleszterinszintről beszámoltak azoknál a peri- és posztmenopauzás nőknél is, akik hormonpótló terápiához adott androgén készítményeket kaptak, és transzdermális tesztoszteron kezelés után [33, 34]. Továbbá a PCOS-ban szenvedő nők alacsony SHBG-szintje alacsony inzulinrezisztenciától és elhízástól független alacsony HDL-koleszterinszinttel járt [35]. Ezzel szemben egy fiatal, túlsúlyos nők tanulmánya nem mutatott különbséget a diszlipidémiában a HA-ban szenvedő nőknél a HA nélküli nőkhöz képest [24]. Így a HA hatása a diszlipidémiára továbbra sem tisztázott, és további kutatások indokoltak.
Hyperandrogenemia és dysglykaemia
A HA-val rendelkező nők aránya csökkent, míg a dysglykaemiás nők aránya az életkor előrehaladtával nőtt (2. ábra). Ennek ellenére szignifikáns összefüggést találtunk a HA és a kortól független dysglykaemia között.
A vizsgálatok kimutatták, hogy a PCOS-ban szenvedő nőknél magas a konverziós arány a csökkent cukorbetegség-tolerancia és a diabetes mellitus között [36, 37]. Eredményeink azt mutatták, hogy a PCOS-szal rendelkező és anélküli nőknél hasonló a prevalencia a dysglykaemiaban. Azonban a HA-ban szenvedő betegeknél a dysglykaemia esélye körülbelül 65% -kal nőtt a HA-val nem rendelkezőkhöz képest, és a kapcsolat megerősödött a PCOS-ban szenvedő nők kizárása után. Ezek a megállapítások alátámasztják azt a hipotézist, miszerint a HA részt vehet a dysglykaemia patofiziológiájában, függetlenül a PCOS státusztól.
Hyperandrogenemia és vérnyomás
Nem találtunk szignifikáns összefüggést a HA és az emelkedett vérnyomás között. Ez ellentétben áll egy fiatal normális vagy túlsúlyos ázsiai nők PCOS-val végzett vizsgálatának eredményeivel, amelyek kimutatták, hogy a magas biohasznosuló tesztoszteronszint az emelkedett vérnyomással jár [38]. Egy másik, középkorú, normál és túlsúlyos nők vizsgálatában az arc hirsutizmusa magasabb szisztolés vérnyomással, míg a végtag-hirsutizmus alacsonyabb diasztolés vérnyomással társult [39]. Ebben a tanulmányban a premenopauzás betegségben szenvedő, betegesen elhízott nők valójában kevésbé használták vérnyomáscsökkentő gyógyszert, mint a HA nélküli nők (18% vs. 25%). Érdekes módon egy nemrégiben publikált, normál és túlsúlyos svéd férfiak és nők keresztmetszeti vizsgálata erős inverz összefüggést mutatott ki a vérnyomás és az SHBG között, míg a szabad tesztoszteron koncentrációja nem volt összefüggésben a magas vérnyomással [40]. A szerzők feltételezték, hogy az SHBG közvetlen hatással lehet az endothelsejtekre az SHBG receptorán keresztül, de ez az összefüggés csak a postmenopauzás, ≥50 éves nőknél volt szignifikáns [40]. Ezzel szemben tanulmányunk nem mutatott összefüggést az SHBG és az emelkedett vérnyomás között a premenopauzás nőknél (az adatokat nem közöljük).
Erősségek és korlátozások
A jelen tanulmány legfőbb erőssége az egymást követő kezelések nagy csoportja, amelyek kórosan elhízott nőket keresnek. A vizsgálatban résztvevőket azonban egy tercier ellátási központba utalták, hogy értékeljék és kezeljék bariatrikus műtéttel, orvosi terápiával vagy hosszú távú életmód-rehabilitációval a kóros elhízás miatt. Ennek megfelelően az eredmények nem általánosíthatók az általános elhízott népességre (azaz nem kezelést igénylő alanyokra).
A tesztoszteron mérésére immunvizsgálatot alkalmaztunk. Habár a hagyományos immunvizsgálatok magas szinten mérik a megbízható tesztoszteront, az immunvizsgálatok szerint alacsony koncentrációknál kevésbé megbízhatóak [41]. A dietil-extrakció szétválasztási eljárását azonban manuálisan hajtották végre, így csökkentenie kellett volna a hamisan magas eredmények számát.
Továbbá, bár a FTI> 0,6-ot definiáltuk HA-ként ebben a vizsgálatban, más adrenokortikális prekurzor szteroidok, beleértve a pregnenolont, a 17-hidroxipregnenolont, a dehidroepiandroszteront (DHEA), az androszténdiont, a 11-dezoxi-kortizolt és a kortizolt is hozzájárulhatnak a HA klinikai megnyilvánulásaihoz. Mindazonáltal a szabad tesztoszteronszint továbbra is az oligomenorrhea-ban szenvedő nőknél a laboratóriumi meghatározó tényező, és a petefészkek jelentik az androgénfelesleg legfőbb forrását PCOS-val és anélkül [6, 12].
Sajnos nem rendelkezünk pontos menopauza-adatokkal. Bizonyos bizonyítékok vannak arra, hogy a magasabb BMI későbbi menopauzát okozhat. Egy tanulmány arról számolt be, hogy az elhízott nők (BMI ≥30 kg/m 2) menopauza medián életkora 53 év volt [17]. Következésképpen az 50 év feletti nők kizárásával néhány kórosan elhízott premenopauzás nő kihagyható elemzésünkből.
Végül a kórosan elhízott nők többsége (97%) kaukázusi volt, és ennek eredményeként előfordulhat, hogy nem alkalmazhatók más etnikumú nőkre.
Következtetés
Ebben a tanulmányban a MetS, a PCOS és a HA prevalenciája magas volt a kórosan elhízott nők körében
- A húgysav, a metabolikus szindróma és a vesebetegség American Society of Nephrology
- Mi a metabolikus szindróma kritériumai, tünetei, étrend és kezelés
- Háromlépcsős laparoszkópos műtét kórosan elhízott, Hinchey III divertikulitiszben szenvedő beteg esetében
- A metabolikus szindróma Johns Hopkins Medicine
- Az elhízott fajok külön kérdés az elhízás és az anyagcserezavarok betegségmodelljei; Mechanizmusok