A szitagliptin-foszfát áttekintése: új típusú kezelés a 2-es típusú cukorbetegség számára
Absztrakt
A szitagliptin (Januvia®, Merck Pharmaceuticals) egy dipeptidil-peptidáz inhibitor (DPP-4 inhibitor), amelyet nemrégiben engedélyeztek a 2-es típusú cukorbetegség kezelésére. Mint más DPP-4 inhibitorok, hatását az inkretin hormonok, a glukagon-szerű peptid-1 (GLP-1) és a gyomor-gátló polipeptid (GIP) növekvő szintje közvetíti. A szitagliptin hatékonyan csökkenti a HbA1c-értéket és az éhezést, valamint az étkezés utáni glükózt monoterápiában és más orális antidiabetikus szerekkel kombinálva. Serkenti az inzulin szekrécióját, ha hiperglikémia van jelen, és gátolja a glükagon szekrécióját. A klinikai vizsgálatokban súlysemleges. Ez a cikk áttekintést nyújt a szitagliptin hatásmechanizmusáról, farmakológiájáról, valamint klinikai hatékonyságáról és biztonságosságáról a 2-es típusú cukorbetegség terápiájában.
A GLP-1 terápiás potenciáljának kihasználása 2-es típusú cukorbetegségben
Mivel a glukagon-szerű peptid-1 (GLP-1) maga a rövid biológiai felezési ideje miatt nem megvalósítható a 2-es típusú cukorbetegség kezelésében, két fő stratégiát dolgoztak ki a GLP-1 jótékony hatásainak hasznosítására (Drucker 2006) . Egyrészt a natív GLP-1-hez nagy hasonlósággal rendelkező, hosszú hatású, dipeptidil-peptidáz ihibitor (DPP-4 inhibitor) ellenálló peptidek alkalmazhatók injekciós terápiás szerként (inkretin utánzó szerek vagy GLP-1 analógok). Az exendin-4 vagy exenatid rekombináns formában egy ilyen peptid, amely eredetileg a gila szörny nyálában található. Az exenatid nagyon magas aminosav-szekvencia-hasonlóságot mutat a GLP-1-vel, és egy GLP-1 receptor agonista. 2-es típusú cukorbetegség kezelésére engedélyezték olyan betegeknél, akiknek a glükózkontrollja nem volt elegendő metforminnal, szulfonilureákkal vagy ezek kombinációjával Byetta® (Eli Lilly Pharmaceuticals, Indianapolis, IN, USA és Amylin Pharmaceuticals, San Diego) alatt., CA, USA) (Bray 2006). A liraglutid egy olyan GLP-1 analóg, amelyet a Novo Nordisk Pharmaceuticals (Koppenhága, Dánia) fejleszt ki, és a III. Fázisú klinikai vizsgálatok során a 2. típusú cukorbetegség hatékonyságát és biztonságosságát értékelik (Feinglos et al 2005).
A GLP-1 hatások 2-es típusú cukorbetegségben történő felhasználásának másik módja a DPP-4 orális hatóanyagok általi közvetlen gátlása (Deacon és Holst 2002). A szitagliptin (Januvia®, Merck Pharmaceuticals, Whitehouse Station NJ, USA) egy rendkívül szelektív DPP-4 inhibitor, amelyet a 2-es típusú cukorbetegség kezelésében engedélyeztek. Más DPP-4 inhibitorok szintén fejlesztés alatt állnak, vagy közel állnak a jóváhagyásukhoz, például a vildagliptin (Galvus®, Novartis Pharmaceuticals, Bázel, Svájc).
DPP-4 gátlás 2-es típusú cukorbetegségben
Asztal 1
Hormonok és szabályozó peptidek a DPP-4 szubsztrátjaiként (módosítva: Mentlein (1999)
| GLP-1 | GRH |
| GIP | Interleukin 1β |
| GLP-2 | Interleukin 2 |
| PACAP | IGF-1 |
| NPY | Prolaktin |
| PYY | HCG |
| Anyag | Bradykinin |
| RANTES |
Rövidítések: DPP-4, dipeptidil-peptidáz inhibitor; GIP, gyomor-gátló polipeptid; GLP, glukagonszerű peptid; GRH, gonadotropin-felszabadító hormon; HCG, humán koriongonatotropin; IFG-1, inzulinszerű növekedési faktor-1; NPY, Y neuropeptid; PACAP, hipofízis-adenilát-cikláz-aktiváló polipeptid; PYY, YY peptid; RANTES, aktiválással szabályozva, normális T-sejt expresszálódik és szekretálódik.
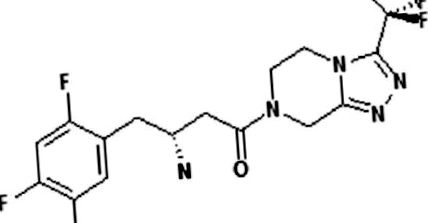
A szitagliptin farmakológiai profilja
A szitagliptin szerkezeti képlete.
Állatkísérletek szitagliptinnel
A szigeti sejtek összetételének morfometrikus elemzése STZ-indukálta diabéteszes egerekben az MK0431 (dez-fluor-szitagliptin) kezelés után. Az immunhisztokémiailag festett hasnyálmirigy-metszetekről digitális képeket készítettünk, hogy az egész hasnyálmirigy-szakaszokban az inzulin-pozitív terület százalékos arányát béta-sejt térfogatként számszerűsítsük (A) (#p 4. ábra). Valamennyi monoterápiás vizsgálatban a szitagliptin súlysemleges volt, a 200 mg/nap dózis még 1,1 kg-os súlycsökkenéshez vezetett a vizsgálati betegeknél. Míg a 200 mg-os adag erősebb volt, mint a 100 mg-os dózis Ashner 24 hetes vizsgálatában (Aschner és mtsai 2006c), a 100 mg és 200 mg hatékonyságának ezt a kis különbségét a rövidebb 18 hetes vizsgálatban nem figyelték meg Raz (Raz és mtsai 2006c). Ennek oka lehet a tanulmányi időtartam különbségei, valamint a különböző vizsgálati populációk. A szitagliptin maximális jóváhagyott adagja napi 100 mg. A szitagliptin terápiát jól tolerálták, és a hipoglikémia vagy más nemkívánatos események előfordulása nem nőtt (Aschner et al 2006a, 2006b; Raz et al 2006a, 2006b).
HbA1c kialakulása a szitagliptin kombinált terápiáiban, akár metforminhoz, akár pioglitazonhoz adva. A HbA1c fejlődésével kapcsolatos kombinációs vizsgálatok eredményeit a metforminnal végzett 24 hetes vizsgálat (bal oldali panel) (Karasik et al 2006 adatai alapján) és a pioglitazonnal végzett vizsgálat (jobb oldali panel) (Rosenstock és mtsai 2006a adatai alapján).
Rövidítések: Pbo, placebo.
- A zsíros májbetegség és a 2-es típusú cukorbetegség új kezelése zsírégetést okoz a májban - ScienceDaily
- A gyógyszeres kezelés költségeinek és a testtömeg-index közötti összefüggés latinul 2-es típusú cukorbetegségben
- A Tandem Diabetes Control IQ Integrated Diabetes Services áttekintése
- Az α-liponsav szájon át történő kezelése javítja a tünetekkel járó diabéteszes polineuropátia cukorbetegség ellátását
- A Saxenda mint krónikus súlykezelés kezelési lehetősége - a Bariatric Times áttekintése