Hasi kulcs
A leggyorsabb hasi insight motor
- itthon
- Belépés
- Regisztráció
- Kategóriák
- HASONOS GYÓGYSZER
- HEPATOPANCREATOBILIARY
- GASZTROENTEROLÓGIA
- GASTOINESTINAL MŰTÉT
- TÁBORNOK
- NEFROLOGIA
- UROLÓGIA
- Ról ről
- Arany tagság
- További hivatkozások
- Hasi kulcs
- Anesztézia kulcs
- Alapvető orvosi kulcs
- Fül-orr-gégészet és szemészet
- Mozgásszervi kulcs
- Neupsy Key
- Key nővér
- Szülészet, nőgyógyászat és gyermekgyógyászat
- Onkológia és hematológia
- Plasztikai sebészet és bőrgyógyászat
- Klinikai fogászat
- Radiológiai kulcs
- Mellkasi kulcs
- Állatorvoslás
- Kapcsolatba lépni
- Fogászati kulcs
4.6. Fejezet
Dekompenzált májbetegség és táplálkozás
Simran Arora 1, Gillian Gatiss 2, Laura M. McGeeney 2 és Nina C. Powell 2
1 Royal Free London NHS Foundation Trust, London, Egyesült Királyság
2 Cambridge University Hospitals NHS Foundation Trust, Cambridge, Egyesült Királyság
4.6.1 A dekompenzált májbetegség étrendi okai és következményei
A májbetegséget különböző tényezők okozhatják, amint azt a 4.6.1. Táblázat mutatja. Nagyrészt a betegség tünetei és súlyossága határozzák meg a táplálkozási kezelést, nem pedig az etiológiát.
4.6.1. Táblázat: A májbetegségek típusai
| Ok | Májbetegség típusa |
| Fertőzések | Hepatitis A, hepatitis B, hepatitis C, hepatitis D, hepatitis E |
| Mérgező | Alkoholhoz kapcsolódó májbetegségek, gyógyszerek túladagolása, egyéb mérgek |
| Kolesztatikus | Elsődleges szklerotizáló cholangitis, primer biliaris cirrhosis |
| Anyagcsere | Alkoholmentes zsírmájbetegség, alkoholmentes steatohepatitis, örökletes haemochromatosis, alfa-1 antitripszinhiány, Wilson-kór |
| Ér | Budd – Chiari szindróma |
| Egyéb | Cisztás fibrózissal összefüggő májbetegség, autoimmun hepatitis, kriptogén májbetegség |
A máj létfontosságú metabolikus szerepe miatt a funkcióvesztés jelentős táplálkozási következményekkel jár. Az alultápláltság jelentett gyakorisága ebben a populációban az értékelési technikától és a betegség stádiumától függően változik; akár 100% is lehet [1–3]. Az alultápláltság befolyásolja a fontos klinikai eredményeket, beleértve a varicealis vérzés, az encephalopathia, a fertőzések, az ascites, a gyenge izomműködés, a kórházi tartózkodás hossza és a halálozási arányokat [4–7]. A fehérje-energia alultápláltság (PEM) szintje a májbetegség súlyosságától és a betegellátás táplálkozási szintjétől függ, nem pedig az etiológiától.
A PEM-et elősegítő tényezők közé tartozik a csökkent orális bevitel, hányinger, hányás, fájdalom, encephalopathia, korai jóllakottság (ami az ascites nyomásának köszönhető), alkoholelvonás, szájon át történő tesztelés nélküli időszakok, étvágytalanság, tápanyagok és folyadék korlátozások, ínytelen étrend (például nagyon alacsony sótartalmú étrend), megváltozott ízérzet és fáradtság. A PEM-ben szenvedő betegeknek hasmenés vagy steatorrhoea formájában is malabszorpciója lehet kolesztázis, rendszeres laktulóz alkalmazása vagy az antibiotikumokat követő GI mikrobiota változásai miatt, és az energia-anyagcsere változásai miatt megnövekedhet az energia és a fehérje iránti igény.
Metabolikus változások a cirrhosisban
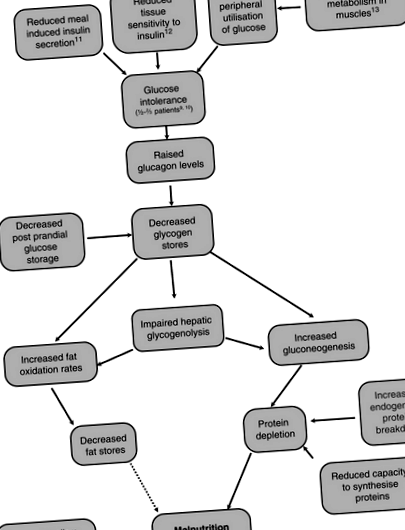
A 4.6.1. Ábra a cirrhosisban szenvedő személynél bekövetkező főbb anyagcsere-változásokat és a közöttük lévő kapcsolatokat mutatja be.
4.6.1. Ábra A fő metabolikus változások, amelyek cirrhosisban szenvednek [7–13].
A májbetegségek alultápláltságát „glikogén tárolási betegségnek” nevezték, mivel még táplált állapotban is alacsonyak a glikogénkészletek [14]. A máj glikogenolízise is károsodott, így a glikogén kevésbé megfelelő üzemanyag a cirrhotikus betegek számára. A vércukor-koncentráció rövid távon történő fenntartása érdekében, amikor a közelmúltban nem vettek be szénhidrátot, megnő az aminosavakból származó glükoneogenezis, ami fehérje kimerülést eredményez [15]. Petersen és mtsai. cirrhotikus alanyokban összehasonlították a glükoneogenezist és a glikogenolízis sebességét, és megfeleltek az egészséges kontrolloknak a magmágneses rezonancia spektroszkópiával és a 2 H 2 O-val, és azt találták, hogy hasonló volt a glükóztermelésük, de a cirrhotikus alanyoknál nagyobb volt a glükoneogenezis és csökkent a glycogenolysis aránya kontrollalanyok [16]. A zsírt alternatív üzemanyagként is használják [17]. A zsír oxidációs sebessége azonban visszatér az újratáplálás után [18].
Közvetett kalorimetriával a zsír, szénhidrát és fehérje teljes energiájának százalékos aránya a kontroll alanyokban 36–72 órás böjt után összehasonlítható volt a cirrhotikus betegeknél az éjszakai böjt (10–12 óra) után tapasztaltal [19]. Ezek az arányok szignifikánsan különböztek az egy éjszakán át éhezett kontrollalanyokétól. Ez azt jelzi, hogy a cirrhotikus betegek sokkal gyorsabban éheznek, mint az egészséges kontrollok; a cirrhosist gyorsított éhezés betegségének nevezik. A fokozott endogén fehérjebontás fokozott fehérjeforgalmat eredményez. A fehérje újraszintézisének sebessége azonban nem növekszik, és a cirrhotikus máj fehérjék szintetizálására és tárolására való képessége csökken, ami izompazarláshoz vezet. Ennek a hipermetabolizmusnak a mechanizmusa nem világos, de úgy gondolják, hogy extrahepatikus, mivel a májtranszplantációt követően több mint egy évig fennáll [20].
Nem minden cirrhotikus beteg hipermetabolikus; olyanok, amelyek izomtömegének százaléka hasonló, mint a normometabolikus cirrhotikus betegeknél, de a testsejtek tömege csökkent (8). Emellett emelték a szérum citokinek szintjét, ami jelzi a gyulladásos válasz lehetséges szerepét a hipermetabolikus állapotban. Greco és mtsai. hypermetabolizmust, megnövekedett lipidoxidációs rátákat és inzulinrezisztenciát mutatott egy éjszakai böjt után Childs B cirrhotikus betegeknél, összehasonlítva az egészséges kontrollokkal [20a]. A betegek testtömeg-indexe (BMI), zsírmentes tömeg és zsírtömeg statisztikailag nem különbözött szignifikánsan az egészséges kontrolltól, ami arra utal, hogy az anyagcsere-változások megelőzik a fogyást, nem pedig annak következményei.
Az izomsorvadás a cirrhosis egyik fő jellemzője lehet, de szakképzett táplálkozási értékeléssel és terápiával ez megelőzhető.
Táplálkozási értékelés
Az alultápláltság jelen lehet a májbetegség korai szakaszában, de ez nem mindig nyilvánvaló, különösen a túlsúlyos embereknél. Részletes táplálkozási értékelésre van szükség az alultáplált vagy annak veszélyeztetettjeinek azonosításához. A tápláltsági állapot pontos felmérése különösen nehéz lehet a cirrhosisban szenvedő betegeknél a megváltozott folyadék homeosztázis miatt. A hagyományos táplálkozás-értékelési módszerek és a táplálkozás-szűrő eszközök gyakran a testsúlyon és a BMI-változáson alapulnak, de ennél a betegcsoportnál specifikusabb tápláltsági állapotmérésekre van szükség.
A táplálékértékelés magában foglalná a tünetek, a kórtörténet, a kórtörténet, a testösszetétel, a biokémia, a részletes étrendi bevitel és a folyadékkorlátozások értékelését. Az olyan tünetek, mint hányinger, étvágytalanság, fájdalom, fáradtság és encephalopathia, akárcsak bármely folyadékkorlátozás, csökkenthetik a táplálékfelvételt. Míg a székrekedés azt eredményezheti, hogy az emberek nagyobb valószínűséggel tapasztalják meg az encephalopathiát, a hasmenés csökkenti a tápanyagok felszívódását, és az embereket is kevésbé hajlandó enni. A kórtörténet, beleértve az együttes betegségeket, mint például a veseelégtelenség, a hepatopulmonáris szindróma vagy a cukorbetegség, potenciálisan hatással lehet a betegek táplálkozási állapotára, valamint az étrendi tanácsadásra. Egy személy társadalmi helyzete, beleértve az anyagi helyzetet, az életkörülményeket, az alkoholt és a tiltott kábítószer-fogyasztást, hatással lesz táplálkozási állapotára. A beteg májfunkciós tesztjeiben bekövetkező változások jelezhetik állapotuk javulását vagy csökkenését; fontos az elektrolitok monitorozása potenciális táplálkozási szindrómás betegeknél, és biokémia is alkalmazható olyan állapotok monitorozására, mint veseelégtelenség.
Az étrend előzményeinek felvételekor különösen fontos figyelembe venni a táplálékfelvétel mintáját, valamint a tápanyagtartalmat és az adagok méretét, különös tekintettel az elfogyasztott szénhidrátok és fehérjék gyakoriságára és mennyiségére. Mint minden más betegcsoportnál, itt is fontos figyelembe venni a betegek preferenciáit és toleranciáit, a napi tevékenységi szokásokat és az esetleges aggályaikat.
A felkar antropometriája
A felkar karjának antropometriáját, a kar középső kerületét (MAC), a tricepsz bőrhajtásának vastagságát (TST) és a közép kar izom kerületét (MAMC) használják a klinikán vagy az osztályon a zsír- és izomraktárak megkülönböztetésére. Ezek a mérések a beteg tápláltsági állapotát mutatják a várható populációhoz képest. A leghatékonyabbak egy betegnél a 3–8. Hetenkénti sorozatmérések, mivel a testzsírnak több kg-mal kell megváltoznia, mielőtt a bőrhajlítással kimutatható lenne [21]. Fontos tisztában lenni a megfigyelők közötti és az intraobserver hibákkal. A megbízhatóság és a pontosság javítható a megfigyelő technikájának szabványosításával vagy speciális antropometriai képzéssel.
A kézi markolat ereje
A kézi tapadás erejét dinamométerrel mérik, és ez az izomfunkció mértéke. A cirrhosisban szenvedő betegeknél a kézfogás alacsony ereje előre jelzi a szövődmények és a gyenge klinikai kimenetelt [22]. A betegek markolatának ereje gyorsabban változik, mint a mért izomtömeg változása, és szükség esetén hetente értékelhető.
Táplálkozási szűrés
Különösen hasznosak lehetnek azok az eszközök, amelyek több forrásból származó információt strukturált módon foglalnak magukban a beteg számára. A Royal Free Hospital Global Assessment (RFH-GA), amely a BMI-t (a becsült száraz testtömeg alapján számolva), a MAMC-t, az étrendi bevitelt és a tüneteket használja egy algoritmusban [23], nagyon jó interszerveren belüli és interobserver reprodukálhatósággal rendelkezik, és ebben a betegcsoportban érvényesítették. [24]. Ennek az értékelésnek a pontos felhasználása speciális képzést igényel, és egy óra is eltelhet. A közelmúltban fejlesztették és validálták a Royal Free Hospital Nutritional Prioritizing Tool-ot (RFH-NPT). Ennek nagyon jó intra- és interobserver reprodukálhatósága van, diagnosztikai érzékenysége 100%, specifitása 73% [25]. 2-3 perc és kevés edzés szükséges a teljesítéshez, de kevésbé részletes értékelést ad, mint az RFH-GA. Ez az eszköz magában foglalja az ascites és/vagy az ödéma jelenlétét/hiányát, a választól függően különböző kérdésekkel.
Száraz tömeg
A 4.6.2. Táblázat felhasználható a folyadék tömegének becslésére és ezért a száraz tömeg kiszámítására. Az ascites és a perifériás ödéma becsült súlyát kivonják a beteg „nedves súlyából”. A betegek 14 kg-nál nagyobb ascitic térfogatúak lehetnek. Még ascites és ödéma nélküli betegeknél is egyedül a súly a táplálkozási állapot nyers mértéke, mivel nem tesz különbséget a zsír- és izomraktárak között. Aszcites betegeknél, akiknek rendszeres paracentézisük van, hasznos megfigyelni a száraz test becsléseit, hogy az egyes paracentézisek során mennyi folyadék távozik, mennyi folyadék marad a paracentézis után, a tipikus posztparacentézis súly és az utolsó paracentézis óta eltelt idő súly.
4.6.2. Táblázat Az ascites és a perifériás ödéma súlyának becslése [26]
| Ascites | Perifériás ödéma | |
| Minimális | 2,2 kg | 1,0 kg |
| Mérsékelt | 6,0 kg | 5,0 kg |
| Szigorú | 14,0 kg | 10,0 kg |
Sokszorosítva Taylor & Francis engedélyével.
Táplálkozási követelmények
Ha a máj glükóz felszabadulásának fenntartása érdekében a glükoneogenezist alkalmazzák, nem pedig a glikogenolízist, akkor mind a nyugalmi energia ráfordítás (REE), mind a fehérjeszükséglet növekszik [19,27]. A glükoneogenezis több energiát használ fel, mint a glikogenolízis, és aminosavakat igényel szubsztrátként, ezért mind a cirrhotikusok energia-, mind a fehérjeigénye megnő. A májbetegségben szenvedők megnövelhetik bevételeiket a raktárakban [28,29]. Az Európai Parenterális és Enterális Táplálkozási Társaság (ESPEN) irányelvei 25–40 kcal/testtömeg-kg-ot céloznak meg, de hogy száraz, tényleges vagy ideális testsúlyt alkalmaznak-e, nem egyeztettek (4.6.3. Táblázat) [30]. Ha a beteg alultáplált, kivéve, ha nyíltan kritikusan beteg vagy szeptikus, napi 400–1000 kcal hozzáadása javasolt az üzletek feltöltésének elősegítése érdekében.
4.6.3. Táblázat: Májbetegek energia- és fehérjeszükséglete
| Stressz tényező a | Energia kcal/kg dBW/nap | Fehérje g/kg dBW/nap | |
| Kompenzált | 0–20% | 25–35 | 1.2–1.3 |
| Dekompenzált | 30–40% | 35–40 | 1.2–1.5 |
| Akut (fulimáns) | 20–30% | | 1.2–1.5 |
| Transzplantáció után (kb. 1 hónap) | 30% | | 1.2–1.5 |
Az Egyesült Királyságban az energia (a testsúly fenntartásához) és a fehérjeszükséglet dBW-t (száraz testtömeg) használ [30,31].
a A stressz tényezőt alkalmazzák a további metabolikus stressz kiigazítására, és megszorozzák az alap metabolikus sebességgel vagy az egyes állapotok testtömegével számított fajlagos kcal/kg-mal [30].
Elsevier engedélyével reprodukálva.
A sovány testtömeg (LBM) fehérjetartalékai kimerülnek az aminosavak glükóztermeléshez való felhasználásával, ezért az LBM fenntartásához és pótlásához extra étrendi fehérje szükséges. Swart és mtsai. radiojelzett [15 N] glicint használt a nitrogénáramlás, a fehérjeszintézis és a fehérjebontás sebességének vizsgálatára cirrhosisban szenvedő és egészséges kontrolloknál, és azt javasolta, hogy a cirrhotikus betegeknél a nitrogén bevitelének növelésére van szükség a pozitív nitrogénegyensúly eléréséhez a glükoneogenezis növekedése miatt 29.] A fehérjeszükségletet a beteg becsült száraz súlya alapján számítják ki, és a 4.6.3. Táblázat mutatja.
A pácienseknek, különösen otthon és mobilon, az izomraktárak feltöltése vagy fenntartása érdekében szükség lehet a bevitt mennyiségek növelésére ezen számított követelmények felett. Fontos, hogy rendszeresen ellenőrizzék táplálkozási állapotukat, és ennek megfelelően módosítsák étrendi ajánlásaikat.
Elhízott betegeknél a fehérje- és energiaigényt kiigazítják a megnövekedett testtömeg és a metabolikusan aktív szövet valószínűleg csökkent százalékos arányának figyelembe vétele érdekében. Az Egyesült Királyságban a fehérje- és az energiaigény napi 25% -kal, illetve 400–1000 kcal-kal csökken. Az ilyen módosítások során fontos, hogy a betegeket rendszeresen ellenőrizzék, hogy a táplálkozási állapot bármilyen csökkenése azonosítható és enyhíthető legyen. Az izomműködés megőrzése és a beteg alkalmassága elsőbbséget élvez a zsírtömeg csökkentésére irányuló célokkal szemben. Az ESPEN irányelvek nem adnak útmutatást kifejezetten az elhízott májbetegek számára.
A folyadékigényt ritkán becsülik előre meghatározott számítások alapján, de egyénileg és a beteg folyadékállapotától függően.
4.6.2 A máj encephalopathia étrendi okai
A hepatikus encephalopathia (HE) oka valószínűleg multifaktoriális, és még mindig nem teljesen ismert. Következésképpen az étrendi manipuláció HE-ben úgy alakult, hogy a bizonyítékok nagyobb szintje alátámasztja vagy cáfolja az elméleteket. Az okok egyik első elmélete az volt, hogy az étkezési fehérje májelégtelenségben okozza a HE-t. Ennélfogva az étkezési fehérje korlátozásának történetileg azt javasolták, hogy csökkentsék a kockázatot és megkönnyítsék a HE kezelését [32]. Ezt már nem javasoljuk, mivel a fehérjeforgalmi vizsgálatok kimutatták, hogy a fehérjeszükséglet és a teljes energiaigény a végstádiumú májelégtelenség kialakulásával növekszik [3,33]. A bevitel korlátozása izomkatabolizmushoz és az ezzel járó rossz eredményekhez vezethet ezeknél a betegeknél [34].
Úgy gondolják, hogy a további táplálékfehérje szükségességét az elágazó láncú aminosavak (BCAA) felhasználása a májkárosodás kijavítására vagy azok ammónia ártalmatlanítására történő felhasználására irányítja [35], csökkentve a BCAA és a BCAA arányát. az aromás aminosavak. Továbbá, ha a további kalóriaigény nem teljesül, az izomfehérje lebontása növeli az aromás aminosavak (fenilalanin, tirozin) keringő koncentrációját a keringő BCAA (leucin, izoleucin, valin) koncentrációihoz képest. Végül az aromás aminosavak és a BCAA nagyobb aránya megkönnyíti az aromás aminosavak mozgását a vér-agy gáton, megváltoztatva a HE-vel kapcsolatos mentális állapotot. Ezt az elméletet támasztja alá az emésztőrendszeri vérzést követő HE kialakulása. Javasoljuk, hogy a vér emésztése, amelyben hiányzik az elágazó láncú izoleucin, egy elágazó láncú aminosav, megváltoztatja az aromás aminosavak és a BCAA arányát, ami akut HE-t okoz [36].
A gyomor-bélrendszeri ammónia magas koncentrációja egy másik elmélet a HE okára. A böjt időszakaiban az izmokból származó aminosavak felhasználása a glükoneogenezishez ammóniát termel. A keringő ammóniát az izomszövet eltávolítja, ezért az izomvesztés önmagában súlyosbíthatja a HE fejlődését [37]. Úgy gondolják, hogy az étrendi tényezők, amelyek megváltoztathatják a gyomor-bél mikrobiotáját és csökkenthetik az ammóniatermelés magas koncentrációját, csökkentik a kockázatot és megkönnyítik a HE kezelését. Az ebben a folyamatban vizsgált étrendi tényezők közé tartozik a laktulóz, a probiotikumok, a növényi fehérje és a cink.
4.6.3 Az ascites táplálkozási következményei
Az ascitic térfogatát általában enyhe, mérsékelt vagy súlyosként definiálják (lásd 4.6.2. Táblázat), de egyes betegeknél meghaladhatja a 25 litert. A mérsékelt vagy súlyos ascites káros hatással lehet a táplálkozási állapotra, több tényező miatt (4.6.1. Háttérmagyarázat).
- Diéta és táplálék a hasi tapadásokhoz - a hasi egészség
- Diéta és táplálkozás a máj egészségéért - A mai Dietetikus Magazin
- Diet for Cirrhosis (NASH) portál hipertónia, portál vénatrombózis - májbetegség - Inspire
- Macska májbetegség Mit kell tudni Hill; s Pet
- Az alacsony hozzáadott cukortartalmú étrend jelentősen javítja a gyermekek zsírmáj betegségét - ScienceDaily