A mellékvese Cortex hiperfunkciója
A hiperadrenokortikizmus izomsorvadást (atrófiát) és gyengeséget okoz a Cushing-kórban szenvedő kutyáknál és lovaknál, valamint a kortikoszteroidok beadását követően (Braund et al., 1980a, 1980b;
Kapcsolódó kifejezések:
- Neoplazma
- Diabetes mellitus
- Agyalapi
- Adrenokortikotrop hormon
- Hidrokortizon
- Elhízottság
- Kortikotropin
- Alkalikus foszfatáz
Letöltés PDF formátumban
Erről az oldalról
Szisztémás vagy multifokális jelek
Michael D. Lorenz BS, DVM, DACVIM,. Marc Kent DVM, BA, DACVIM, az Állatorvosi Neurológia Kézikönyvében (Ötödik kiadás), 2011
Hyperadrenocorticismus
Hyperadrenocorticismus (Cushing-betegség/szindróma) kutyáknál, lovaknál és macskáknál jelentkezik. Kutyáknál és lovaknál a hipofízis adenoma, amely hiperszekretálja az adrenokortikotrop hormont (ACTH), a leggyakoribb ok, de a funkcionális kortizolt szekretáló mellékvese daganatok ezt a szindrómát is előidézik kutyákban és macskákban. A klinikai tüneteket a hiperkortizolémia metabolikus hatása okozza. A glükokortikoidok katabolikus hatásaiból eredő általános izomgyengeség gyakori megállapítás. Egyes kutyáknál izomdegeneráció alakul ki, amelyet szteroidok által kiváltott myopathiának neveznek (lásd 7. és 10. fejezet, 7. fejezet, 10. fejezet). Ez az állapot spontán izomösszehúzódásokat (pseudomyotonia) és merev járást eredményez.
Az agyalapi mirigy adenoma (macroadenoma) neurológiai jeleket hozhat létre a növekedés és a hipotalamuszba való terjeszkedés révén (lásd 15-5. Ábra, A-tól C-ig). Az agyalapi mirigy macroadenomáinak jelei általában homályosak, és depressziót, zavartságot, körözést, ataxiát és görcsrohamokat tartalmaznak. 57 A macroadenomák gyakoribbak az idősebb, nagy fajtájú kutyáknál. Hyperadrenocorticismusokat okozó hipofízis daganatok jelen lehetnek anélkül, hogy neurológiai tüneteket okoznának. 57
Endokrin rendszer
Hyperadrenocorticismus (Cushing-szindróma vagy betegség)
A hiperadrenokortikizmus idősebb kutyáknál viszonylag gyakori, macskáknál egyre inkább elismert, más háziállatoknál ritka. A jatrogén hiperadrenokortikizmus a glükokortikoid terápia eredménye, amely csökkent ACTH szekréciót és adrenokortikális atrófiát eredményez. A spontán Cushing-szindróma ezzel szemben általában hiperplasztikus vagy neoplasztikus adenohypophysealis (hipofízis elülső mirigy) kortikotrófok által okozott ACTH-szekréció eredménye, amely bilaterális, diffúz vagy multifokális adrenokortikális hiperpláziát okoz, különösen a zona fasciculata-ban (lásd 12–17. Ábra, A és C, valamint 12-35). A funkcionális adrenokortikális adenomák vagy karcinómák (lásd 12-37. Ábra) a kutya Cushing-szindróma kevésbé gyakori okai. A hiperadrenokortikalizmus patogenezisének meghatározásához a bazális plazma kortizolkoncentrációt összehasonlítjuk a dexametazon szuppresszió és az ACTH stimuláció után mért koncentrációval.
A fokozott glükoneogenezis, lipogenezis és fehérje katabolizmus számos klinikai tünetet és elváltozást magyaráz. A vázizom atrófiája függő hasat eredményez (lásd 12-36. Ábra). A hepatomegáliát a lipid és a glikogén megnövekedett lerakódása okozza (szteroid hepatopathia; lásd 8-78. Ábra). A bőrelváltozások kezdetben a kopás pontjain (pl. Nyak, szárak vagy a fül mögött) vagy a csontos kiemelkedéseken fejlődnek ki, majd kétoldali szimmetrikus mintázatban terjednek a testfelület nagy részének bevonásával (lásd: 12-36., 17-74. és 17-75). A hypercortisolismus bőrelváltozásai közé tartozik az epidermisz és a pilosebaceus egységek sorvadása, a bőr kollagénje és az elasztin elvesztésével. A calcinosis cutisban, amely a hiperadrenokortikális kutyák legfeljebb 30% -ában jellemző elváltozás, a kalciumkristályok a bőr kollagén és elasztin rostjai mentén rakódnak le, és behatolhatnak az atrófiás epidermiszbe vagy a follikuláris hámba. Ez a bőr meszesedés valószínűleg összefügg a kortizol glikoneogén és fehérje katabolikus hatásával, amely a kollagén és az elasztin molekuláris átrendeződését eredményezi egy olyan mátrix kialakulásával, amely vonzza a kalciumot. A kalcium más szövetekben is elhelyezhető, például a tüdőben, a vázizomban és a gyomorban.
A csontváz izomfunkciója
1 Kortikoszteroid myopathia
A hiperadrenokortikizmus izomsorvadást (atrófiát) és gyengeséget okoz a Cushing-kórban szenvedő kutyáknál és lovaknál, valamint a kortikoszteroidok beadását követően (Braund et al., 1980a, 1980b; Duncan et al., 1977); (Aleman és mtsai, 2006). Az izomsorvadás a 2-es típusú miofiberek meglehetősen szelektív anguloid és angularis atrophiájának köszönhető; kvantitatív vizsgálatok azonban az 1. típusú szálak atrófiáját is feltárják. A myotonia ennek a rendellenességnek a változó kísérő jele (Duncan et al., 1977). Az izomsorvadás a fehérjeszintézis megváltozott transzkripciója által közvetített katabolizmusnak köszönhető, amely a csökkent fehérjeszintézissel és fokozott fehérjebontással jár.
Glükokortikoidok és az öregedő agy: ok vagy következmény?
Paul J. Lucassen, E. Ron De Kloet, az öregedés funkcionális neurobiológiájában, 2001
1. Funkcionális változások
Korábbi tanulmányok már kimutatták, hogy a GC-k egy GR által közvetített mechanizmus révén hatnak a hippocampus neuronokba jutó feszültségfüggő kalcium beáramlás növelésére. A hiperkortikizmus elhúzódó és megnövekedett kalciumfüggőséget vált ki hiperpolarizációk, csökkentett küszöbértékek gerjesztő posztszinaptikus potenciálok (EPSP) kiváltására, csökkent EPSP amplitúdók és összességében megnövekedett kalciumáramok, minden feltétel tudja, hogy gátolja a megfelelő szinaptikus transzmissziót. A megváltozott kalciumszabályozás jelentőségét az öregedésben az idős állatokban megfigyelt változások is alátámasztják, amelyek idegsejt-degenerációval társulnak, az intracelluláris kalciumpufferelésben szerepet játszó tényezőkben, például a kalbindin, a kalretinin, a calmodulin stb. a kalciumfüggő protein-kinázok változásához (Fordyce és Wehner, 1993a, b; Colombo és mtsai, 1997; Krugers és mtsai, 1997b). Az intracelluláris kalcium farmakológiai manipulációja továbbá bebizonyosodott, hogy hatással van a megismerés szempontjainak befolyásolására az idős agyban (Landfield et al., 1978, 1981; Joëls és de Kloet, 1989; Kerr et al., 1991; Nair et al., 1998; Vekhratsky és Toescu, 1998).
A glükokortikoidok befolyásolják a memória kialakulásának elektrofiziológiai modelljét, a hosszú távú potenciálozást (LTP) is. Érdekes módon úgy tűnik, hogy ez U-alakú dózis-válasz összefüggést is követ, mivel a hippocampus szeletekben a hosszú távú potencírozási válasz csak akkor károsodik, ha a GC-koncentrációk túl magasak vagy túl alacsonyak (Joëls és De Kloet, 1992; De Kloet et al., 1999). Az idős patkányok hippocampusában képtelenség LTP-t létrehozni ezen állatok aberrált, magas GC-kitettségének tulajdonítják (Kerr et al., 1991). A GC-k hasonló dózis-válasz viszonyban vannak olyan feszültségfüggő ionvezetéseknél, mint a kalcium és a szerotonin la-receptor által közvetített hiperpolarizáció (Joëls és De Kloet, 1992; Joëls, 1997; De Kloet és mtsai, 1998).
Reproduktív és endokrin toxikológia
11.13.5.2 Az adrenokortikális hiperaktivitás feltételei
A Cushing-szindrómának nevezett hiperadrenokortikizmus a mellékvesekérgi túlsúly leggyakoribb állapota. Ez az állapot lehet agyalapi mirigy-független, ha a mellékvese autonóm módon termeli a glükokortikoidok feleslegét, vagy lehet agyalapi mirigy-függő, ha az agyalapi mirigy ACTH-t termel. A glükokortikoid túlsúlyának tipikus „cushingoidi” tünetei közé tartozik a központi elhízás vagy súlygyarapodás, magas vérnyomás, vékony bőr, gyenge sebgyógyulás, diszlipidémia, osteopenia és izomgyengeség (az áttekintéseket lásd Holt és Hanley 2008; Newell-Price et al. 2006). A farmakotoxikológiailag kiváltott állapotok közé tartozik a túlzott alkoholfogyasztásból eredő „pseudo-Cushing-szindróma”, amely az embereknél kortizol hiperszekréciót eredményezhet (lásd Holt és Hanley 2008), és mint korábban említettük, az iatrogén Cushing-szindróma a hosszú távú glükokortikoid gyakori mellékhatása. terápia. Holt és Hanley (2008) az adrenokortikális felesleg egyéb körülményeit is tárgyalja, beleértve a hiperaldoszteronizmust (Conn-szindróma) és a veleszületett mellékvese hiperpláziát, amelyet a CYP21 inaktiválása okoz (ami elsősorban a mellékvese-kéreg androgéntermelésének feleslegét okozza, de glükokortikoid elégtelenséget is eredményezhet az úgynevezett virilizálásban és sóban hulladék formák).
Az egyik általános szempont, hogy különféle farmakológiai vegyületeket fejlesztenek ki az adrenokortikális enzimek, különösen a CYP17 és a CYP11B megcélzására (Hakki és Bernhardt 2006), bizonyos hiperaktivitási szindrómák kezelésére. Ez azt is bizonyítja, hogy a mellékvese egyre nagyobb szerepet játszik a farmakológiában és a toxikológiában, valamint azt, hogy a vegyületek specifikusan szintetizálhatók a szteroidogén folyamatok megzavarása érdekében, ezért a szerkezet-aktivitás kapcsolatok kialakulnak. Harvey és munkatársai irodalmi elemzése. (2007, 2008) több mint 70 vegyületet sorol fel, amelyekről beszámoltak arról, hogy befolyásolják a szteroidogenezist és az általuk befolyásolt molekuláris célpontokat, ezek közé tartozik a környezeti szennyezők, a mezőgazdasági vegyi anyagok, a fogyasztói vegyi anyagok (pl. Alkohol) és a gyógyszerek széles skálája. Ez felveti a kérdést, hogy az alacsony szintű környezeti expozíció hajlamosíthatja-e az emberi populáció bizonyos szektorait a mellékvese állapotok kialakulására, és ezt a következő szakasz tárgyalja tovább.
Adrenokortikális funkció
A rutin laboratóriumi diagnosztika
A hypoadrenocorticismusban és a hyperadrenocorticismusban is számos olyan kóros laboratóriumi eredmény található, amelyek gyakoribbak, mint más betegségeknél. Ezen rendellenességek közül sok a glükokortikoidok és az mineralokortikoidok fent leírt hatásából származhat (II.F. szakasz). A lényegeket itt foglaljuk össze.
Az elsődleges hipoadrenokortikizmusban a csökkent aldoszteron termelés hiponatrémiát és hiperkalémiát eredményez. A kapcsolódó hypovolemia prerenalis urémiához vezet. A hiperadrenokortikális betegségben a klasszikus hematológiai rendellenesség az eozinopénia, amely társulhat limfopéniával, esetenként leukocitózissal és eritrocitózissal. Gyakori biokémiai rendellenesség az alkalikus foszfatáz megemelkedett plazmakoncentrációja (Eckersall és Nash, 1983), amely az alanin-aminotranszferáz (ALT) enyhe emelkedésével együtt fordulhat elő. Ezenkívül hiperglikémia, hiperlipidémia és alacsony tiroxin-koncentráció figyelhető meg. A vizelet-fajlagos súly általában alacsony, az esetek 5-10% -ában glükózuria található.
Ezen rendellenességek közül a megemelkedett alkalikus foszfatáz (AP) koncentráció a leggyakoribb laboratóriumi rendellenesség azoknál a kutyáknál, akiknél kortikoszteroidfelesleg van (akár exogén, akár endogén). Ez a növekedés egy specifikus izoenzim indukciójának köszönhető, amelynek 65 ° C-on nagyobb hőstabilitása van, mint más AP-izoenzimeknek (Teske és mtsai., 1986), ezért rutin laboratóriumi eljárással könnyen mérhető. A kórosan magas AP-65 ° C-érték utalhat a hyperadrenocorticismusra, de alacsony specifitása miatt nem alkalmas diagnosztikai tesztként (Teske és mtsai., 1989). A hiperadrenokorticizmusban megfigyelhető alacsony tiroxin (T4) koncentráció a plazmában a T4 transzportjának, eloszlásának és anyagcseréjének megváltozásának következménye, nem pedig a hiposzekréció eredménye (Rijnberk, 1996).
Más rendellenességek is okozhatják ezeket a rendellenességeket, és egyes esetekben nincsenek jellemző rutin laboratóriumi jellemzők. Ezért elengedhetetlen a mellékvesekéreg működésének vizsgálatához általánosan használt specifikus laboratóriumi vizsgálatok részletes megértése. Ezenkívül a hiperadrenokortikalizmus spontán formái az agyalapi mirigy ACTH túltermeléséből vagy az adrenokortikális daganatok autonóm hiperszekretálásából eredhetnek. Ezek mindegyike más-más kezelési módot igényel, ezért a differenciáldiagnózisban alkalmazott tesztek bepillantása elsődleges fontosságú.
A csont átalakításának központi ellenőrzése
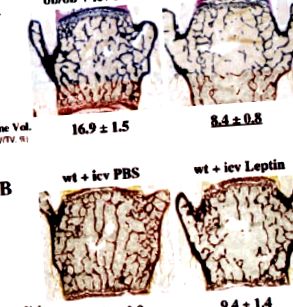
B. Leptinhiány és csont egerekben
Kóros biomarkerek a toxikológiában
Meliton N. Novilla,. Stewart B. Jacobson, Toxikológiai biomarkerek, 2014
Endokrin alopecia
Az endokrin alopecia kutyák iatrogén hyperadrenocorticismusából vagy hyperestrogenismusából származhat glükokortikoidok vagy ösztrogének beadása miatt. További jelentett okok az agyalapi mirigy daganata által szekunder bilaterális adrenocorticalis hyperplasia, a hyperadrenocorticismus és a hyperestrogenismus funkcionális adrenocorticalis hyperplasticus göbje vagy neoplazma, a nők petefészekciszta és a hímivarú herék funkcionális Sertoli sejtdaganata (Hargis és Ginn, 2006). A hiperadrenokortikális kutyáknál truncalis alopecia van, megkímélve a fejet és a végtagokat, kitágult hasat és vékony bőrt.
A hipestrogenizmusban a durva eredmények szimmetrikus alopeciát és hiperpigmentációt jelentenek a hátsó törzsön és a végtagokon (54.2. Ábra). Ezenkívül a hím kutyáknál függő előmellékhatás, a mellbimbók és a prosztata megnagyobbodása alakulhat ki, míg a nőstény kutyáknál megnagyobbodott a vulva és az abnormális ivarzási ciklus. Szövettanilag az epidermisz, a dermis és a szőrtüszők atrófiásak, a follikuláris hyperkeratosis és a calcinosis cutis a hyperadrenocorticismusban, míg az epidermis és a follikuláris hyperkeratosis és a follikuláris atrófia a hyperestrogenismusban figyelhető meg. A glükokortikoidok vagy az ösztrogén iatrogén expozíciójának története, a klinikai és morfológiai megállapításokkal együtt alátámasztja az endokrin alopecia diagnózisát.
54.2. Ábra Hiperestrogenizmus, iatrogén diethylstilbestrol, kutya.
(Reprodukálva az állatorvosi betegségek patológiai alapjairól, 4. kiadás, 17-69. Ábra, 123. o. Academic Press/Elsevier).
- Bariatric Surgery - áttekintés a ScienceDirect témákról
- Cékla - áttekintés a ScienceDirect témákról
- Anthelmintikus - áttekintés a ScienceDirect témákról
- Anorexia Nervosa - áttekintés a ScienceDirect témákról
- Anális sipoly - áttekintés a ScienceDirect témákról